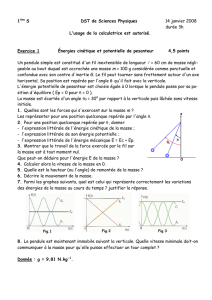
TMS nH2 = 1,98 mol TMS mHg = 602 g

Page 1 sur 14
CORRIGÉ
Feuille d’exercices #1 en chimie
LA RÉVISION DE SEC 4
1- Inscrire le numéro atomique des 20 premiers éléments du tableau périodique, accompagné de
leur symbole chimique et de leur masse atomique arrondie aux centièmes.
#
atmq
symbole
masse
#
atmq
symbole
masse
#
atmq
symbole
masse
#
atmq
symbole
masse
1
H
1,01
6
C
12,01
11
Na
22,99
16
S
32,07
2
He
4,00
7
N
14,01
12
Mg
24,31
17
Cl
35,45
3
Li
6,94
8
O
16,00
13
Al
26,98
18
Ar
39,95
4
Be
9,01
9
F
19,00
14
Si
28,09
19
K
39,10
5
B
10,81
10
Ne
20,18
15
P
30,97
20
Ca
40,08
2- Convertir ces quantités de gramme à mole et vise versa. Inclure une démarche complète
avec les unités de mesure. ATTENTION!!! Il y a des # supplémentaires. Bien vérifier si
la substance chimique coordonne!!
4,00 g de H2
RÉSUMÉ RÉSOLUTION
M = 2,02 g/mol 1- M = m
nH2 = ? nH2
m = 4,00 g 2- 2,02 g/mol = 4,00 g
3,00 mol
3- nH2 = 4,00 g
2,02 g
mol
4- nH2 = 1,98 mol
TMS nH2 = 1,98 mol
3,00 moles de Hg
RÉSUMÉ RÉSOLUTION
M = 200,59 g/mol 1- M = mHg
mHg = ? n
n = 3,00 mol 2- 200,59 g/mol = mHg
n
3- mHg = 200,59 g x 3,00 mol
mol
4- mHg = 601,77 g
TMS mHg = 602 g

Page 2 sur 14
2a) 82,00 g de N2
RÉSUMÉ RÉSOLUTION
M = 28,02 g/mol 1- M = m
nN2 = ? nN2
m = 82,00 g 2- 28,02 g/mol = 82,00 g
nN2
3- nN2 = 82,00 g
28,02 g
mol
4- nN2 = 2,93 mol
TMS nH2 = 2,926 mol
b) 2,5 moles de NH4Cl
RÉSUMÉ RÉSOLUTION
M = 53,50 g/mol 1- M = mNH4Cl
mNH4Cl = ? n
n = 2,5 mol 2- 53,50 g/mol = mNH4Cl
2,5 mol
3- mNH4Cl = 53,50 g x 2,5 mol
mol
4- mNH4Cl = 133,75 g
TMS m
NH4Cl
= 13 x 10 g
35 g de NaCl
RÉSUMÉ RÉSOLUTION
M = 59,44 g/mol 1- M = m
nNaCl = ? nNaCl
m = 35 g 2- 58,44 g/mol = 35 g
nNaCl
3- nNaCl = 35 g
58,44 g
mol
4- nNaCl = 0,60 mol
TMS n
NaCl
= 0,60 mol

Page 3 sur 14
3,4 moles de KOH
RÉSUMÉ RÉSOLUTION
M = 56,11 g/mol 1- M = mKOH
mKOH = ? n
n = 3,4 mol 2- 56,11 g/mol = mKOH
3,4 mol
3- mKOH = 56,11 g x 3,4 mol
mol
4- mKOH = 190,77 g
TMS m
KOH
= 19 x 10 g
2 c) 300,27 g de CaCO3
RÉSUMÉ RÉSOLUTION
M = 100,09 g/mol 1- M = m
nCaCO3 = ? nCaCO3
m = 300,27 g 2- 100,09 g/mol = 300,27 g
nCaCO3
3- nCaCO3 = 300,27 g
100,09 g
mol
4- nCaCO3 = 3 mol
TMS n
CaCO3
= 3,0000 mol
d) 1,5 moles de Na2S2O3
RÉSUMÉ RÉSOLUTION
M = 158,12 g/mol 1- M = mNa2S2O3
mNa2S2O3 = ? n
n = 1,5 mol 2- 158,12 g/mol = mNa2S2O3
1,5 mol
3- mNa2S2O3 = 158,12 g x 1,5 mol
mol
4- mNa2S2O3 = 237,18 g
TMS m
Na2S2O3
= 24 x 10 g

Page 4 sur 14
2 e) 260,00 g de CoCl2
RÉSUMÉ RÉSOLUTION
M = 129,83 g/mol 1- M = m
nCoCl2 = ? nCoCl2
m = 260,00 g 2- 129,83 g/mol = 260,00 g
nCoCl2
3- nCoCl2 = 260,00 g
129,83 g
mol
4- nCoCl2 = 2,00 mol
TMS n
CoCl2
= 2,0026 mol
f) 0,34 mole de PbNO3
RÉSUMÉ RÉSOLUTION
M = 269,21 g/mol 1- M = m PbNO3
mPbNO3 = ? n
n = 0,34 mol 2- 269,21 g/mol = m PbNO3
0,34 mol
3- mPbNO3 = 269,21 g x 0,34 mol
mol
4- mPbNO3 = 91,53 g
TMS m
PbNO3
= 92 g
g) 99,11 g de H2O
RÉSUMÉ RÉSOLUTION
M = 18,02 g/mol 1- M = m
nH2O = ? nH2O
m = 99,11 g 2- 18,02 g/mol = 99,11 g
nH2O
3- nH2O = 99,11 g
18,02 g
mol
4- nH2O = 5,5 mol
TMS n
H2O
= 5,5000 mol

Page 5 sur 14
2 h) 0,06 mole de C12H22O11
RÉSUMÉ RÉSOLUTION
M = 342,34 g/mol 1- M = mC12H22O11
mC12H22O11 = ? n
n = 0,06 mol 2- 342,34 g/mol = mC12H22O11
0,06 mol
3- mC12H22O11 = 342,34 g x 0,06 mol
mol
4- mC12H22O11 = 20,54 g
TMS m
C12H22O11
= 2 x 10 g
3- Trouver la masse en grammes de (avec démarche complète et unités de mesure):
ATTENTION!!! Il y a des # supplémentaires. Bien vérifier si la substance chimique coordonne!!
a) 3,01 x 1023 molécules de O2
RÉSUMÉ RÉSOLUTION
NA = 6,022 x 1023 moléc/mol 1- n = Nmoléc
M = 32,00 g/mol NA
Nmoléc = 3,01 x 1023 moléc 2- mO2 = Nmoléc
mO2 = ? M NA
3- mO2 = 3,01 x 1023 moléc
32,00 g/mol 6,022 x 1023 moléc/mol
4- mO2 = 3,01 x 1023 moléc x 32,00 g
mol
6,022 x 1023 moléc
mol
5- mO2 = 15,99 g
TMS mO2 = 16,0 g
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%