Os et thérapies moléculaires ciblées : nouveaux agents* Bone

Journal Identification = MET Article Identification = 0447 Date: June 25, 2014 Time: 9:0 am
Synthèse
mt 2014 ; 20 (2) : 118-24
Os et thérapies
moléculaires ciblées :
nouveaux agents*
Bone targeted therapies: new agents
Claire Barth1, Christophe Massard2, Stéphane Vignot3
1Service d’Oncologie, Hôpital Henri Mondor, 51 Avenue du Maréchal de Lattre de
Tassigny, 94010 Créteil, France
2Gustave-Roussy, département de médecine, 114, rue Édouard-Vaillant, 94805 Villejuif
cedex, France
3Service Oncologie et Hématologie, Hôpital Louis Pasteur, 4 rue Claude Bernard, 28000
Chartres Le Coudray, France
<svignot@ch-chartres.fr>
Le développement des bisphosphonates et des agents anti-RANK/RANKL a été associée à
une meilleure compréhension des processus physiologiques et pathologiques du remodelage
osseux. De nouveaux agents ont ensuite été développés dans l’optique du ciblage de facteurs
associés à l’ostéoclastogenèse (TGF, PTHrP), de voies de signalisations activées au cours
du remodelage osseux (Src, Cathepsin K) ou des processus de dissémination (homing) des
cellules tumorales dans l’os (chemokines). Cette revue propose de présenter le rationnel sous-
jacent pour ces différentes pistes ainsi que les résultats cliniques disponibles. Les perspectives
d’émergence de nouveaux agents ciblant le remodelage osseux sont ainsi discutées.
Mots clés : remodelage osseux, thérapies moléculaires ciblées
The development of bisphosphonates and anti-RANK/RANKL agents was associated with a
better understanding of physiological and pathological processes of bone remodeling. New
agents are now developed in this context targeting factors associated with osteoclastogenesis
(TGF, PTHrP), with signaling pathways activated during bone remodeling (Src, Cathepsin K)
or with tumor cells homing into bone (chemokines). This review aims to present the underlying
rationale for these developments as well as the clinical results. The emergence of new bone
targeting therapies is discussed.
Key words: bone targeted therapies
Bisphophonates puis inhibiteurs
RANK/RANL peuvent être consi-
dérés comme les premiers agents
d’une nouvelle classe thérapeutique
en oncologie, les inhibiteurs de
remodelage osseux (ou bone targeted
therapies en version anglo-saxonne).
Cette définition peut se justifier à la
lumière de l’activité de ces agents sur
les complications liées aux lésions
métastatiques osseuses mais aussi
sur le traitement de l’ostéoporose.
La meilleure compréhension des
processus physiologiques et patho-
logiques du remodelage osseux [1]
ouvre également de nouvelles pers-
pectives afin de chercher à cibler
des facteurs associés à la promotion
de l’ostéoclastogenèse (Transforming
Growth Factor ˇ[TGF], Parathyroid
hormone-related peptide [PTHrP])
ou des voies de signalisations acti-
vées au cours du remodelage osseux
(Src, Cathepsin K). Une autre piste
repose sur le ciblage des proces-
sus de dissémination (homing) des
cellules tumorales dans l’os (chemo-
kines) dans l’optique de développer
alors des agents agissant sur les
mécanismes supposés de la diffusion
∗Paru dans Bull Cancer 2013 ; 100 : 1215-21. doi : 10.1684/bdc.2013.1834.
Reproduit avec l’autorisation du comité de rédaction.
doi:10.1684/met.2014.0447
mt
Tirés à part : S. Vignot
118
Pour citer cet article : Barth C, Massard C, Vignot S. Os et thérapies moléculaires ciblées : nouveaux agents. mt 2014 ; 20 (2) : 118-24 doi:10.1684/met.2014.0447
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Journal Identification = MET Article Identification = 0447 Date: June 25, 2014 Time: 9:0 am
métastatique (seed and soil targeted therapies). Pour cha-
cune de ces pistes, se pose la question du développement
optimal de ces agents en soulignant la difficulté de définir
les populations cibles pour les études cliniques (activité
sur les lésions osseuses existantes ? Prévention de la dis-
sémination osseuse ?) mais aussi difficulté de préciser
l’objectif précis des études mises en œuvre (prévention
des complications liées aux métastases osseuses ? Activité
anti-tumorale directe ?).
Inhibiteurs de Src kinases
La famille des SFK - Src Family Kinases regroupe
huit protéines kinases dont la protéine cytoplasmique
Src. Les SFK sont impliquées dans la transduction du
signal de nombreuses voies de signalisation et ont
donc de nombreux effets sur les fonctions cellulaires
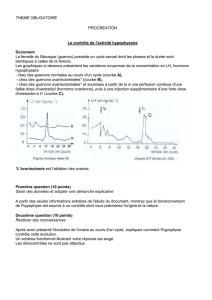
(figure 1). Elles régulent notamment le signal en aval
de différents récepteurs transmembranaires à activité
tyrosines kinases comme l’epidermal growth factor recep-
tor (EGFR), le platelet-derived growth factor receptor
(PDGFR), l’insulin-like growth factor-1 receptor (IGF-1R),
le vascular endothelial growth factor receptor (VEGFR)
mais aussi HER2 ou le récepteur aux œstrogènes. Les SFK
activent alors les voies PI3-kinase, RAS, FAK (focal adhe-
sion kinase)etSTAT3(signal transducers and activators of
transcription 3). Ces voies convergent vers un signal de
promotion de survie cellulaire, de prolifération, de diffé-
renciation, d’angiogenèse et d’invasion.
Une augmentation de l’activité de Src et des autres
protéines SFK a été mise en évidence dans de nombreuses
tumeurs humaines notamment dans les cancers du côlon,
du sein, du pancréas, de la prostate, les mélanomes et
les glioblastomes [2-5]. Les mécanismes de l’activation
Survie Angiogenèse Prolifération Migration cellulaire
SRC
Effecteurs cytoplasmiques
voie PI3K voie STAT 3 voie JNKvoie RAS
αβ
Récepteurs
tyrosine kinase
Canaux
ioniques Intégrines
Ligands
Membrane
cellulaire
Figure 1. Voies SRC (d’après : «Thérapies moléculaires ciblées.
Vignot S. et Soria JC. Montrouge : Éditions John Libbey Eurotext,
2008 et «Diaporama thérapies moléculaires ciblées. »Vignot S. et
Soria JC. Montrouge : Éditions John Libbey Eurotext, 2009).
de Src restent imprécis. Une part peut être attribuée à
des altérations du contrôle de l’activité de la protéine
par augmentation de l’expression de protéines activatrices
ou du signal transmis par des récepteurs membranaires
activés de fac¸on pathologique mais une augmentation de
l’expression du gène a également été rapportée.
L’implication de Src dans la progression métastatique
osseuse a initialement été expertisée dans les cancers
du sein où il a été montré que Src active les ostéo-
clastes et inhibe les ostéoblastes via de complexes voies
de signalisation. Les ostéoclastes expriment de hauts
niveaux de protéines Src, essentielles dans leur migration
et des études précliniques ont montré que les inhibiteurs
de Src diminuent la résorption osseuse par les ostéo-
clastes. Src est donc une cible prometteuse pour casser le
cercle vicieux du microenvironnement osseux favorisant
les métastases et les inhibiteurs de Src pourraient dimi-
nuer les phénomènes d’ostéolyse liés à la tumeur ainsi
que la croissance tumorale. Ce sont ces arguments biolo-
giques qui conduisent à considérer les inhibiteurs de Src
comme des thérapies moléculaires ciblées agissant plus
spécifiquement sur l’os.
Actuellement, trois inhibiteurs de Src sont en cours
d’études cliniques dans cette optique : le dasatinib, le
bosutinib et le saracatinib (tableau 1).
Le dasatinib est une petite molécule disponible par
voie orale qui s’est avérée être un puissant inhibiteur de Src
mais aussi d’autres kinases telles que Abl, KIT et PDGFR.
Son développement a été initialement axé sur le ciblage
de la protéine de fusion Bcr-Abl impliquée dans les leucé-
mies myéloïdes chroniques (LMC) et certaines leucémies
aiguës lymphoblastiques (LAL Ph+). Les essais cliniques
ont confirmé l’intérêt de cette molécule et le dasatinib a été
approuvé par la Food and Drug Administration pour le trai-
tement des LMC après échec ou intolérance de l’imatinib.
Dans le cadre des tumeurs solides, une étude de phase
II chez 44 patients présentant un cancer du sein triple
négatif localement avancé ou métastatique a été réalisée
afin d’évaluer l’efficacité et la tolérance du dasatinib. Les
résultats montrent un taux de réponse globale à 4,7 %
incluant deux patientes avec une réponse partielle et une
médiane de survie sans progression de 8,3 semaines. Une
autre étude a été réalisé chez 70 patientes atteints de can-
cers du sein RE+ (n= 46) et/ou HER2+ (n= 24). Un taux de
réponse de4%aétéretrouvé sur l’ensemble des patientes
évaluables. Ces résultats sont peu impressionnants mais
d’autres études sont en cours pour essayer de sélection-
ner une sous-population de patients qui pourraient tirer
un bénéfice de cette thérapie. L’association du dasatinib
à d’autres molécules notamment aux agents cytotoxiques
ou à l’hormonothérapie paraît également intéressante à
étudier. Une première étude de phase I a ainsi évalué la
tolérance et la dose maximale tolérée (DMT) du dasatinib
associé à la capécitabine dans les cancers de seins locale-
ment avancés [6]. Les principaux événements indésirables
mt, vol. 20, n◦2, avril-mai-juin 2014 119
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Journal Identification = MET Article Identification = 0447 Date: June 25, 2014 Time: 9:0 am
Synthèse
Tableau 1. Stade de développement des agents présentés dans l’article.
Nom Cibles Contexte Phases
Dasatinib Src
Abl
Cancer du sein
- en monothérapie
- en association avec hormonothérapie
- en association avec cytotoxiques
- en association avec acide zolédronique
II
Cancer de la prostate
- en monothérapie
- en association avec docétaxel
II
Mélanome, glioblastome, cancer de l’ovaire I/II
Bosutinib Src
Abl
Cancer du sein
- en monothérapie
- en association avec hormonothérapie
- en association avec cytotoxiques
Saracatinib Src
Abl
Cancer du sein
Cancer de la prostate
Balicatib Cathepsine K actuellement, développement dans le traitement de l’ostéoporose
Odanacatib Cathepsine K Actuellement, développement dans le traitement de l’ostéoporose
Cancer du sein métastatique osseux II
Plerixafor CXCR4 Mobilisation de cellules souches Autorisé
CtCe-9908 Analogue du SDF1 Cancer métastatique I
de tous grades retrouvés ont été les nausées (58 %), le syn-
drome pieds-main (44 %), la diarrhée (33 %), l’asthénie
(33 %), les vomissements (31 %) tandis que les effets
indésirables de grade 3-4 concernaient des syndromes
pieds-mains (12 %), la diarrhée (8 %), l’asthénie (8 %), les
épanchements pleuraux (8 %) et les vomissements (6 %).
La dose maximale tolérée a été définie avec la capécita-
bine à 1 000 mg/m2deux fois par jour et le dasatinib à
100 mg/jour. Sur les 25 patients traités à cette dose dont la
réponse était évaluable, ilyaeu24%deréponse partielle
et 32 % de stabilisation de la maladie. Une autre étude
de phase I a montré que la DMT du dasatinib associé au
paclitaxel à la dose de 80 mg/m2trois semaines sur quatre
chez des patientes métastatiques était de 120 mg/jour [7].
Un intérêt particulier est également porté à la combinai-
son des inhibiteurs de Src avec l’hormonothérapie. Des
essais sont en cours pour tester cette combinaison chez
des patientes hormonorésistantes.
Le dasatinib est également développé dans le cancer
de la prostate. Dans l’idée de cibler à la fois la tumeur
et le microenvironnement osseux, une étude de phase I/II
associant le docétaxel et le dasatinib a été menée chez des
patients avec un cancer de la prostate résistant à la castra-
tion. Dans l’étude de phase I, 16 hommes ont été inclus
et 30 patients supplémentaires ont été inclus en phase II.
L’efficacité était évaluée par la mesure de PSA, par le taux
de réponse selon les critères RECIST et un dosage des mar-
queurs osseux a aussi été réalisé. Une diminution de PSA
de 50 % ou plus pendant plus de six semaines a été retrou-
vée chez 26 des 46 patients (57 %). Sur les 30 patients
ayant une maladie évaluable, 18 (60 %) ont eu une réponse
partielle, 14 (30 %) ont présenté une disparition des lésions
osseuses au scanner. L’évaluation des marqueurs osseux a
montré une diminution des N-télopeptides urinaires chez
33/38 patients (87 %) et des PAL chez 26/34 patients
(76 %). L’association était globalement bien tolérée (28 %
d’effets indésirables de grade 3-4 à type d’asthénie et
d’épanchement pleural). On note que 28 patients (61 %)
ont poursuivi le dasatinib en monothérapie après arrêt du
docétaxel et ont présenté une stabilisation de leur mala-
die pendant un à 12 mois. Ces données d’efficacité et
le bon profil de tolérance sont prometteurs et justifient
la réalisation d’études randomisées dans cette population
de patients. La diminution du PSA et des marqueurs du
métabolisme osseux évoque un ciblage en parallèle des
compartiments épithéliaux et osseux du cancer. Le traite-
ment d’entretien après arrêt du docétaxel paraît également
intéressant à étudier [8].
Dans la même population de patients, une autre
étude de phase II cherchant à déterminer l’efficacité et
la tolérance du dasatinib 100 mg/jour en monothérapie a
également été effectuée. Sur les 48 patients inclus, la sur-
vie sans progression à 12 semaines était de 44 % (n= 21) et
de 17 % (n= 8) à un an. Une réduction de plus de 40 % des
N-télépeptides urinaires chez 51 % des patients (n= 22/43)
et des PAL chez 59 % (n= 26/44) a été retrouvée. Le
dasatinib était bien toléré [9]. Enfin, une autre de phase II
sur 47 patients recevant du dasatinib à 100mg/jour (n= 25)
120 mt, vol. 20, n◦2, avril-mai-juin 2014
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Journal Identification = MET Article Identification = 0447 Date: June 25, 2014 Time: 9:0 am
ou 70 mg/jour (n= 22) retrouve des résultats similaires en
termes de survie sans progression, de diminution des mar-
queurs osseux et de tolérance [10].
La molécule est par ailleurs également en cours
d’évaluation dans d’autres contextes, sans être spécifique-
ment ciblé sur la problématique de la progression osseuse
(cancer colorectal, cancers gynécologiques, mélanome)
avec des résultats préliminaires montrant une activité
modeste en monothérapie [11-14].
Le bosutinib est un inhibiteur sélectif de Src et de Abl
administrable par voie orale en cours de développement
[15]. Dans les études précliniques, une inhibition des voies
de signalisation impliquées dans la prolifération cellulaire,
l’angiogenèse, la mobilité et l’invasion a été montrée sur
les cellules de cancers du sein. Une étude de phase II
récemment réalisée a évalué l’intérêt du bosutinib chez
des patients avec un cancer du sein localement avancé
ou métastatique déjà traité. Soixante treize patientes ont
été inclues [16]. Le taux de survie sans progression à
16 semaines était de 39,6 %. De fac¸on intéressante, toutes
les patientes répondeuses (n= 4) avaient des récepteurs
hormonaux positifs. La survie globale à deux ans était de
26,4 %. Les principaux effets secondaires retrouvés ont été
les diarrhées, les nausées et les vomissements. Aux vues
des résultats de cette étude, une autre étude de phase II
randomisée s’est intéressée à l’association du bosutinib au
létrozole versus létrozole seul chez des patientes méno-
pausées en première ou deuxième ligne de traitement
ayant un cancer du sein localement avancé ou métasta-
tique RH+. La première partie de l’étude était une étude de
tolérance avant de réaliser la partie deux pour l’évaluation
de l’efficacité. Seize patientes ont été inclues dans la
partie 1 en utilisant bosutinib à 400 mg/jour et létrozole
à 2,5 mg/jour. Les principaux effets indésirables de tout
grade ont été la diarrhée, les vomissements, les nausées,
les rashs, l’asthénie et la dyspnée. Les effets indésirables
de grade 3-4 incluaient des augmentations des enzymes
hépatiques à type de cytolyse et concernaient plus de 15 %
des patientes. Ces patientes ont dû interrompre le traite-
ment et l’étude a été arrêtée devant un ratio défavorable
de la balance bénéfice-risque. Aucune étude d’efficacité
n’a donc pu être réalisée [17].
Une étude de phase II randomisée a évalué la survie
sans progression de 42 patientes ménopausées avec un
cancer du sein RH+ et HER2- traitées soit par du bosu-
tinib et de l’exémestane soit par de l’exémestane seule
en seconde ligne après un premier échec de traitement
par anti-aromatase. La médiane de survie sans progres-
sion était de 12,3 semaines et le taux de réponse global
de 3,6 %, avec une tolérance jugée acceptable dans cette
étude [18].
Enfin, le saracatinib, un autre inhibiteur de non sélectif
de Src et de Abl [19], a montré dans les études pré-
cliniques une action inhibitrice de la résorption osseuse
par les ostéoclastes. Le saracatinib préviendrait en outre
l’apparition de résistance aux hormonothérapies in vitro et
a montré un effet anti-tumoral in vivo. Une étude de phase
II réalisée sur neuf patientes atteintes d’un cancer du sein
métastatique RH- a été réalisée [20]. Aucune patiente n’a
eu de réponse complète, partielle ou de stabilisation de la
maladie pendant plus de six mois. Le temps de traitement
médian avant la rechute était de 82 jours (12-109 jours).
Les effets indésirables les plus fréquents ont été l’asthénie,
une perturbation du bilan hépatique, des nausées, une dys-
pnée et une insuffisance surrénalienne. À noter qu’une
patiente a dû être sortie de l’étude du fait d’une pneumo-
pathie interstitielle hypoxémiante potentiellement liée au
traitement.
Une autre étude de phase II visant à comparer les effets
du saracatinib et de l’acide zolédronique chez des patients
atteints de cancers du sein ou de la prostate métastatique
osseuse est en cours.
Inhibiteurs de la cathepsine K
La cathepsine K est une protéase à cystéine lysoso-
male principalement produite par les ostéoclastes. Les
ostéoclastes participent à la formation d’un microenvi-
ronnement acide à la surface des os optimal pour la
dégradation du collagène de type I par la cathepsine K.
Le rôle de la cathepsine K dans la résorption osseuse
est démontré par les études précliniques. Les souris défi-
cientes en cathepsine K développent de l’ostéopétrose (ou
maladie des os de marbre) et la fonction de dégradation
de la matrice osseuse par leurs ostéoclastes est altérée.
Dans une étude préclinique utilisant des modèles murins
de cancers du sein métastatiques osseux, il a été montré
que la cathepsine K n’était pas seulement exprimée par
les ostéoclastes mais aussi par les cellules cancéreuses
métastatiques aux os. L’utilisation d’un inhibiteur de la
cathepsine K réduit alors de fac¸on significative (p= 0,016)
l’ostéolyse induite par la tumeur et la masse tumorale
osseuse (p= 0,007). Cette altération (blocage ou diminu-
tion d’activité) de la fonction des ostéoclastes a conduit à
une diminution de la production de facteurs de croissance
tumoraux impliqués dans le cercle vicieux du microenvi-
ronnement osseux [21].
Le développement d’un inhibiteur de la cathepsine K
a ainsi permis une nouvelle approche dans le traitement
de l’ostéoporose. Deux médicaments sont actuellement
en cours d’essais cliniques pour cette indication : le bali-
catib et l’odanacatib. Une étude de phase II utilisant le
balicatib réalisée chez des femmes ménopausées atteintes
d’ostéoporose a montré une réduction dose-dépendante
des taux des marqueurs de résorption osseuse et une aug-
mentation de la densité osseuse [22]. Le balicatinib a
une action lysosomotrope et peut s’accumuler dans les
lysosomes avec une concentration suffisante pour causer
mt, vol. 20, n◦2, avril-mai-juin 2014 121
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Journal Identification = MET Article Identification = 0447 Date: June 25, 2014 Time: 9:0 am
Synthèse
une inhibition d’autres types de cathepsines, dont cer-
taines sont exprimées par les fibroblastes cutanés. Étant
donné ces effets potentiels, un développement futur du
balicatinib est en attente.
L’odanacatib, un inhibiteur sélectif de la cathepsine
K, est l’agent le plus prometteur de cette classe thérapeu-
tique. Une étude de phase II de l’odanacatib réalisée chez
des femmes ménopausées atteintes d’ostéoporose a mon-
tré une diminution des taux des marqueurs de résorption
osseuse et une augmentation de la densité osseuse, avec
une bonne tolérance clinique [23]. Des études de phase III
sont actuellement en cours. Une seule est actuellement ter-
minée et a étudié les modifications de la densité minérale
osseuse (DMO) et des taux des marqueurs osseux chez
258 patientes ménopausées atteintes d’ostéoporose trai-
tées soit par odanacatib (à plusieurs doses) soit par placebo
soit par alendronate 70 mg / semaine. Une augmentation
significative de la DMO a été retrouvée avec l’alendronate
ainsi qu’avec l’odanacatib, sans différence entre les deux
[24].
À l’heure actuelle, peu d’études sur les inhibiteurs de
la cathepsine K chez des patients atteints de cancers sont
en cours. Seule une étude de phase II cherchant à évaluer
l’efficacité de l’odanacatib comparé à l’acide zolédro-
nique dans la diminution de la résorption osseuse et chez
des patientes atteintes de cancer du sein est terminée. Les
résultats montrent une réduction des taux de marqueurs
de résorption osseuse après quatre semaines de traitement
sans différence entre les deux traitements [25]. D’autres
études en oncologie sont en cours.
Cibler les récepteurs aux chimiokines
CXCR4 est un récepteur membranaire couplé aux pro-
téines G de la famille des récepteurs aux chimiokines. Le
ligand du récepteur CXCR4 est le Stromal cell-derived fac-
tor 1 (SDF1 ou CXCI12). Ce récepteur est surexprimé dans
de nombreux cancers et notamment dans le tissu mam-
maire tumoral alors qu’il est peu exprimé dans le tissu
mammaire normal [26].
On a également pu remarquer que CXCR4 était plus
fortement exprimé dans les métastases osseuses que vis-
cérales de cancer du sein [27]. CXCR4 a un rôle important
dans l’attachement des cellules souches à la matrice
de la moelle osseuse qui est une zone riche en SDF-1
[28]. De plus, il a été montré qu’une forte expression de
CXCR4 dans les cellules tumorales de cancer du sein était
associé à un risque significativement plus élevé de méta-
stases osseuses [29], de rechute [30] et à un moins bon
pronostique [31].
L’axe CRCR4/SDF-1 paraît donc être une cible
thérapeutique intéressante. Cependant, des études
supplémentaires doivent être réalisées afin de mieux
connaître les effets parallèles de l’inhibition de cet
axe. En effet, cet axe est également impliqué dans la
modulation du système immunitaire et dans une étude
préclinique étudiant les effets de l’inhibition de SDF1 et
de CXCR4 dans les métastases osseuses de cancers du
sein et de la prostate, il a été montré un risque théorique
d’altération du système immunitaire et de mobilisation
des cellules tumorales pouvant peut-être favoriser la
formation de métastases sur d’autres sites à distance [32].
Parmi les molécules en cours de développement pré-
coce ciblant cet axe, mentionnons le CtCe-9908 qui est un
analogue du SDF-1 qui a une action compétitive antago-
niste sur CXCR4. Dans un modèle murin, l’utilisation du
CtCe-9908 ne réduisait pas la fréquence des métastases
mais diminuait à la fois le volume tumoral des métastases
[33] et celui de la tumeur primitive [34]. Une étude de
phase I/II étudiant le CtCe-9908 chez des patients présen-
tant un cancer solide réfractaire (cancer du sein : n=8)a
montré une réponse clinique modeste (17 patients ont pro-
gressé, 5 étaient stables) avec une bonne tolérance [35].
D’autres essais cliniques sont en cours, notamment dans
les cancers ORL, les myélomes multiples et les leucémies.
Le plerixafor est une autre molécule en développe-
ment. Il s’agit d’un antagoniste du récepteur CXCR4 qui
permet la mobilisation des cellules souches hématopoïé-
tiques de la moelle osseuse à la circulation sanguine. Il est
actuellement couramment utilisé en hématologie pour les
autogreffes de moelle [36]. De nombreux essais cliniques
sont en cours en hématologie, mais le plerixafor appa-
raît également intéressant en association avec d’autres
molécules comme les bisphosphonates et notamment à
l’acide zolédronique qui est aussi connu pour avoir une
action inhibitrice sur le CXCR4 présent dans les cellules de
cancer du sein [37]. Ces molécules pourraient également
présenter un intérêt dans le traitement des infections par
le VIH, les récepteurs aux chimiokines pouvant participer
à l’internalisation du virus.
Autres pistes et perspectives
La meilleure compréhension des mécanismes du
remodelage osseux et de la progression métastatique a
également conduit à envisager d’autres cibles potentielles
telles que la PTHrP ou le TGF. Si le rationnel de leur
ciblage est cohérent, les résultats cliniques restent préli-
minaires.
Cibler la PTHrP ?
La PTHrP est un facteur favorisant physiologique-
ment l’ostéogenèse en stimulant l’activité ostéoblastique
[38, 39]. L’intérêt de son ciblage est basé sur des études
précliniques conduites sur modèles murins qui ont pu
montrer une diminution de la taille de lésions ostéoly-
tiques avec un anticorps neutralisant anti-PTHrP [38]. Un
122 mt, vol. 20, n◦2, avril-mai-juin 2014
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
1
/
7
100%