Œil et rhumatisme : le point de vue de l`ophtalmologue

MISE AU POINT
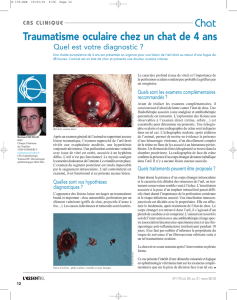
Figure 1. Syndrome sec oculaire. A. Test de Schirmer. B. Kératite fi lamenteuse.
A B
14 | La Lettre du Rhumatologue • No 393 - juin 2013
Œil et rhumatisme : le point
de vue de l’ophtalmologue
Eye and rhumatism, the ophthalmologist’s point of view
A. Sauer*
* Service d’ophtalmologie, CHRU
de Strasbourg.
L
es interactions entre le rhumatologue et
l’ophtalmo logue sont multiples. En effet, de
nombreuses maladies rhumatismales peuvent
être à l’origine d’atteintes touchant tous les seg-
ments de l’œil. Ainsi, les antécédents rhumato-
logiques doivent être recherchés, quel que soit le
motif de consultation en ophtalmologie (1, 2). Les
mécanismes physiopathologiques sont :
➤immunitaires ou infl ammatoires ;
➤consécutifs à une toxicité médicamenteuse ;
➤mécaniques.
Les kératoconjonctivites
La conjonctivite et la kératite sont défi nies comme
une atteinte infl ammatoire respectivement de la
conjonctive ou de la cornée, quelle qu’en soit la
cause. La conjonctivite se manifeste habituellement
par un œil rouge et une sensation de corps étranger
sans douleur. Lors d’une kératite, la douleur est tou-
jours présente, mais d’intensité variable, accom-
pagnée d’une photophobie et d’un larmoiement.
À l’examen à la lampe à fente, un défect épithélial
cornéen est mis en évidence à l’aide de fl uorescéine
en cas de kératite.
Le syndrome sec oculaire et le syndrome
de Gougerot-Sjögren
Le rhumatologue est confronté aux conjonctivites et
aux kératites en cas de patients présentant un syn-
drome sec oculaire (xérophtalmie) [3]. Une attention
toute particulière doit être portée à la recherche
d’un syndrome de Gougerot-Sjögren (SGS) en
cas de sécheresse oculaire. Le patient se plaint en
général d’une brûlure oculaire ou d’une sensation
de grains de sable ou de graviers. La photophobie
sera observée en cas de kératite.
Le “tear break-up time” (BUT) [temps de rupture
du fi lm lacrymal] est observé à la lampe à fente en
fi ltre bleu après l’instillation d’une goutte de fl uo-
rescéine. L’examinateur mesure le temps nécessaire
à la rupture du fi lm lacrymal (normalement supé-
rieur à 10 secondes). Le test de Schirmer permet
d’objectiver le syndrome sec. Il existe 2 techniques
possibles. La première se fait sans anesthésie locale
et permet de mesurer les sécrétions lacrymales
basale et réfl exe. Le buvard, placé à la jonction
entre le tiers externe et la moitié de la paupière
inférieure (figure 1A), est mouillé jusqu’à la troi-
sième division (soit 15 mm) au bout de 5 minutes
chez un patient normal. En cas d’application d’un
anesthésiant topique (méthode la plus classique),
seule la sécrétion basale est quantifi ée. Une humi-
difi cation insuffi sante est défi nie par une hauteur
inférieure à 5 mm en 5 minutes. La présence d’une

Points forts
La Lettre du Rhumatologue • No 393 - juin 2013 | 15
»
Le syndrome sec oculaire sévère nécessite une prise en charge ophtalmologique dans un centre spécialisé.
»Le diagnostic de sclérite doit rapidement être évoqué par le rhumatologue dans le cadre du suivi d’un
patient atteint d’une maladie rhumatismale présentant un œil rouge ou douloureux.
»
La polyarthrite rhumatoïde, la maladie de Wegener, la polychondrite atrophiante, la panartérite noueuse
et le lupus érythémateux disséminé peuvent être responsables d’une perforation cornéenne pauci sympto-
matique.
Mots-clés
Kératite
Syndrome sec oculaire
Sclérite
Uvéite
Hydroxychloroquine
Highlights
»
Severe dry eye disease
requires ophthalmologic care
in a specialized center.
»
Rheumatologists have to con-
sider the diagnosis of scleritis
in the follow-up of a patient
with rheumatic disease pre-
senting with a red or painful
eye.
»
Rheumatoid arthritis,
Wegener’s granulomatosis,
relapsing polychondritis, poly-
arteritis nodosa and lupus ery-
thematosus may be responsible
for pauci-symptomatic corneal
perforation.
Keywords
Keratitis
Dry eye disease
Scleritis
Uveitis
Hydroxychloroquine
kératite ponctuée superficielle ou filamenteuse
(figure 1B) ou d’un ulcère cornéen, voire d’une
perforation cornéenne, traduit de manière graduelle
la complication du syndrome sec oculaire. Un bilan
étiologique de SGS est conduit conjointement avec
le rhumatologue au moindre doute (3, 4).
Le traitement du syndrome sec oculaire (y compris
dans le SGS) vise à stabiliser la maladie systémique,
à augmenter ou maintenir la sécrétion lacrymale et
à diminuer l’inflammation de surface (4). Il repose
en premier lieu sur les substituts lacrymaux, en
respectant si possible une marche croissante allant
des larmes artificielles aux gels de carbomère puis
aux acides hyaluroniques. Des produits sans conser-
vateurs, non toxiques pour la surface oculaire,
déjà altérée, sont prescrits en première intention
en traitement chronique (5). Si ces mesures sont
insuffisantes, la mise en place de bouchons méa-
tiques (clous acryliques) peut s’avérer utile. Au
stade suivant, la ciclosporine en collyre pourra être
introduite, soit à une concentration de 0,05 %, soit,
plus classiquement, à 0,5 % (dispensation hospita-
lière). Les sécréta gogues comme la pilocarpine sont
parfois efficaces, mais peuvent causer des difficultés
à la lecture. En cas de persistance du syndrome
sec, des collyres à base de sérum autologue, une
thérapie matricielle, des lentilles SPOT® (verres
Scléraux Perméables à l’Oxygène de Thonon) ou,
dans les cas extrêmes, une tarsorraphie peuvent
être indiqués dans des centres ophtalmologiques
spécialisés (4, 5). Parallèlement à ces traitements,
les patients présentant un syndrome sec oculaire
doivent bénéficier d’une série de conseils permet-
tant d’améliorer la symptomatologie au quotidien
(tableau I).
Ulcération cornéenne périphérique
Dans le cadre des kératites, le rhumatologue peut
aussi avoir à faire face aux ulcérations cornéennes
périphériques (Peripheral Ulcerative Keratitis [PUK])
ou ulcère de pseudo-Mooren. Parfois indolentes,
elles se manifestent toujours par un œil rouge (6).
À la lampe à fente, l’ophtalmologiste observe un
amincissement périphérique, parfois circonférentiel,
de la cornée, qui peut mener à une perforation cor-
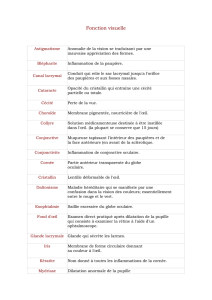
néenne (figure 2, p. 16). Les ulcérations cornéennes
périphériques sont l’apanage des connectivites, dont
la polyarthrite rhumatoïde, la maladie de Wegener,
la polychondrite atrophiante, la panartérite noueuse
ou le lupus érythémateux disséminé. La présence
d’un œil rouge chez un patient présentant une de ces
maladies doit faire pratiquer un examen ophtalmo-
logique en urgence afin de permettre une prise en
charge avant la perforation cornéenne (6, 7).
Le traitement repose sur une excellente coordination
entre le rhumatologue et l’ophtalmologue. Le traite-
ment de la maladie systémique doit être commencé
en urgence et comprend toujours au minimum une
corticothérapie systémique. Au niveau oculaire
seront associés des antibiotiques topiques, des col-
lyres cycloplégiques à visée antalgique, de la doxy-
cycline (100 mg/ j) pour ses propriétés d’inhibition
des métallo protéinases, et des larmes artificielles
dispensées de manière extrêmement rapprochée.
En cas de perforation cornéenne, la prise en charge
chirurgicale dépendra de la taille de la perforation ;
en cas de perforation de petite taille, un patch de
colle cyanoacrylate et une lentille de contact seront
mis en place ; en cas de large perforation, une greffe
de cornée sera indiquée (6, 7).
Tableau I. Conseils pratiques à donner aux patients souffrant de xérophtalmie.
À faire À éviter
Boire abondamment, consommer de la caféine Médicaments généraux à éviter : contraceptifs oraux, antihistaminiques,
bêtabloquants, phénothiazines, atropine, antalgiques opiacés
Bien dormir Tabagisme actif ou passif
Limiter la luminosité (lunettes de soleil, stores,etc.) Pollution extérieure (allergènes, poussières, particules fines,etc.)
Avoir une bonne hygiène des mains et du visage Pollution intérieure (air conditionné, cheminée, sèche-cheveux,etc.)
Renforcer la lubrification des yeux
et penser à cligner lors du travail sur écran
Temps venteux, chaud et sec
Fermer les yeux quelques instants dans la journée Lentilles de contact (à discuter…) et chirurgie réfractive

Œil et rhumatisme : le point de vue de l’ophtalmologue
MISE AU POINT
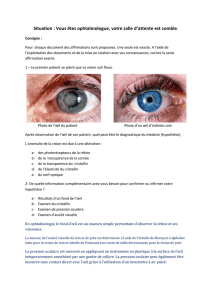
Figure 3. Sclérite. A. Sclérite nodulaire. B. Sclérite nécrosante.
B
A
Figure 2. Ulcération périphérique cornéenne compliquée d’une perforation avec incar-
cération irienne.
16 | La Lettre du Rhumatologue • No 393 - juin 2013
Les sclérites et les épisclérites
La sclère est la tunique blanche externe de l’œil sur
laquelle s’insèrent les muscles oculomoteurs. La
sclère peut être divisée en 3 couches : l’épisclère
est la plus superfi cielle, le stroma scléral, l’inter-
médiaire, et la lamina fusca, la plus profonde, en
contact avec l’uvée. La localisation de l’inflam-
mation et les modifi cations de la vascularisation
sclérale associées permettent de distinguer les épi-
sclérites des sclérites. Les épisclérites correspondent
à des infl ammations superfi cielles aiguës bénignes
caractérisées par une gêne oculaire dont l’origine
est le plus souvent une pathologie de la surface
oculaire. Les sclérites sont au contraire des infl am-
mations plus profondes, chroniques, douloureuses
et potentiellement cécitantes. Elles sont souvent
associées à des pathologies systémiques parfois
mortelles (7, 8).
La classifi cation actuelle des sclérites sépare de
manière anatomique les sclérites antérieures des
sclérites postérieures, selon que l’inflammation
sclérale survient en avant ou en arrière de l’ora
serrata. Les sclérites antérieures sont elles-mêmes
divisées selon leur aspect clinique, présentant des
degrés de sévérité croissante (tant sur le plan local
que général par leur association à des vascularites
systémiques), en sclérites antérieures diffuses, nodu-
laires (fi gure 3A) et nécrosantes (fi gure 3B) avec
infl ammation ou sans infl ammation (8).
La matrice sclérale est riche en collagènes, élastine
et protéoglycanes, et comporte de nombreuses
similitudes avec les constituants articulaires. L’œil
mobile au sein de l’orbite ressemble ainsi à une arti-
culation dont les muscles oculomoteurs, les plexus
épiscléraux et la capsule de Tenon rappellent les
structures synoviales et les capsules articulaires. Il
n’est donc pas étonnant de noter de nombreuses
pathologies rhumatismales parmi les étiologies
d’infl ammations sclérales (8).
Typiquement, 2 types de patients sont amenés
à consulter pour une sclérite. En milieu hospita-
lier, le patient est le plus souvent suivi pour une
pathologie systémique, la sclérite en est un épisode
inter current, qui se manifeste par un œil rouge
plus ou moins douloureux. Dans ce cas, le rôle de
l’ophtalmo logiste est d’éclairer le rhumatologue en
rappelant l’association de ce type de complication
ophtalmologique à une évolutivité de l’affection
causale et en pointant les signes de gravité pouvant
nécessiter une prise en charge urgente. Le traitement
de fond de la pathologie causale devra alors être
modifi é (7-9).

MISE AU POINT
La Lettre du Rhumatologue • No 393 - juin 2013 | 17
Le second type de patients, sans antécédents
médicaux, consulte généralement aux urgences
ophtalmologiques en raison de douleurs insom-
niantes et d’un œil sectoriellement rouge. Ces
patients doivent bénéficier, dès la première poussée
de sclérite, d’un bilan biologique (tableau II), ciblé
selon les éléments de l’interrogatoire et de l’examen
clinique, en premier lieu à la recherche des connec-
tivites et des vascularites (polyarthrite rhumatoïde,
maladie de Wegener, polychondrite atrophiante,
lupus érythémateux disséminé, panartérite noueuse
et spondyloarthrites), puis de certaines maladies
infectieuses (7-9).
Les sclérites ne répondent généralement pas aux
traitements anti-inflammatoires locaux stéroï-
diens ou non stéroïdiens. Cependant, les corti-
coïdes locaux pourraient diminuer les doses totales
cumulées de corticoïdes systémiques, voire prévenir
parfois leur utilisation lorsque la pathologie causale
est purement locale. Les anti-inflammatoires non
stéroïdiens (AINS) oraux représentent le traitement
de première ligne des sclérites non nécrosantes.
Certains patients y répondent extrêmement bien.
Les sclérites entrant dans le cadre d’une maladie
systémique ne sont pas de bonnes indications des
AINS oraux en monothérapie ; une corticothérapie
par voie orale et/ou une immunosuppression sont
toujours indiquées (8, 9).
Les uvéites
Le rhumatologue peut aussi être confronté aux
uvéites. Ces dernières sont habituellement classées
selon leur localisation : antérieure, intermédiaire,
postérieure ou touchant les 3 segments de l’œil
(panuvéite). Dans le cadre des uvéites antérieures,
le rhumatologue est en général face à 2 situations,
une uvéite consécutive à une maladie rhumatismale
ou une uvéite infectieuse compliquant une immu-
nosuppression systémique (1, 2).
Il pourra ainsi s’agir d’une uvéite en rapport avec une
maladie rhumatismale diagnostiquée au décours
de l’épisode ou antérieurement connue. Les uvéites
à HLA-B27 en sont un exemple classique et repré-
sentent la première cause d’uvéite antérieure de
l’adulte jeune en France. Leur traitement repose sur
une corticothérapie locale, voire systémique, selon
la gravité de l’atteinte (10). Les uvéites des arthrites
juvéniles infantiles (AJI) font partie du même groupe
nosologique et sont la cause principale d’uvéite de
l’enfant derrière les maladies infectieuses. Ces uvéites
se rencontrent préférentiellement dans les formes
oligo articulaires d’AJI, chez la petite fille ayant des
anticorps antinucléaires positifs. Le traitement des
uvéites dans l’AJI est local et repose sur la cortico-
thérapie. Le méthotrexate ou les anti-TNF (tels que
l’infliximab ou l’adalimumab) sont utiles dans la
prévention des rechutes et permettent une épargne
cortisonique (11). En dehors de ces 2 causes clas-
siques d’uvéite, l’interrogatoire et l’examen clinique
des patients présentant une uvéite et une arthrite
permettront d’orienter le patient vers le rhumato-
logue afin de rechercher, notamment, une maladie
de Behçet (uvéite à hypopion et/ ou vascularite réti-
nienne), une maladie de Lyme, une polychondrite
atrophiante ou un rhumatisme psoriasique (1, 2).
Par ailleurs, une uvéite peut survenir chez un patient
sous immunosuppresseurs. Devant une baisse
d’acuité visuelle associée ou non à un œil rouge
et douloureux, le diagnostic sera une panuvéite,
qui peut notamment inclure une rétinite ou une
rétino choroïdite, dont l’évolution vers la nécrose
rétinienne peut être fulgurante. Dans ce cas, la
recherche d’une cause infectieuse devient la priorité
de l’ophtalmologue. Une ponction de la chambre
antérieure avec recherche des virus de la famille
des herpès par PCR (virus de l’herpès simplex, virus
d’Epstein-Barr, cyto mégalo virus et virus varicelle-
zona) et de Toxoplasma gondii doit être pratiquée en
urgence. Un traitement par voie veineuse (ciblant les
virus herpétiques) ou par voie orale (en cas de toxo-
plasmose oculaire) est instauré au moindre doute.
La survenue d’une infection est ainsi une complica-
tion redoutée des immunosuppresseurs (1, 2, 11). La
toxicité maculaire de l’hydroxychloroquine fait aussi
partie des effets indésirables médicamenteux liant
l’activité des ophtalmologues et celle des rhumato-
logues.
Tableau II. Bilan étiologique devant une sclérite ou une épisclérite récidivante.
Bilan à réaliser face à un premier épisode de sclérite
ou en cas d’épisclérite récidivante
Bilan biologique NFS, VS, CRP, fibrinogène
Électrophorèse des protéines plasmatiques
Bilan rénal et hépatique
Facteur rhumatoïde, anticorps anticitrulline
Anticorps anti-Ro-SSA ; la-SSB, biopsie des glandes salivaires accessoires
Anticorps antinucléaires ± anti-ADN natifs
ANCA
TPHA-VDRL, sérologies VIH, VHB, VHC, intradermoréaction à la tuberculine
Imagerie Radiographie du thorax
Radiographie des articulations douloureuses

www.edimark.fr
le courrier du spécialiste
Société éditrice : EDIMARK SAS
CPPAP : 0413T81251 – ISSN : 0761-5027
PÉRIODIQUE DE FORMATION
EN LANGUE FRANÇAISE
Mensuel
Prix du numéro : 21 €
N
o
393 ~ juin 2013
Toute l’actualité
de votre spécialité sur
www.edimark.tv
ÉDITORIAL
L’IL-23 : chef d’orchestre
de la physiopathologie
des spondyloarthrites ?
par D. Wendling
MISES AU POINT
Œil et rhumatisme :
le point de vue de l’ophtalmologue
Prothèses digitales :
quoi de neuf en 2013 ?
ABONNEZVOUS ET BÉNÉFICIEZ DE NOMBREUX SERVICES ■ Oui, je m’abonne
À TRÈS VITE ! ... POUR UNE INFORMATION INDISPENSABLE À LA PRATIQUE DE VOTRE PROFESSION
Œil et rhumatisme : le point de vue de l’ophtalmologue
MISE AU POINT
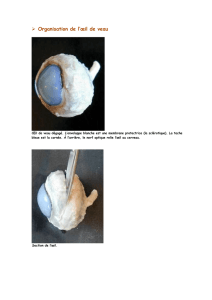
Figure 4. Maculopathie due aux antipaludéens de synthèse.
18 | La Lettre du Rhumatologue • No 393 - juin 2013
La surveillance des toxicités
médicamenteuses
La rétinopathie due aux antipaludéens de synthèse
(APS), hydroxychloroquine et chloroquine prin-
cipalement, est très rare mais peut être sévère.
Les patients traités peuvent d’abord développer
une “intoxication rétinienne préclinique aux APS”.
Celle-ci est réversible : il existe une altération des
paramètres de surveillance sans atteinte clinique
visible. L’examen du champ visuel central montre
une diminution de la sensibilité parafovéale.
L’électro rétino gramme (ERG) multifocal retrouve
une dépression des réponses paracentrales. L’Optical
Coherence Tomography-Spectral Domain (OCT-SD)
objective un amincissement rétinien parafovéal. Si
le traitement est poursuivi, l’atteinte évolue vers
l’“intoxication rétinienne aux APS”. À ce stade,
les anomalies décrites ci-dessus sont accentuées,
et l’atteinte de la rétine est visible au fond d’œil
(fi gure 4). La baisse visuelle est alors sévère et irré-
versible, et l’examen du champ visuel objective un
scotome paracentral profond (12).
Le dépistage des intoxications rétiniennes aux
APS au stade préclinique est donc indispensable
et a d’ailleurs fait l’objet de recommandations
récentes (13). La première évaluation est réalisée
dans l’année qui suit le début du traitement. Elle
comprend l’information du patient, un examen
ophtalmologique complet avec fond d’œil dilaté,
un examen du champ visuel central automatisé
et un ou plusieurs examens objectifs, selon leur
disponibilité (ERG multifocal, OCT-SD, clichés en
autofl uorescence du fond d’œil). Pendant le traite-
ment, une surveillance comparative est effectuée
à un rythme annuel. L’ophtalmologiste peut rap-
procher les examens en fonction de l’existence ou
non de facteurs de risque. Les facteurs de risque
pour l’hydroxychloroquine sont une dose ingérée
cumulée supérieure à 1 000 g, une durée de trai-
tement supérieure à 5 ans, une dose supérieure à
6,5 mg/kg/j, une insuffi sance rénale ou hépatique,
un âge supérieur à 65 ans et la préexistence d’une
anomalie maculaire (12, 13).
Conclusion
Les atteintes oculaires des maladies rhumatismales
sont multiples et variées. Une bonne coordination
entre l’ophtalmologiste et le rhumatologue est
nécessaire afi n d’optimiser la prise en charge des
patients atteints d’une maladie rhumatismale. ■
Références bibliographiques
1. Mohsenin A, Huang JJ. Ocular manifestations of systemic
infl ammatory diseases. Conn Med 2012;76:533-44.
2. Petris CK, Almony A. Ophthalmic manifestations of
rheumatologic disease: diagnosis and management.
Mo Med 2012;109:53-8.
3. Varoquier C, Sibilia J, Gottenberg JE. Des critères précis
et rigoureux : critères diagnostiques du syndrome de
Gougerot-Sjögren. Rev Prat 2012;62:225-8.
4. Robert PY. Traitement de la xérophtalmie dans le
syndrome de Gougerot-Sjögren. Rev Prat 2012;62:236-7.
5. Tong L, Petznick A, Lee S, Tan J. Choice of artifi cial tear
formulation for patients with dry eye: where do we start?
Cornea 2012; 31(Suppl. 1):S32-6.
6. Ladas JG, Mondino BJ. Systemic disorders associated
with peripheral corneal ulceration. Curr Opin Ophthalmol
2000;11:468-71.
7. Galor A, Thorne JE. Scleritis and peripheral ulce-
rative keratitis. Rheum Dis Clin North Am 2007;
33:835-54.
8. Gabison E, Hoang-Xuan T. Sclérites : quand évoquer
une pathologie systémique ? J Fr Ophtalmol 2010;
33:593-8.
9. Rachitskaya A, Mandelcorn ED, Albini TA. An update on
the cause and treatment of scleritis. Curr Opin Ophthalmol
2010;21:463-7.
10. Wakefield D, Chang JH, Amjadi S, Maconochie Z,
Abu El-Asrar A, McCluskey P. What is new HLA-B27 acute
anterior uveitis? Ocul Immunol Infl amm 2011;19:139-44.
11. Rabinovich CE. Treatment of juvenile idiopathic arth-
ritis-associated uveitis: challenges and update. Curr Opin
Rheumatol 2011;23:432-6.
12. Rousseau A, Labetoulle M. Atteintes ophtalmologiques
d’origine médicamenteuse. EMC Ophtalmologie 2012;9:1-9.
13. Marmor MF, Kellner U, Lai TY, Lyons JS, Mieler WF;
American Academy of Ophthalmology. Revised recom-
mendations on screening for chloroquine and hydroxychlo-
roquine retinopathy. Ophthalmology 2011;118:415-22.
L’auteur déclare ne pas avoir
deliens d’intérêts.
1
/
5
100%