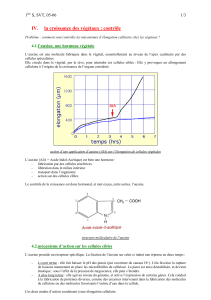
HORMONES FONGIQUES, ECTOMYCORHIZES ET RHIZOGÉNÈSE

HORMONES FONGIQUES,
ECTOMYCORHIZES ET RHIZOGÉNÈSE
ChafikaKARABAGHLI -B.SOTTA -G.GAY
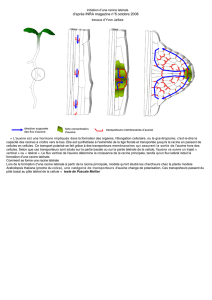
Les hormones végétales participent àla régulation de lacroissanceet du développement des
plantes,en réponsenotamment aux facteurs environnementaux.Défini d’abordenphysiologie
animale,le terme d’hormone se réfèreàdes substances organiques actives à très faible concentra-
tion et qui,produites dans un tissu, sont le plus souvent transportées vers unautre tissu où elles
déclenchent une réponsephysiologiquedonnée. Cinq familles d’hormones végétales sont connues
àcejour :les auxines,les cytokinines,les gibbérellines,l’acide abscissiqueet l’éthylène.
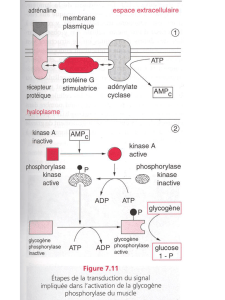
Les rôles des phytohormones ont étédécouverts principalement grâceàdes apports exogènes sur
les plantes mais les mécanismes d’action au niveau cellulaire sont encore très malconnus.Ilest
frappant de constater qu’un sipetit nombredemolécules,contenant en elles-mêmes très peu d’in-
formations,orientent et régulent toutes les étapes de croissanceet de développement des plantes.
Le rapport entreles différentes hormones présentes dans un tissu,leur quantité,l’organe ciblé et
son stade de développement, sont autant de facteurs qui vont déterminer le type de réponse
physiologiqueet le sens de la réponse:inhibition ou activation.
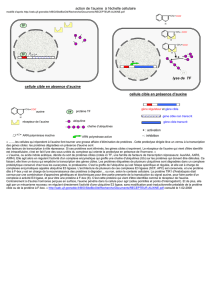
Les auxines ont étéles premières phytohormones découvertes et les plus étudiées.En1880,Darwin
met en évidence unfacteur agissant àdistance, responsable de l’élongation et de lacourburedes
coléoptiles d’avoine sous l’action de lalumière. Paàl,en 1919,établit lanaturehormonale de ce
facteur quiest isolé par Went en 1926 et nommé auxine (du grecauxein :accroître). En1931,Kögl
et Haagen-Smit purifient l’auxine et établissent sacomposition chimique(in Raven et al.,1986). La
principale auxine activeprésentedans les plantes est l’acide indole-3-acétique(AIA)et,générale-
ment,le terme d’auxine désigne cettemolécule. L’AIA est non seulement responsable du phototro-
pisme mais est aussiimpliquédans la réponsegravitropique. Cettehormone participe également au
contrôle de lacroissancedes fruits,de ladominanceapicale,de l’élongation des tiges et de nom-
breux processus mettant en jeu ladivision et ladifférenciation cellulaires.Ainsi,l’AIA est-il bien
connu pour déclencher les divisions du cambiumet favoriser l’apparition de racines adventives sur
les boutures tout en inhibant leur élongation.
Ungrand nombredemicro-organismes,bactéries et champignons sont capables de produiredes
hormones végétales (Akiyoshi et al.,1987;Strzelczyket Pokojska-Burdziej,1984 ; Frankenberger et
Arshad,1991 ; Young et al.,1991) et peuvent ainsiinfluencer le développement des plantes.C’est,
en particulier,le cas des champignons ectomycorhiziens.
L’objet de cet article est de fairelepoint des connaissances actuelles sur laproduction d’hormones
végétales par les champignons ectomycorhiziens et sur le rôle de ces hormones au cours de la
99
Rev.For.Fr.XLIX -n°sp. 1997

formation des ectomycorhizes.Nous commencerons par montrer quelaplupart des champignons
ectomycorhiziens peuvent synthétiser des phytohormones,en particulier l’acide indole-3-acétique.
Puis,nous concentrerons notreattention sur cetteauxine dont nous essaierons de préciser le rôle
dans l’établissement de la symbioseectomycorhizienne ; enfin,nous présenterons différents travaux
quiont utilisélacapacitéde synthèsed’auxine par les champignons ectomycorhiziens pour favori-
ser laformation de racines adventives sur des boutures.
LES CHAMPIGNONS ECTOMYCORHIZIENS SYNTHÉTISENT DES HORMONES VÉGÉTALES
Certains champignons ectomycorhiziens libèrent des cytokinines (Ho,1987a, 1987b; Kampert et
Strzelczyk,1990;Kraigher et al.,1991),des gibbérellines (Gogala, 1971) ou de l’éthylène (Graham
et Linderman,1980;DeVries et al.,1987)mais laproduction de ces phytohormones est beaucoup
moins fréquenteparmi les champignons ectomycorhiziens quecelle de l’auxine. Denombreux
auteurs ont montréqueles champignons ectomycorhiziens étaient capables de synthétiser de l’AIA
lorsqu’ils sont cultivés sur unmilieu contenant du tryptophane (Ulrich,1960 ; Eket al.,1983;
Strzelczyket Pokojska-Burdziej,1984 ; Frankenberger et Poth,1987; Gay et al.,1989). Les pre-
mières méthodes d’analysedel’AIA utilisées étaient des tests biologiques mesurant notamment la
courburedecoléoptiles d’avoine en réaction àl’application d’auxine. Ces tests sont sensibles mais
relativement difficiles à réaliser et peu reproductibles.Les réactifs colorés,plus simples àemployer,
présentent cependant l’inconvénient d’êtrepeu spécifiques et environ 100 fois moins sensibles que
les précédents.
Dans toutes les études antérieures aux années80,l’auxine produitepar les champignons ectomy-
corhiziens était détectée en utilisant des réactifs colorés parfois associés àlachromatographie sur
couche mince. La faible sensibilitédeces méthodes permettait de détecter une production d’AIA
seulement lorsqu’unprécurseur de l’auxine,comme le tryptophane,était ajoutéau milieu de culture,
àdes concentrations allant jusqu’à10 ou 50mM(1).La quantitéd’AIA produitedans ces conditions
était énorme,doncfacilement détectable,mais n’avait aucune signification physiologique. La
conclusion de ces études est quelaplupart des champignons ectomycorhiziens ne sont pas
capables de produiredel’auxine en l’absencedeprécurseur exogène. Toutefois,le développement
des méthodes d’analyse, telles quelachromatographie liquide hauteperformanceou lachromato-
graphie en phasegazeuseassociées àla spectrométrie de masse,ou encorel’immunochimie,ont
permis de doser avecprécision des quantités d’auxine de l’ordredelapicomole. Ces méthodes,
dans tous les cas où elles ont été utilisées,ont permis de détecter des quantités d’auxine très
faibles,mais suffisantes pour affecter laphysiologie d’un système racinaire,dans les milieux de
culturedes champignons ectomycorhiziens cultivés en l’absencedeprécurseur (Eket al.,1983;
Frankenberger et Poth,1987;Gay et al.,1994). Sur labasedeces résultats,il semble réalistede
considérer quelaplupart des champignons ectomycorhiziens sont capables de produiredes
quantités physiologiquement actives d’AIA, même en l’absencedeprécurseur.
Silaproduction d’auxine est très commune parmi les champignons ectomycorhiziens,les quantités
synthétisées varient énormément entreles espèces,entreles souches d’une même espèceet même
au sein de ladescendanced’une seule souche (Gay et Debaud,1987). Deplus,les conditions de
cultureinfluencent beaucouplaquantitéd’AIA synthétisée :des conditions de culturedéfavorables
au métabolisme primaire stimulent laproduction d’AIA (Gay,1986). Onpeut remarquer queles
conditions de culturefavorables àl’établissement de la symbioseectomycorhizienne,notamment de
faibles concentrations en azote, sont également très favorables àla synthèsed’AIA par les
champignons ectomycorhiziens (Gay,1988).
ChafikaKARABAGHLI -B.SOTTA -G.GAY
100
(1) mM=millimolaire.

La généralitédelacapacitéde synthèsedel’AIA parmi les champignons ectomycorhiziens a suscité
de nombreux travaux sur le rôle de cettehormone dans laformation des ectomycorhizes.Le rôle
des autres phytohormones qui sont synthétisées par certains champignons ectomycorhiziens est,
quant àlui,encoremalconnu.Par ailleurs,il est vraisemblable que,lorsqueplusieurs hormones
peuvent être synthétisées,elles interagissent et leur rôle respectif est plus difficile àcerner.C’est
pourquoi la suitedecet article est focalisée sur le rôle de l’AIA fongiquedans l’établissement de la
symbioseectomycorhizienne.
RÔLE DE L’AUXINE FONGIQUE DANS L’ÉTABLISSEMENT
DE LA SYMBIOSE ECTOMYCORHIZIENNE
L’auxine modifie lamorphologie des systèmes racinaires
Les systèmes racinaires colonisés par des champignons ectomycorhiziens sont hyper-ramifiés.Les
causes de cettehyper-ramification ont étéparticulièrement étudiées dans le cas des pins qui
forment des mycorhizes dichotomes.Slankis (1950,1973)a soumis des racines excisées de Pin syl-
vestreà unapport d’auxine synthétiqueou de filtrats de culturedechampignons ectomycorhiziens
comme Suillus luteus ouSuillus variegatus.Ce traitement induit laformation de racines courtes,
dichotomes,dépourvues de poils absorbants,ayant une morphologie semblable àcelle des ecto-
mycorhizes.Unapport régulier d’auxine est nécessairepour stabiliser ces déviations morpholo-
giques quidisparaissent dès l’arrêt du traitement.Slankis en aconclu quel’auxine produitepar le
champignon était indispensable àl’établissement et au maintien de la symbioseectomycorhizienne.
Ilaétabli unparallèle entrelefait quel’élévation de la teneur en azotedu milieu de cultureprovo-
quait ladisparition des mycorhizes pré-existantes tout en inhibant laformation de nouvelles myco-
rhizes et bloquait la synthèsed’auxine fongique. Sur labasedeces résultats,Slankis (1973)a
proposé une théorie “hormonale” de laformation des mycorhizes.Selon cette théorie,lamorpholo-
gie typiquedes systèmes racinaires porteurs d’ectomycorhizes serait dueàl’auxine fongique. En
stimulant l’activité rhizogène de laplante,l’AIA fongiqueaugmenterait le nombrede sites potentiels
de colonisation et favoriserait ainsil’établissement de l’association symbiotique. Deplus, unflux
continu d’auxine fongique serait indispensable au maintien de l’association symbiotique.
L’interruption de ceflux par une augmentation de la teneur en azotedu milieu de culture,quiinhibe
laproduction d’AIA fongique,provoquerait ladisparition de la symbiose.
La théorie “hormonale” de Slankis sous-entend quel’apport d’AIA fongiquedevrait provoquer une
hyper-auxinie dans les racines colonisées.Mais une hyper-auxinie racinairepourrait aussiêtrela
conséquenced’une inhibition des auxines-oxydases racinaires.Or,on sait quedenombreux cham-
pignons ectomycorhiziens produisent des composés phénoliques et des flavonoïdes quipeuvent
inactiver les auxines-oxydases de l’hôte. De tels composés peuvent également être synthétisés par
laplante-hôte,en réponseàlacolonisation fongique. Bien quel’hyper-auxinie des mycorhizes
demeure une hypothèse, une influencedes composés phénoliques fongiques sur le métabolisme
auxiniquedes racines colonisées ne peut pas êtreexclue(Gay et al.,1982). Cependant,la théorie
de Slankis aétébeaucoupdiscutée,notamment par Harley et Smith(1983)qui soulignent qu’elle ne
s’appuie sur aucune donnée expérimentale précise.
Des souches fongiques surproductrices d’auxine ont une activitémycorhizogène accrue
Des mutants surproducteurs d’auxine du champignon ectomycorhizien Hebelomacylindrosporum
Romagnésiont été sélectionnés par Durand et al.(1992)en vuedeconstituer unmodèle biologique
permettant de préciser le rôle de l’AIA fongiquedans la symbioseectomycorhizienne. Lorsqu’ils sont
associés avecleur plante-hôtehabituelle,le Pin maritime (Pinus pinaster),ces mutants forment plus
de mycorhizes quela souche sauvage (figure1,p. 102). Leurs descendances mono- et di-caryo-
tiques ont étéisolées et l’activitémycorhizienne d’unéchantillon de 80monocaryons fils et des
Lefonctionnement des symbioses mycorhiziennes
101
Rev.For.Fr.XLIX -n°sp. 1997

ChafikaKARABAGHLI -B.SOTTA -G.GAY
102
Figure1 PLANTS DE PIN MARITIME (PINUS PINASTER )ÂGÉS D’UN MOIS ET MYCORHIZÉS IN VITRO
AVEC LE CHAMPIGNON ECTOMYCORHIZIEN HEBELOMA CYLINDROSPORUM
L’activitémycorhizogène de la souche monocaryotique sauvage h1 (bet c)et celle de la souche monocaryotiquemutante 331
(a, d,e,f) surproductriced’AIA ont étécomparées.
Barre=5mm; i:inoculumfongique; flèche :exemples de mycorhizes dichotomes.
abc
def

dicaryons obtenus en effectuant tous les croisements possibles entreces monocaryons aété
étudiée (Gay et al.,1994). L’activitémycorhizienne des monocaryons présente une variation conti-
nue,cequiindiquequelecontrôle de l’établissement de l’association symbiotiqueest polygénique.
L’activitémoyenne des monocaryons présentant le phénotype sauvage correspond àl’activitédu
parent sauvage alors queles monocaryons surproducteurs d’AIA ont,en général, une activitémyco-
rhizienne plus forte,comparable àcelle du parent mutant.Tous les dicaryons homozygotes pour la
mutation àl’origine de la surproduction d’AIA forment plus de mycorhizes queles monocaryons
présentant cettemutation. Selon Gay et al. (1995),l’ensemble des résultats obtenus avecces
mutants montrequel’AIA fongiqueest undes déterminants de l’infectivitédes champignons
ectomycorhiziens.
L’auxine fongiqueparticipe-t-elle àl’établissement et au fonctionnement des ectomycorhizes?
Le réseau de Hartig joue un rôle essentiel dans le fonctionnement de la symbiose. C’est l’interface
où sefont les échanges entreles deux partenaires.Ilest constituépar des hyphes quipénètrent
entreles cellules corticales de la racine-hôte. Dans les mycorhizes formées par les souches sau-
vages,ce réseau est “normal”,c’est-à-direconstituéd’une seule couche d’hyphes quin’atteignent
en généralpas l’endoderme (figure2,p. 104). En revanche,le réseau de Hartig est hypertrophié
dans le cas des ectomycorhizes formées par les mutants surproducteurs d’AIA.Les cellules végé-
tales sont entourées de plusieurs couches d’hyphes (de 1à8) quiatteignent l’endoderme de la
racine (figure3,p. 104). Les hyphes de la souche mutantepeuvent même pénétrer àl’intérieur des
cellules végétales vivantes du parenchyme cortical,cequin’est jamais le cas dans les ectomyco-
rhizes normales (Geaet al.,1994). Ces résultats indiquent quel’AIA fongiqueest impliquédans la
miseenplacedu réseau de Hartig. Des mesures cytométriques ayant montréquel’AIA libérépar le
champignon affecteaussilapolaritédecroissancedes cellules corticales des racines colonisées,
on peut émettrel’hypothèsequel’auxine fongiquepourrait faciliter laformation du réseau de Hartig
en affectant le métabolisme de laparoi des cellules-hôtes.Eneffet,on sait que,dans les tiges,l’AIA
induit une acidification de l’espacepériplasmiquequiprovoque un relâchement de la structurede
laparoi. Ce ramollissement de laparoi permet le grandissement cellulaire. Si un tel mécanisme exis-
tait dans les mycorhizes,il pourrait favoriser lapénétration intercellulairedes hyphes du réseau de
Hartig. Dans le cas du mutant surproducteur d’AIA, un relâchement excessif de laparoi pourrait
expliquer l’hypertrophie du réseau de Hartig ainsiqueles changements de polaritédecroissance
des cellules corticales.
L’auxine fongique semble aussiaffecter le métabolisme carboné de laplante. Eneffet,lafortepro-
lifération mycélienne dans les mycorhizes formées par les mutants surproducteurs d’AIA représente
uncoût supplémentaireenhydrates de carbone pour laplantepar rapport aux mycorhizes formées
par la souche sauvage. Or,les plants mycorhizés contiennent plus de sucres solubles (glucose,fruc-
tose, saccharose) queles plants témoins,et les plants inoculés par unmutant sont plus riches en
sucres solubles queceux mycorhizés par une souche sauvage. Ainsi,bien que représentant uncoût
élevéenhydrates de carbone,la symbiosemycorhizienne se traduit par une amélioration du bilan
carboné de laplante-hôte. Soulignons quel’auxine est typiquement unmessager capable d’affec-
ter laphysiologie de tissus éloignés des sites où elle aétéproduite. Àce titre,l’auxine fongique
produitedans les mycorhizes pourrait affecter laphysiologie de lapartie aérienne et notamment
l’activitéphotosynthétiquedelaplante.
Récemment, un résultat extrêmement important et porteur de nombreuses perspectives aétépublié
par Nehls et Martin (1995) quiont montréqu’ungène régulé par l’auxine,le gène par,est surex-
primé dans les mycorhizes formées par Eucalyptus globulus associé àPisolithus tinctorius.Ce résultat
suggèrequel’auxine fongiquepourrait affecter l’expression des gènes de laplante-hôteet ouvrela
voie vers des études concernant le rôle de l’auxine fongiqueen tant quemédiateur des interactions
génétiques entreles partenaires de la symbioseectomycorhizienne.
Lefonctionnement des symbioses mycorhiziennes
103
Rev.For.Fr.XLIX -n°sp. 1997
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%