Comment obtenir un réglage optimal d`un stimulateur cardiaque ?

Revue
Comment obtenir un réglage optimal
d’un stimulateur cardiaque ?
Gaël Jauvert, Christine Alonso, Arnaud Lazarus
Inparys, 12 rue Pasteur, 92210 Saint-Cloud
Résumé.La stimulation cardiaque ne se résume pas à la mise en place d’une prothèse et au simple suivi de l’état de la batterie. Les indications
de stimulation cardiaque ont évolué avec une majorité d’implantations pour dysfonctions sinusales et un nombre croissant de stimulations
multisites à visée hémodynamique dans l’insuffisance cardiaque. Les prothèses doivent donc répondre de manière aussi physiologique que
possible pour ne pas générer de symptômes potentiellement plus inconfortables que ceux ayant conduit à l’indication d’implantation. Il existe
de nombreux paramètres programmables. Certains sont essentiels au bon fonctionnement du système de stimulation. Leur programmation
adéquate et leur optimisation souvent individuelle sont primordiales.
Mots clés : stimulation cardiaque, optimisation, échocardiographie
Abstract. How to achieve optimal pacemaker settings? Cardiac pacing can not be reduced any more to a device implantation and its
battery drain follow-up. Pacing indications have evolved and increased displaying a large part for sinus node dysfunction and a growing number
of multisite pacing for heart failure. As far as pacing may generate very uncomfortable detrimental effects, devices are expected to provide the
most physiological therapy. Programmable parameters are numerous. Some of them are essential to warrant an appropriate functioning. Their
adequate programming and their often individual optimisation is fundamental.
Key words: cardiac pacing, optimization, echocardiography
Chaque année, environ 60 000 sti-
mulateurs sont implantés en
France : des doubles chambres en
grande majorité avec une part crois-
sante de stimulateurs triple chambre
de resynchronisation (environ 20 %).
Les indications de stimulation sont
majoritairement des dysfonctions si-
nusales associées ou non à des trou-
bles du rythme supraventriculaire. Le
nombre de défibrillateurs implanta-
bles est croissant en rapport avec l’ex-
tension des indications de prévention
primaire. Deux tiers sont des appareils
double ou triple chambre. Par consé-
quent, la fonction stimulation est au
premier plan.
Les appareils sont devenus de plus
en plus paramétrables dans le but de
rendre leur fonctionnement le plus
physiologique possible. Ils embar-
quent également diverses fonctions
diagnostiques de plus en plus perfor-
mantes et complètes. Leur interpréta-
tion et leur utilisation permettent
d’améliorer la qualité du suivi et de la
programmation.
Le suivi périodique de ces appa-
reils dans un centre de rythmologie est
primordial. Au cours de ce suivi, le
bon fonctionnement de la prothèse est
vérifié, les fonctions diagnostiques
sont interrogées et remises à zéro, le
réglage des paramètres est optimisé si
nécessaire. Les données recueillies
sont alors synthétisées et transmises au
cardiologue et/ou au médecin traitant.
Un réglage inadapté ou bien non
optimal peut avoir des conséquences
cliniques dont les symptômes peuvent
être plus inconfortables que ceux, dif-
férents, éventuellement présents au
moment de l’implantation. Il ne s’agit
plus seulement et depuis bien long-
temps de palier une bradycardie ex-
trême par une stimulation mono-
chambre à fréquence fixe, mais de
répondre à des indications plus pro-
phylactiques de façon physiologique.
m
t
c
Tirés à part : G. Jauvert
mt cardio 2008 ; 4 (2) : 163-75
mt cardio, vol. 4, n° 2, mars-avril 2008 163
Revue
doi: 10.1684/mtc.2008.0138
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Effets délétères de la stimulation
cardiaque
Le syndrome du pacemaker et la désynchronisation
ventriculaire représentent les meilleurs exemples des ef-
fets délétères de la stimulation cardiaque. Il en existe
d’autres.
Le syndrome du pacemaker a été initialement décrit
chez les patients porteurs de stimulateurs VVI pour bloc
auriculo-ventriculaire (BAV) complet alors que les oreillet-
tes sont sinusales. Une dyspnée, voire une blockpnée
d’effort, peut être associée à une asthénie, des douleurs
thoraciques, des malaises lipothymiques, et des troubles
vasomoteurs désagréables. Bien entendu aujourd’hui en
France, la mise en place d’un stimulateur VVI pour BAV
complet avec ondes P sinusales est exceptionnelle ; ce-
pendant, l’indication d’une stimulation double chambre
pourrait être discutable et l’a été ou l’est encore dans
d’autres pays d’Europe, tant la preuve de la supériorité
d’une stimulation DDD versus VVI n’est pas évidente en
termes de morbi-mortalité et de survenue d’arythmies à
l’échelle d’une population. Le syndrome du pacemaker
n’a pas pour autant disparu avec la stimulation double
chambre. On peut définir le syndrome du pacemaker
comme la conséquence d’une « synchronisation auriculo-
ventriculaire suboptimale » selon Ellenbogen, entraînant
la mise en jeu du système nerveux autonome pour s’adap-
ter aux perturbations hémodynamiques induites [1, 2]. Les
symptômes sont liés à la perte de la systole atriale et à la
mise en jeu du système nerveux autonome. Leurs méca-
nismes physiopathologiques, en partie liés à une hypoten-
sion, restent mal connus. Cette hypotension peut être (au
moins partiellement) la conséquence d’une sécrétion
inappropriée de facteur natriurétique atrial.
La stimulation ventriculaire (apicale le plus souvent)
permanente a potentiellement des effets hémodynami-
ques délétères. Ils expliquent en partie pourquoi la stimu-
lation double chambre, « a priori plus physiologique »,
n’a pas supplanté la stimulation monochambre de ma-
nière éclatante [3-6]. De nombreux travaux ont bien mon-
tré que la stimulation ventriculaire droite apicale pouvait
être responsable à plus ou moins long terme d’insuffisance
cardiaque systolique, par altération de la fonction ventri-
culaire gauche et dilatation cavitaire [7-11]. La stimulation
ventriculaire apicale droite peut en effet induire un remo-
delage ventriculaire et modifier les propriétés électriques
du myocarde [12]. Des troubles conductifs distaux, intra-
ventriculaires gauches accentués ou révélés par la stimu-
lation monoventriculaire droite sont à l’origine d’une dé-
synchronisation intraventriculaire gauche, elle-même
responsable de l’accentuation ou de l’apparition de signes
d’insuffisance cardiaque.
Ces effets hémodynamiques indésirables ont eux-
mêmes des conséquences électrophysiologiques poten-
tielles. La survenue de troubles du rythme ventriculaire
graves peut compliquer l’évolution d’une insuffisance car-
diaque systolique. Une désynchronisation auriculo-
ventriculaire induite par la stimulation cardiaque entraîne
volontiers une dilatation atriale et la survenue d’arythmie
supraventriculaires [13-15].
Réglage des paramètres de base
Polarité de stimulation/détection
Les sondes de stimulateurs implantées aujourd’hui
sont en grande majorité bipolaires. En mode unipolaire, la
détection et la stimulation s’effectuent entre le boîtier et
l’électrode distale de la sonde. En mode bipolaire, elles
s’effectuent entre les électrodes proximale et distale de la
sonde séparée de 10 à 15 mm. Les stimulateurs sont livrés
en mode unipolaire.
La détection doit être reprogrammée en mode bipo-
laire car le champ étant restreint en intracardiaque, le
risque d’interférence extérieure ou de détection de myo-
potentiels est quasi nul. Le risque de détection d’onde T
par la sonde ventriculaire ou d’onde R par la sonde atriale
est également minimisé. Le niveau de détection peut donc
être reprogrammé plus bas pour une meilleure sensibilité
notamment dans l’oreillette. La qualité de la détection
atriale est déterminante pour le bon fonctionnement d’un
système double chambre.
La reprogrammation de la stimulation en mode bipo-
laire peut être très utile en cas de stimulation phrénique ou
pectorale.
En stimulation multisite, les appareils de première
génération avaient sur le connecteur deux « sorties » ven-
triculaires, qui n’étaient autres que la division d’un même
canal ventriculaire. Les canaux ventriculaires sont depuis
véritablement séparés. Il est donc possible de programmer
des énergies de stimulation différentes sur chaque sonde,
adaptées à leurs seuils respectifs de stimulation. Il est
également possible de programmer des configurations de
détection et de stimulation multiples. Les différentes
options possibles de stimulation, notamment de la sonde
ventriculaire gauche (VG) (monopolaire, bipolaire,
Liste des abréviations
AV : auriculo-ventriculaire
BAV : bloc auriculo-ventriculaire
DAV : délai atrio-ventriculaire
ECG : électrocardiogramme
PRAPV : période réfractaire atriale post ventriculaire
PRAT : période réfractaire atriale totale
TRE : tachycardie par réentrée électronique
VD : ventricule droit
VG : ventricule gauche
VTI : intégrale temps-vitesse
VV : délai ventriculo-ventriculaire
Comment obtenir un réglage optimal d’un stimulateur cardiaque ?
mt cardio, vol. 4, n° 2, mars-avril 2008
164
Revue
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

bipolaire inversée, bipolaire étendue entre la sonde VD et
la sonde VG) permettent parfois de palier une stimulation
phrénique ou bien d’améliorer de façon très significative
le seuil de stimulation. Cette programmabilité permet dans
nombre de cas d’éviter de réintervenir pour repositionner
la sonde gauche et d’espérer une longévité accrue de la
prothèse.
Seuil de stimulation, détection,
période réfractaire atriale
Ces trois paramètres ne sont bien entendu pas les seuls
qui méritent une programmation simple mais adaptée ; il
s’agit des principaux, des incontournables.
Après une période de cicatrisation de 3 à 6 mois
pendant laquelle les seuils de stimulation peuvent éven-
tuellement s’élever, ces derniers atteignent généralement
un plateau, on parle de seuils chroniques. Les appareils
sont livrés avec une programmation de stimulation de
3,5 volts pour 0,4 ms de largeur d’impulsion en général.
Pour garantir une stimulation efficace, l’énergie de stimu-
lation doit être égale à 2 fois le seuil de stimulation, c’est la
marge de sécurité. Pour garantir une longévité normale, il
est généralement possible et recommandé de réduire
l’énergie de stimulation à moins de 3 volts tout en gardant
la même marge de sécurité. La longévité d’un appareil est
la première préoccupation, sinon la principale, du patient
implanté ! Un système d’autocapture est présent sur cer-
tains modèles. Il permet de délivrer une énergie réduite
juste au-dessus du seuil, automatiquement mesuré par
l’appareil plusieurs fois par jour, tout en assurant la déli-
vrance immédiate d’une énergie bien plus élevée en cas
de perte de capture automatiquement détectée par l’appa-
reil (réponse évoquée...).
Une détection correcte garantit un fonctionnement
approprié de la stimulation. L’amplitude des signaux re-
cueillis dans l’oreillette est plus faible que dans les ventri-
cules, et davantage en cas d’arythmie supraventriculaire.
La sensibilité atriale programmée doit être suffisamment
élevée, inférieureà1mV,pour pouvoir détecter les ondes
P sinusales voire plus élevée, inférieure à 0,5 mV pour
détecter une activité atriale en arythmie mais pas trop
élevée pour éviter les surdétections de signaux extra-
atriaux. La détection des ondes P sinusales garantit la
synchronisation atrio-ventriculaire. La détection des seu-
les arythmies supraventriculaires garantit un repli efficace
et approprié du stimulateur. En effet, afin d’éviter une
synchronisation AV prolongée (et donc un rythme ventri-
culaire stimulé rapide) en tachycardie supraventriculaire,
l’appareil interrompt automatiquement la séquence AV : il
commute de façon réversible de DDD en VVI pendant la
durée du trouble du rythme.
La période réfractaire atriale totale (PRAT) est la
somme du délai atrio-ventriculaire (DAV) et de période
réfractaire atriale post-ventriculaire (PRAPV) dont le but
est d’éviter la prise en compte d’une éventuelle onde P
rétrograde ou une télé onde R, qui induirait un nouveau
DAV et une possible tachycardie par réentrée électronique
(TRE). La PRAT définit donc l’intervalle minimum possible
entre deux stimulations atriales (fréquence max) et entre
une onde P spontanée et une stimulation ventriculaire
synchrone (fréquence max synchrone et point de 2/1).
La programmation de la période réfractaire atriale et de la
fréquence maximale synchrone doit donc être adaptée
aux capacités d’effort d’un patient. Une désynchronisation
AV « programmée » trop précoce peut être mal vécue
chez un patient stimulé pour BAV dont le rythme sinusal
peut encore physiologiquement s’accélérer au-delà de
140 bpm.
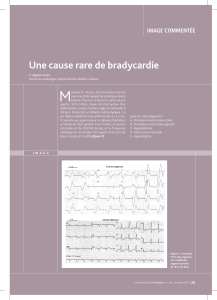
L’épreuve d’effort est un outil intéressant, parfois indis-
pensable pour vérifier notamment la bonne détection
atriale à l’effort, le comportement approprié du délai atrio-
ventriculaire ou l’absence de surdétection (myopotentiels)
(figure 1).
Réglage de l’asservissement de fréquence
La dysfonction sinusale et l’incompétence chrono-
trope, spontanées ou induites par des traitements que l’on
ne peut pas interrompre ou remplacer, sont très fréquen-
tes. L’incompétence chronotrope peut apparaître d’em-
blée ou s’aggraver avec le temps. Elle est corrigée par la
mise en route de l’asservissement de fréquence. Les pro-
thèses sont munies d’un capteur d’exercice. Il en existe
deux types principaux : accéléromètre et ventilation-
minute. Selon les fabricants, les stimulateurs possèdent
l’un ou l’autre type ou les deux, pouvant être activés
séparément ou simultanément. Sollicité, ce capteur dé-
clenche une réponse se traduisant par une accélération de
la fréquence de base jusqu’à une fréquence max pro-
grammable selon une pente d’accélération également
programmable. A l’arrêt de l’effort, la fréquence décroît
progressivement selon une pente programmable.
L’incompétence chronotrope se manifeste généralement
par une dyspnée d’effort et/ou une fatigue musculaire
souvent durement et injustement ressenties. Chez les pa-
tients ayant une stimulation ventriculaire permanente, ce
symptôme peut bien entendu faire suspecter et rechercher
une désynchronisation ventriculaire qui peut n’être pré-
sente qu’à l’effort. La programmation de l’asservissement
de fréquence doit être adaptée au patient (âge, niveau
d’activité, sport) et à sa cardiopathie. Une cardiopathie
ischémique stable ne contre-indique pas la mise en route
d’un asservissement de fréquence adapté. Les stimulateurs
proposent en général la possibilité d’une gestion automa-
tique de la pente. Cela peut suffire, mais il peut être
difficile d’obtenir d’emblée une réponse optimale, même
chez des patients a priori sédentaires. Un réglage manuel
est parfois nécessaire. Une épreuve d’effort peut s’avérer
indispensable pour affiner la programmation.
mt cardio, vol. 4, n° 2, mars-avril 2008 165
Revue
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Optimisation du délai
atrio-ventriculaire
Le DAV est un paramètre fondamental des stimula-
teurs. Il détermine la synchronisation AV. Son réglage est
d’autant plus important qu’il existe une cardiopathie.
Le DAV optimal pourrait être défini de différentes
manières.
–Il peut s’agir du DAV programmé (sur une onde P
stimulée ou détectée) permettant d’obtenir le meilleur
remplissage cardiaque gauche grâce à la meilleure syn-
chronisation auriculo-ventriculaire gauche ; autrement
dit, il s’agit d’obtenir le remplissage mitral le plus long
associé à une systole atriale complète la plus distincte
possible de l’onde E et non interrompue par la systole
ventriculaire pour une fréquence cardiaque donnée.
–Il peut s’agir au contraire d’un compromis entre 2 va-
leurs de DAV différentes : l’une optimale pour le remplis-
sage cardiaque gauche, l’autre pour le remplissage ventri-
culaire droit.
–Il peut enfin s’agir d’un DAV ne visant pas forcément le
meilleur remplissage gauche mais permettant la systole
ventriculaire gauche la plus performante possible.
Il faut avoir à l’esprit que les oreillettes seront stimulées
ou détectées à partir d’une sonde se trouvant dans
l’oreillette droite...
A l’état basal, chez le sujet sain, la contribution de
l’oreillette gauche au remplissage ventriculaire (et au débit
AB
C
D
Figure 1.Période réfractaire atriale totale trop longue. Comportement de la synchronisation AV chez un patient sportif en stimulé pour BAV
complet présentant une dyspnée d’effort. A) Synchronisation 1:1 au repos. B) Phénomène de Wenckebach électrique à l’effort : certaines ondes
P sinusales tombent en période réfractaire et ne sont pas conduites. C) Au maximum de l’effort : une onde P sur deux est en période réfractaire,
le rythme ventriculaire a brutalement chuté. D) Même patient après reprogrammation du DAV d’effort et de la PRAPV. L’association AV 1:1 est
respectée. L’épreuve d’effort a permis de le vérifier.
Comment obtenir un réglage optimal d’un stimulateur cardiaque ?
mt cardio, vol. 4, n° 2, mars-avril 2008
166
Revue
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

cardiaque) n’est que 20 % environ. Mais cette proportion
augmente en cas de dysfonction diastolique, en fonction
des pressions de remplissage du ventricule gauche. Elle est
d’autant plus grande que la fraction d’éjection est basse.
En revanche, en cas de pressions trop élevées, cette contri-
bution s’effondre [16-19].
Un retard d’activation et de contraction de l’oreillette
gauche secondaire à un trouble conductif inter- ou intra-
auriculaire peut avoir des conséquences hémodynami-
ques. Indépendamment de toute stimulation cardiaque,
Ramsaran et al. [20] ont montré, chez des patients ayant
des troubles conductifs interatriaux incomplets ou avan-
cés authentifiés à l’ECG, qu’il existe une corrélation étroite
entre le retard d’activation atriale gauche et le retard de la
systole atriale gauche par rapport à la systole atriale droite,
évalué par l’étude du flux mitral à l’échographie, affirmant
ainsi que le retard de contraction de l’oreillette gauche est
bien la conséquence directe d’un bloc intra- et/ou inter-
atrial. De tels troubles conductifs peuvent être accentués
ou révélés par la stimulation atriale droite, de façon varia-
ble en fonction du site, de la fréquence et de l’énergie de
stimulation [21, 22]. Il en résulte que la programmation
d’un délai auriculo-ventriculaire « standard » compris
entre 150 et 200 ms a priori «physiologique» n’entraîne
A
B
C
Figure 2. Détermination du DAV optimal au repos sur onde P détectée par la formule de Ritter chez un patient stimulé pour BAV
complet. A) DAV court, B) DAV long, C) DAV optimal.
mt cardio, vol. 4, n° 2, mars-avril 2008 167
Revue
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%