Revue Vieillissement cardiovasculaire, dysfonction diastolique et

Revue
Vieillissement
cardiovasculaire,
dysfonction diastolique
et insuffisance cardiaque
François Puisieux
Service de Médecine Interne et de Gériatrie, hôpital gériatrique les Bateliers,
23 rue des Bateliers, CHRU Lille, 59037 Lille Cedex
Résumé. La prévalence de l’insuffisance cardiaque secondaire à une dysfonction diastolique
augmente considérablement avec l’âge. Cela est dû à l’effet du vieillissement cardiovasculaire
normal et à la forte prévalence chez la personne âgée des pathologies cardiaques qui peuvent
altérer le remplissage ventriculaire comme la maladie coronaire ou hypertensive. Contraire-
ment à la fonction systolique qui est relativement conservée, la fonction diastolique peut être
significativement altérée avec l’âge. Le vieillissement est associé à une rigidité augmentée de
la paroi artérielle des grosses artères, une augmentation de la pression artérielle systolique, un
épaississement de la paroi ventriculaire, une dysfonction diastolique caractérisée par une
diminution du remplissage protodiastolique et une augmentation de contribution atriale, un
débit cardiaque inchangé au repos et lors d’un effort sous-maximal. Les personnes âgées ayant
des anomalies infracliniques de la fonction diastolique sont prédisposées à développer une
insuffisance cardiaque congestive à l’occasion d’un événement précipitant comme une
fibrillation auriculaire, une tachycardie soutenue, une ischémie, une anémie, des poussées
tensionnelles ou une surcharge volumique.
Mots clés : insuffisance cardiaque, dysfonction diastolique, vieillissement
L’insuffisance cardiaque est une
pathologie fréquente et grave
chez le sujet âgé. En France, en 1991,
l’incidence de la maladie a été esti-
mée à 120 000 nouveaux cas par an,
dont les deux tiers intéressent des su-
jets de plus de 75 ans [1]. La préva-
lence de la maladie augmente de ma-
nière exponentielle après l’âge de
60 ans et passe de 1 % dans la sixième
décennieà8à9%dans la huitième
décennie dans l’étude Framingham
[2, 3]. L’âge moyen des patients insuf-
fisants cardiaques est d’environ
75 ans en France. L’insuffisance car-
diaque serait la première cause d’hos-
pitalisation et d’hospitalisations répé-
tées de la personne âgée. Le taux de
mortalité des malades insuffisants car-
diaques augmente avec l’âge, de 27 %
par décennie chez les hommes et de
61 % par décennie chez les femmes
[2, 3]. Au total, 90 % des décès asso-
ciés à une insuffisance cardiaque sur-
viennent après 70 ans. La surmortalité
observée chez le sujet âgé s’explique
autant par la polypathologie qui com-
plique la prise en charge que par une
gravité plus grande de la maladie car-
diaque.
L’insuffisance cardiaque est
l’aboutissement final de nombreuses
cardiopathies. Chez le sujet âgé, les
étiologies peuvent être multiples et in-
triquées.
L’insuffisance cardiaque du sujet
âgé est aussi caractérisée par une
grande fréquence des formes à fonc-
tion systolique conservée [4, 5]. Chez
les insuffisants cardiaques de plus de
75 ans, la fonction systolique du ven-
tricule gauche est normale dans près
m
t
c
Tirés à part : F. Puisieux
mt cardio, vol. 1, n° 1, janvier-février 2005 57
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

de 50 % des cas [5-7]. Dans la récente étude Euro Heart
Failure qui a intéressé 11 327 patients hospitalisés pour
insuffisance cardiaque [8], 28 % des femmes avaient une
fraction d’éjection ventriculaire gauche inférieure à 40 %,
alors que c’était le cas pour 51 % des hommes.
Quoique de meilleur pronostic que l’insuffisance car-
diaque à fonction systolique altérée, l’insuffisance cardia-
que du sujet âgé reste marquée par une importante mor-
talité [6, 9, 10].
La prévalence élevée de l’insuffisance cardiaque et,
singulièrement, de l’insuffisance cardiaque à fonction sys-
tolique conservée chez le sujet âgé s’explique par le
vieillissement cardiovasculaire lui-même et par la grande
fréquence des cardiopathies ischémiques et hypertensives
[11].
Vieillissement de l’organisme
Le vieillissement correspond à l’ensemble des proces-
sus physiologiques qui modifient la structure et les fonc-
tions de l’organisme à partir de l’âge mûr. Il est la résul-
tante des effets intriqués de facteurs génétiques
(vieillissement intrinsèque) et de facteurs environnemen-
taux auxquels est soumis l’organisme tout au long de sa
vie. Le vieillissement s’accompagne d’une diminution des
réserves fonctionnelles de sorte que l’organisme âgé est
moins apte à s’adapter aux situations d’agression. La ré-
duction fonctionnelle liée au vieillissement est très varia-
ble d’un organe à l’autre (vieillissement différentiel inte-
rorgane) et d’un individu à l’autre. La population âgée est
ainsi caractérisée par une grande hétérogénéité. L’état de
santé d’une personne âgée résulte habituellement des
effets du vieillissement et des effets additifs de maladies
passées (séquelles), actuelles, chroniques ou aiguës.
Le vieillissement cardiovasculaire normal induit des
modifications de la structure et de la fonction des vais-
seaux et du cœur qui réduisent les réserves fonctionnelles
cardiaques. On est cependant jamais insuffisant cardiaque
du seul fait de son âge. L’insuffisance cardiaque est la
conséquence des maladies cardiovasculaires dont la pré-
valence augmente avec l’âge.
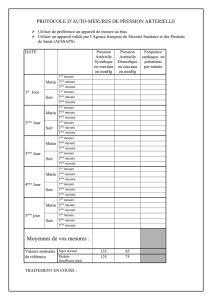
Les concepts de décompensation et de fragilité déve-
loppés en gériatrie et le « schéma 1+2+3»développés
par Bouchon s’appliquent parfaitement à la fonction car-
diaque (figure 1). Chez le sujet âgé, trois éléments contri-
buent à la décompensation d’une fonction :
–les effets du vieillissement qui réduisent progressive-
ment les réserves fonctionnelles, sans jamais à eux seuls
entraîner la décompensation,
–les affections chroniques surajoutées qui altèrent les
fonctions,
–les facteurs de décompensation qui sont souvent
multiples et associés chez un même patient : affections
médicales aiguës, pathologie iatrogène et stress psycholo-
gique.L’étude du vieillissement et particulièrement du
vieillissement cardiovasculaire chez l’homme est rendue
difficile par l’intrication possible avec les effets des mala-
dies cardiovasculaires très fréquentes au grand âge [12-
14]. Dans le passé, des études, principalement transversa-
les, ont pu conduire à des résultats erronés. Cependant,
nous disposons de données fiables chez l’homme qui
proviennent notamment d’importantes études longitudi-
nales comme la Baltimore Longitudinal Study qui suit des
participants volontaires rigoureusement sélectionnés pour
repérer les pathologies cardiovasculaires cliniquement
parlantes ou occultes. Nous disposons, d’autre part, de
données chez l’animal vieillissant qui éclairent les méca-
nismes intimes, même si les résultats ne sont pas immé-
diatement applicables à l’homme.
Vieillissement artériel
Il est nécessaire de rappeler en préambule que le
vieillissement artériel et l’athérosclérose sont deux phéno-
mènes distincts. Le vieillissement artériel est un processus
physiologique et diffus. L’athérosclérose est une maladie
multifocale. Si l’épaississement de l’intima et la dégéné-
rescence des fibres élastiques sont communs, l’accumula-
tion de lipides dans l’intima est propre à l’athérosclérose.
Cependant, les modifications liées au vieillissement favo-
risent le développement des lésions d’athérosclérose [15-
17]. La preuve en est apportée par les études chez le lapin
soumis à un régime hyperlipidique [16]. Pour la même
augmentation des lipides sanguins, les lésions d’athéros-
clérose se développent plus rapidement chez l’animal âgé
que chez l’animal jeune.
Le vieillissement physiologique du système cardiovas-
culaire et les modifications secondaires à l’hypertension
artérielle ont en revanche beaucoup de points communs.
Il n’est pas douteux que les contraintes hémodynamiques
auxquelles sont soumises les artères et le cœur jouent un
rôle essentiel dans le vieillissement cardiovasculaire. C’est
seuil de défaillance
1
2
2
3
Figure 1.Schéma1+2+3:analyse des performances d’un organe
sous l’effet du vieillissement (1), des pathologies chroniques (2) et des
pathologies intercurrentes (3).
Revue
mt cardio, vol. 1, n° 1, janvier-février 2005
58
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

une des raisons qui peut expliquer que toutes les artères ne
vieillissent pas de la même façon, ni au même rythme, car
elles ne sont pas toutes exposées au même régime de
pression.
Modifications de structure
Les principales modifications macroscopiques au
cours du vieillissement consistent en une augmentation de
calibre des grosses artères élastiques et un épaississement
de leur paroi [12-14]. Les diamètres interne et externe
augmentent. Les artères élastiques subissent aussi une
augmentation de longueur entraînant un déroulement de
la crosse de l’aorte et une tortuosité artérielle. Au niveau
des petites artères musculaires, il existe une majoration
moindre du diamètre externe mais l’augmentation de
l’épaisseur pariétale y est importante, entraînant une dimi-
nution du diamètre interne.
Les modifications touchent toutes les tuniques des
artères [12-14]. Des études post mortem ont indiqué que
l’épaississement de la paroi intéresse avant tout l’intima,
même dans les populations avec une faible incidence
d’athérosclérose [18]. Des mesures non invasives au ni-
veau de la carotide ont indiqué que l’épaisseur intima-
média était multipliée par deux ou trois entre 20 et 90 ans.
Il existe cependant une très grande hétérogénéité d’un
individu à l’autre appartenant pourtant à une même tran-
che d’âge. Comme l’ont montré des études déjà anciennes
chez l’animal, l’épaississement intimal est lié à l’accumu-
lation de collagène, de cellules musculaires lisses, de
mononucléaires et de macrophages [19, 20]. Il a été
avancé que l’épaississement intimal pouvait constituer un
premier stade de la maladie athéromateuse. En effet, un
épaississement intimal exagéré à un âge donné coexiste
fréquemment avec une maladie coronaire silencieuse, qui
peut elle-même évoluer vers une maladie coronaire clini-
que.
L’aspect morphologique des cellules endothéliales est
peu changé. Selon Gerrity et Cliff [20], les cellules endo-
théliales qui sont, chez le jeune rat, de forme losangique et
allongées dans la direction du flux sanguin, sont, chez le
rat âgé, plus arrondies, de plus grand volume et renfer-
ment des inclusions lipidiques. Ces changements pour-
raient rendre le flux sanguin moins laminaire et favoriser
les dépôts lipidiques.
Dans la média, le vieillissement induit un épaississe-
ment de la couche musculaire lisse. Les cellules muscu-
laires lisses sont modifiées. Leur nombre n’est pas changé
mais il y a une hypertrophie cellulaire. Les cellules aug-
mentent leur capacité proliférative et sécrétoire [21]. La
matrice extracellulaire se transforme. Les fibres d’élastine
s’altèrent et se fragmentent sous l’effet d’une augmentation
de l’activité élastasique. La quantité de collagène aug-
mente, aboutissant à une diminution du rapport
élastine/collagène. Des calcifications apparaissent. Le
collagène subit des modifications, des ponts inter-brins
(cross-linking) s’établissent. La moindre sensibilité du col-
lagène ponté à l’action des collagénases compromet sa
dégradation et son renouvellement. La prédominance de
ce collagène ponté dans les parois vasculaires, avec la
calcification, sous-tend les phénomènes de fibrose et de
perte d’élasticité artérielle [17].
Les phénomènes de glycation jouent un rôle essentiel à
ce niveau [22]. Les produits finaux de glycation (AGEs
pour Advanced Glycation Endproducts) sont issus de
liaison entre un aldose tel que le glucose, le galactose ou
le fructose et la fonction amine libre (lysine, arginine)
d’une protéine ou lipoprotéine. Les AGEs s’accumulent
avec l’âge dans la paroi artérielle. Ils sont directement
responsables d’une désorganisation de l’assemblage des
protéines matricielles et du pontage des protéines, en
particulier du collagène. De plus, les AGEs empêche-
raient, par un phénomène de « quenching », l’action du
NO qui est considéré comme jouant un rôle de frein au
développement de l’athérosclérose. D’autre part, les AGEs
peuvent interagir avec des récepteurs membranaires dont
le mieux caractérisé est appelé RAGE. Au niveau de
l’endothélium vasculaire, l’interaction AGEs-RAGE
contribuerait à l’augmentation de la perméabilité endo-
théliale et de l’expression de la molécule d’adhérence
vasculaire VCAM-1, ce qui favorise l’adhérence à la paroi
vasculaire des monocytes macrophages contribuant au
développant des lésions d’athérome. La participation des
AGEs au phénomène de perte d’élasticité des tissus artériel
et cardiaque a été établie par plusieurs études chez l’ani-
mal [23] ou chez l’homme [24] montrant l’effet protecteur
de l’aminoguanidine, qui inhibe la synthèse des AGEs et
de ALT 711, agent pharmacologique pouvant rompre les
ponts interbrins.
Modifications de fonction
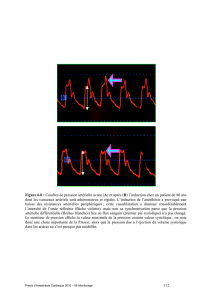
Le vieillissement fonctionnel résulte des modifications
de structure. De façon schématique, on peut retenir que la
diminution de la compliance artérielle entraîne une élé-
vation de la pression artérielle systolique, une augmenta-
tion de l’onde de pouls et une surcharge en pression du
ventricule gauche avec une augmentation des contraintes
pariétales, à l’origine d’un remodelage concentrique du
ventricule gauche, des anomalies de sa fonction diastoli-
que et d’une augmentation de taille de l’oreillette gauche
(figure 2).
Perte de compliance des artères élastiques
L’épaississement de la paroi s’accompagne d’une ré-
duction de la lumière vasculaire et d’une diminution de la
distensibilité et de la compliance artérielle. L’augmenta-
tion de la vitesse de pouls qui lui est associée peut être
mesurée chez l’homme ce qui permet d’évaluer de façon
non invasive la rigidité artérielle [25]. Une telle augmen-
tation avec l’âge de la rigidité artérielle a été observée
dans des populations développant peu d’athérosclérose
de sorte que ce phénomène est bien indépendant de la
mt cardio, vol. 1, n° 1, janvier-février 2005 59
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

maladie athéromateuse [26]. Cependant plusieurs études
épidémiologiques ont montré aussi qu’une augmentation
de la rigidité artérielle survient aussi au cours du diabète et
de l’athérosclérose [27, 28]. L’explication peut être que la
rigidité artérielle ne dépend pas seulement des modifica-
tions de la matrice extracellulaire mais aussi d’autres
facteurs liés à la structure et à la fonction de la paroi
artérielle. On pense en premier lieu à la régulation de la
vasomotricité artérielle par l’endothélium dont on sait
qu’elle est précocement altérée dans le diabète et la
maladie athéroscléreuse [29] mais aussi qu’elle s’altère
avec l’âge [30-32]. Il y a donc un cercle vicieux qui
s’établit entre l’altération des propriétés mécaniques de la
paroi artérielle, le développement de l’athérosclérose, la
dysfonction endothéliale, qui elle-même favorise la perte
de la compliance artérielle.
Augmentation de la post-charge
La post-charge dépend des résistances vasculaires pé-
riphériques, de l’impédance aortique et de la vitesse de
l’onde de pouls. Avec l’âge, l’impédance aortique aug-
mente de même que la vitesse de l’onde pouls, de sorte
que l’onde de pression est renvoyée plus rapidement
depuis les sites périphériques vers le cœur. Chez les
personnes âgées en bonne santé, la courbe de pression
dans la racine aortique atteint son maximum plus tard
dans la systole que chez le sujet jeune. L’augmentation de
la rigidité des artères et de la vitesse de l’onde de pouls et
la modification de la courbe de pression systolique contri-
buent à l’augmentation de la PA systolique chez le sujet
âgé.
Augmentation de la pression artérielle systolique
L’étude de Framingham a confirmé que la pression
artérielle systolique augmentait avec l’âge, tandis que la
pression diastolique qui s’élève jusque vers 50 ans, dimi-
nue au-delà [33]. Il en résulte une augmentation de la
pression pulsée. L’augmentation de la rigidité artérielle
précède l’hypertension artérielle. En retour l’hypertension
artérielle systolique contribue à l’épaississement de paroi
et à la rigidité artérielle. En conséquence, l’hypertension
artérielle de la personne âgée est le plus souvent systoli-
que pure. Plusieurs études récentes ont montré que la
pression pulsée était un facteur de risque puissant et
indépendant d’événements cardiovasculaires chez le su-
jet âgé [34, 35].
Vieillissement cardiaque
Modifications structurales
Des études transversales de sujets non hypertendus et
sans maladie cardiovasculaire cliniquement apparente
ont montré une augmentation de l’épaisseur de la paroi du
ventricule gauche avec l’âge, mesurée par échocardiogra-
phie [36]. Cette hypertrophie intéresse surtout le septum.
Elle constitue un processus compensatoire d’adaptation à
l’élévation tensionnelle et à la réduction des compliances
artérielles.
Des études chez l’animal et des études autopsiques
chez des patients sans maladie cardiovasculaire appa-
rente ont montré que le vieillissement était associé à une
hypertrophie des myocytes et une diminution du nombre
de myocytes [37, 38]. L’hypertrophie myocytaire com-
↑ Rigidité artérielle
↑ Vitesse de l’onde de pouls
↑ Impédance aortique
↑ post-charge
Hypertrophie ventriculaire gauche Prolongation de la contraction
↑ Taille de l’oreillette Maintien de la fraction d’éjection ↓ Remplissage VG
protodiastolique
↑ contribution atriale
au remplissage
↑ Pression artérielle systolique
Figure 2.Schéma représentant de façon simplifiée la dynamique des modifications du système cardiovasculaire avec l’âge en dehors de toute
pathologie cardiaque.
Revue
mt cardio, vol. 1, n° 1, janvier-février 2005
60
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

pense la perte cellulaire mais elle répond aussi à l’aug-
mentation de l’impédance aortique car elle est très asymé-
trique et prédomine dans le ventricule gauche.
Cependant, les myocytes cardiaques sont probablement
capables d’effectuer encore un cycle cellulaire et de pro-
liférer, compensant ainsi en partie la perte cellulaire liée à
l’apoptose et la nécrose. Une augmentation du taux et une
modification des propriétés physiques du collagène (pon-
tages), des dépôts de lipofuschine et de substance amy-
loïde ont aussi été observés dans les myocardes de sujets
âgés [37]. Des altérations des myofibrilles ont été rappor-
tées à l’âge comme une réduction de la forme alpha-
myocardique de l’actine au profit de la forme alpha-
squelettique et une réduction de l’isoforme VI de la
myosine au profit de l’isoforme V3. L’ensemble de ces
modifications concourt à une augmentation de la rigidité
myocardique.
Les valves sont le siège d’une involution fibreuse et de
calcifications qui altèrent leur jeu, gênant le remplissage
des cavités cardiaques et créant des souffles.
Le tissu nodal dans son ensemble est le siège d’une
fibrose collagène, d’une infiltration graisseuse et de calci-
fications. Le nœud sinusal s’appauvrit en cellules P, pace-
makers. Ces modifications favorisent le dysfonctionne-
ment sinusal, les troubles du rythme et de la conduction et
la toxicité des anti-arythmiques.
Modifications fonctionnelles
Le débit cardiaque au repos indexé ou non est in-
changé chez le sujet, de même que chacun de ses deux
composants : le volume éjecté et la fréquence cardiaque.
Deux paramètres sont modifiés au repos : la post-charge et
le remplissage diastolique. Des mécanismes compensa-
teurs interviennent qui sont l’hypertrophie myocardique et
l’augmentation de la contribution atriale au remplissage.
Le cœur âgé sain peut également adapter son débit lors
d’un effort mais cette adaptation se fait moins par la
fréquence que par la mise en jeu de la loi de Starling,
c’est-à-dire par une augmentation des volumes systoliques
et télédiastoliques.
Fonction contractile du myocarde
La contractilité myocardique implique l’activation par
le Ca
++
des myofilaments (couplage excitation-
contraction). Les effets de l’âge sur ce phénomène ont été
étudiés sur des modèles animaux [39]. Les études sur le
muscle papillaire isolé de rat âgé entre 6 et 24 mois ont
montré que la fonction contractile ne variait pas avec
l’âge. En revanche, les durées de la contraction et surtout
de la relaxation sont augmentées dans le muscle cardia-
que sénescent. La cause en est probablement un ralentis-
sement du cycle cellulaire du calcium. Le Ca
++
est éliminé
plus lentement du myoplasme pendant la diastole. Le
potentiel d’action du myocyte âgé est allongé, du fait des
altérations des courants ioniques [40]. Mais le rôle de
cette modification dans l’allongement de la contraction
n’est pas clair. Il s’agit probablement d’un processus
d’adaptation qui permet au muscle de maintenir une
tension active normale aux dépens de la vitesse à laquelle
cette tension se développe.
Fonction diastolique ventriculaire gauche
La fonction diastolique est dépendante des propriétés
élastiques passives du ventricule gauche et du processus
de relaxation active qui sont altérés avec l’âge. Le remplis-
sage protodiastolique du ventricule gauche se réduit pro-
gressivement dès l’âge de 20 ans [41-43]. À 80 ans, il est
diminué de moitié. Dans une étude allemande concernant
1 274 hommes ou femmes âgés de 27 à 75 ans, 2,3 % de
la population a une fraction d’éjection ventriculaire gau-
che inférieure à 45 % [44]. Parmi les autres, 11,1 %
avaient une dysfonction diastolique (critères européens).
La prévalence de la dysfonction diastolique augmentait
avec l’âge passant de 2,8 % dans la tranche d’âge 25-
35 ans à 15,8 % dans la tranche d’âge plus de 65 ans. Ces
changements sont attribués aux modifications de structure
de la paroi ventriculaire gauche et/ou à une activation
résiduelle des myofilaments depuis la systole précédente,
ce qui provoque une relaxation isovolumique prolongée
[41-43]. Le défaut de remplissage protodiastolique est
compensé par une augmentation du remplissage télédias-
tolique liée à la contraction auriculaire. Cela se traduit sur
l’écho-Doppler transmitral par une augmentation de
l’onde A et une diminution de l’onde E. Le remplissage
ventriculaire gauche du sujet âgé est donc très dépendant
de la contraction auriculaire. La perte de contraction
auriculaire en cas de fibrillation auriculaire peut entraîner
une décompensation cardiaque d’autant que la fonction
ventriculaire est atteinte pour d’autres raisons et que la
fréquence ventriculaire est élevée.
En dépit des modifications du remplissage ventricu-
laire gauche, chez les personnes âgées saines, le volume
ventriculaire gauche télédiastolique rapporté à la surface
corporelle en position couché est conservé et non différent
de l’adulte jeune (EDVI) [45, 46]. En revanche, les répon-
ses volumiques cardiaques aux manœuvres posturales et à
l’effort sont modifiées. Le passage de la position couchée à
la position assise réduit l’EDVI chez les sujets jeunes plus
que chez les sujets âgés sains [45, 46]. Durant un court
effort sous-maximal en position assise sur cycle l’EDVI
augmente pareillement à tous les âges. Mais durant un
effort maximal, l’EDVI s’abaisse à son niveau de repos en
position assise chez le sujet jeune tandis qu’il reste élevé
chez le sujet âgé.
Fonction systolique ventriculaire gauche
La fonction systolique du cœur âgé au repos n’est pas
modifiée [47]. La fraction d’éjection ventriculaire gauche
qui est le paramètre le plus souvent utilisé pour mesurer la
fonction systolique ventriculaire gauche ne décline pas
avec l’âge. La valeur moyenne de la fraction d’éjection est
de 65 % et très peu de sujets âgés sains, sélectionnés pour
mt cardio, vol. 1, n° 1, janvier-février 2005 61
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
1
/
8
100%