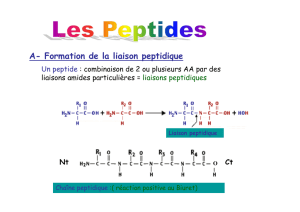
Projet de thèse : Biosynthèse et Régulation de l`Expression de

Projet de thèse :
Biosynthèse et Régulation de l’Expression des cyclolipopeptides de
Acronyme : BREx6
Établissements porteurs
du projet
Ecole Doctorale : ED SML
Directeur de thèse :
Alexis Bazire
Co-encadrant
Benjamin Brillet (LBCM
Résumé du projet :
L
e foisonnement de bactéries multi
thérapeutiques acculant l
es praticiens hospitaliers
colistine.
Nous avons caractérisé une famille originale de
bactérie marine du genre
Pseudoalteromonas
activité bactéricide puissante sur les bactéries à Gram négatif.
hydrocarbonée liée à un
cycle peptidique
dont 5 exotiques, l’acide diaminobutyrique (Dab), la déhydrobutyrine (Dhb) et 3 acides
diaminobutyrique (
HO-Dab)
uniquement décris dans les CLP de
putatif de biosynthèse
des CLP a été identifié
enzymes de type Non Ribosomal Peptide Synthetase
de biosynthèse des monomères exotiques, le transport membranaire ou la régulation de la
production. Le
s objectifs de ce proje
NRPS impliquées
dans la biosynthèse des CLP,
biosynthèse des
HO-Dab, (iii)
élucider
dépendante
de CLP et enfin (iv) établir
des bactéries marines.
Ce projet comporte à la fois un intérêt fondamental (biosynthèse de peptides
non ribosomiaux et d’acides aminés exotique
(nouveaux antibiotiques et
monomères
Contexte du projet
La souche
Pseudoalteromonas
Crassostrea gigas,
pour des activité
cyclolipopeptides
(CLPs) présentant des activités antibactériennes puissantes (Brevet
WO2014187993). Ces CLPs présentent une structure originale composée d’un cycle peptidique
cationique contenant 5 résidus exotiques lié à une chaine hydrocarbonnée variant en longueur,
hyd
roxylation et insaturation en position 3’ (Figure 1). La caractérisation du mécanisme d’action a
montré qu’ils agissent par perméabilisation membranaire après interaction avec le
lipopolysaccharide (LPS
) de la membrane externe
bactéries cibles.
Figure 1
: Structure chimique des cyclolipopeptides (CLP) de
Pseudoalteromonas hCg-6
1
Biosynthèse et Régulation de l’Expression des cyclolipopeptides de
Pseudoalteromonas
du projet
: Université de Bretagne Occidentale
Université de Bretagne Sud
Financement CDE
(50% UBO et 50% UBS)
Alexis Bazire
(LBCM, UBS)
Benjamin Brillet (LBCM
, UBO)
e foisonnement de bactéries multi
-résistantes aux antibiotiques
entraine
es praticiens hospitaliers
à ressusciter d’anciens antibiotiques
Nous avons caractérisé une famille originale de
cyclolipopeptides (CLP)
Pseudoalteromonas
(Brevet WO2014187993). Ces
activité bactéricide puissante sur les bactéries à Gram négatif.
Ils diffèrent par la nature de la chaine
cycle peptidique
identique. Ce
dernier contient 7 résidus d’acides aminés
dont 5 exotiques, l’acide diaminobutyrique (Dab), la déhydrobutyrine (Dhb) et 3 acides
uniquement décris dans les CLP de
Pseudoalteromonas
des CLP a été identifié
, par analyse bioinformatique,
inclu
enzymes de type Non Ribosomal Peptide Synthetase
(NRPS) et des protéines impliquées dans la voie
de biosynthèse des monomères exotiques, le transport membranaire ou la régulation de la
s objectifs de ce proje
t sont de (i) valider et conduire
la dissection moléculaire des
dans la biosynthèse des CLP,
(ii) caractériser l
es enzymes responsables de la
élucider
d
es mécanismes de régulation de la production
de CLP et enfin (iv) établir
la prévalence de ces résidus exotiques
dans les métabolomes
Ce projet comporte à la fois un intérêt fondamental (biosynthèse de peptides
non ribosomiaux et d’acides aminés exotique
s
) et des potentialités d’applications importantes
monomères
non-usuels).
Pseudoalteromonas
hCg-6
a été isolée d’hémolymphe d
pour des activité
s antibactériennes. Elle
produit une nouvelle famille de
(CLPs) présentant des activités antibactériennes puissantes (Brevet
WO2014187993). Ces CLPs présentent une structure originale composée d’un cycle peptidique
cationique contenant 5 résidus exotiques lié à une chaine hydrocarbonnée variant en longueur,
roxylation et insaturation en position 3’ (Figure 1). La caractérisation du mécanisme d’action a
montré qu’ils agissent par perméabilisation membranaire après interaction avec le
) de la membrane externe
des bactéries sensibles et ab
outissent à
: Structure chimique des cyclolipopeptides (CLP) de
Pseudoalteromonas
hCg-6
(50% UBO et 50% UBS)
entraine
des impasses
à ressusciter d’anciens antibiotiques
tels que la
cyclolipopeptides (CLP)
produite par une
(Brevet WO2014187993). Ces
CLP exercent une
Ils diffèrent par la nature de la chaine
dernier contient 7 résidus d’acides aminés
dont 5 exotiques, l’acide diaminobutyrique (Dab), la déhydrobutyrine (Dhb) et 3 acides
hydroxy
Pseudoalteromonas
. Un système
inclu
ant deux méga-
(NRPS) et des protéines impliquées dans la voie
de biosynthèse des monomères exotiques, le transport membranaire ou la régulation de la
la dissection moléculaire des
2
es enzymes responsables de la
es mécanismes de régulation de la production
température-
dans les métabolomes
Ce projet comporte à la fois un intérêt fondamental (biosynthèse de peptides
) et des potentialités d’applications importantes
a été isolée d’hémolymphe d
e l’huitre creuse,
produit une nouvelle famille de
(CLPs) présentant des activités antibactériennes puissantes (Brevet
WO2014187993). Ces CLPs présentent une structure originale composée d’un cycle peptidique
cationique contenant 5 résidus exotiques lié à une chaine hydrocarbonnée variant en longueur,
roxylation et insaturation en position 3’ (Figure 1). La caractérisation du mécanisme d’action a
montré qu’ils agissent par perméabilisation membranaire après interaction avec le
outissent à
la lyse des

Nous avons réalisé le séquençage du génome de la souche h
appelé Cluster 5, a été identifié
anti-SMASH1,2
. Il contient 36 Coding DNA Sequences (CDS) dont deux
Non Ribosomal Peptide Synthetases (NRPS) (Figure 2).
Figure 2 : Structure du
cluster 5 identifié
comme impliqué dans
la biosynthèse des
CLPs (A) et structure
des 2 NRPS (B).
L’analyse bioinformatique
l’heptapeptide est Dab1-Thr2-
Dab
configuration (L
), (iii) le premier domaine d’adénylation présente une séquence caractéristique dite
start
qui indique la liaison d’un acide gras et (iv) le domaine de condensation du module 3 présente
une séquence « modified AA
» qui suggère la déshydratation de la T
sont pas prédites en position 6 et 7 car non recensées dans les bases de données. Le module 7
assurerait la cyclisation de l’heptapeptide. Par conséquent, les prédictions sont en adéquation avec la
structure des CLP.
Les CDS
situées en amont et en aval des 2 NRPS ont été également analysées pour définir
les enzymes impliquées dans la biosynthèse des monomères exotiques composant les CLPs. Les
analyses bioinformatiques montrent que
-
la Dhb proviendrait de la deshydratation
- l
es CDS a2042 et a2045 situées en amont des NRPS dans le cluster de gènes n°5 codent des
protéines présentant des homologies de séquences importantes avec les enzymes impliquées dans la
biosynthèse de Dab (Figure 3).
-
les CDS a2043 et a2044 montrent des homologies de séquences avec des hydroxylases.
Figure 3 : CDS a2042 –
a2045 dans
le cluster 5.
La recherche de synténie avec les CDS a2043, a2044 et a2045 dans la base de données
MAGE a révélé l’existence d’un système homologue chez
analyse plus approfondie du cluster de CDS de
présence d’un système NRPS associé qui génèrerait d’après nos analyses un tripeptide
Dab2-Ala3
. Ces résultats renforcent l’hypothèse d’une implication de la CDS a2043 dans
l’hydroxylation de la Dab préalable à son incorporation dans l
2
Nous avons réalisé le séquençage du génome de la souche h
Cg-6.
Un groupe de gènes,
appelé Cluster 5, a été identifié
dans le chromosome 1 de la souche hCg
6 à l’aide de la plateforme
. Il contient 36 Coding DNA Sequences (CDS) dont deux
codant potentiellement des
Non Ribosomal Peptide Synthetases (NRPS) (Figure 2).
L’analyse bioinformatique
2
des 2 NRPS putatives montre que (i) la séquence de
Dab
3-Leu4-Arg5-X6-X7
, (ii) les acides aminés incorporés sont de
), (iii) le premier domaine d’adénylation présente une séquence caractéristique dite
qui indique la liaison d’un acide gras et (iv) le domaine de condensation du module 3 présente
» qui suggère la déshydratation de la T
hr2
en Dhb
sont pas prédites en position 6 et 7 car non recensées dans les bases de données. Le module 7
assurerait la cyclisation de l’heptapeptide. Par conséquent, les prédictions sont en adéquation avec la
situées en amont et en aval des 2 NRPS ont été également analysées pour définir
les enzymes impliquées dans la biosynthèse des monomères exotiques composant les CLPs. Les
analyses bioinformatiques montrent que
:
la Dhb proviendrait de la deshydratation
d’une (L)-
thréonine par le module 3 de la NRPS 1,
es CDS a2042 et a2045 situées en amont des NRPS dans le cluster de gènes n°5 codent des
protéines présentant des homologies de séquences importantes avec les enzymes impliquées dans la
les CDS a2043 et a2044 montrent des homologies de séquences avec des hydroxylases.
a2045 dans
La recherche de synténie avec les CDS a2043, a2044 et a2045 dans la base de données
MAGE a révélé l’existence d’un système homologue chez
Photorhabdus luminescens
analyse plus approfondie du cluster de CDS de
Photorhabdus luminescens
présence d’un système NRPS associé qui génèrerait d’après nos analyses un tripeptide
. Ces résultats renforcent l’hypothèse d’une implication de la CDS a2043 dans
l’hydroxylation de la Dab préalable à son incorporation dans l
a chaîne peptidique.
Un groupe de gènes,
6 à l’aide de la plateforme
codant potentiellement des
des 2 NRPS putatives montre que (i) la séquence de
, (ii) les acides aminés incorporés sont de
), (iii) le premier domaine d’adénylation présente une séquence caractéristique dite
qui indique la liaison d’un acide gras et (iv) le domaine de condensation du module 3 présente
en Dhb
2. Les
HO-Dab ne
sont pas prédites en position 6 et 7 car non recensées dans les bases de données. Le module 7
assurerait la cyclisation de l’heptapeptide. Par conséquent, les prédictions sont en adéquation avec la
situées en amont et en aval des 2 NRPS ont été également analysées pour définir
les enzymes impliquées dans la biosynthèse des monomères exotiques composant les CLPs. Les
thréonine par le module 3 de la NRPS 1,
es CDS a2042 et a2045 situées en amont des NRPS dans le cluster de gènes n°5 codent des
protéines présentant des homologies de séquences importantes avec les enzymes impliquées dans la
les CDS a2043 et a2044 montrent des homologies de séquences avec des hydroxylases.
La recherche de synténie avec les CDS a2043, a2044 et a2045 dans la base de données
Photorhabdus luminescens
NBA II. Une
Photorhabdus luminescens
NBA II a montré la
présence d’un système NRPS associé qui génèrerait d’après nos analyses un tripeptide
: Lys1-
HO-
. Ces résultats renforcent l’hypothèse d’une implication de la CDS a2043 dans
a chaîne peptidique.

3
Projet de thèse :
Le projet de thèse « Biosynthèse et Régulation de l’Expression des CLP de
Pseudoalteromonas hCg-6 » (BREx6) est consacré à l’analyse des CDS du cluster 5. Il est focalisé sur
l’analyse fonctionnelle des CDS impliquées dans la biosynthèse des CLPs et sa régulation. Il est
articulé en 3 étapes indépendantes qui pourront être menées simultanément.
- (i) dissection moléculaire des 2 NRPS impliquées dans la biosynthèse des CLP :
La dissection fonctionnelle du système NRPS impliqué dans la production des CLP sera
menée par différentes approches moléculaires (CRISPR-Cas9, par exemple). L'identification
fonctionnelle des différents modules sera alors établie, en suivant une stratégie d’expression en
système hétérologue et mesure de l’hydrolyse d’ATP consécutive à l’activation du monomère. Cette
approche combine des techniques de biologie moléculaire, d’enzymologie et de biochimie
analytique. Elle constitue les bases d’un programme d’ingénierie moléculaire des CLP.
- (ii) caractérisation des enzymes responsables de la biosynthèse des
HO-Dab,
Nous proposons de valider les activités Dab-hydroxylases de la protéine codée par la CDS
a2043. La stratégie préconisée va consister à produire cette hydroxylase putative chez E. coli.
Différentes étiquettes seront ajoutées afin de faciliter la purification et la manipulation de la protéine
recombinante. Les conditions d’activité (pH et température optimale) et les paramètres cinétiques
(Km, Vmax) seront définis de manière à sélectionner la construction la plus efficace. L’activité
enzymatique d’hydroxylation de la Dab sera vérifiée par LC-MS.
Cette validation ouvrira des perspectives d’écologies chimiques. En effet, nous
rechercherons des CDS homologues dans les génomes des souches bactériennes disponibles dans les
différentes bases de données telles que GOLD, MBGD… qui cumulent plus ~80 000 génomes. Cette
exploration génomique nous permettra d’accéder à (i) la prévalence des NRPS incorporant des
-OH-
Dab et (ii) la chimio-diversité structurale des peptides non ribosomiaux contenant des
-OH-Dab.
Disposant alors des monomères exotiques
-OH-Dab, la synthèse chimique de ces peptides sera
menée pour explorer et illustrer leur diversité fonctionnelle.
- (iii) élucidation des mécanismes de régulation de la production température-dépendante de CLP :
Les conditions de culture de la souche hCg-6, notamment la température, influencent la
production de CLP. En effet, bien que le taux de croissance optimal de la souche soit observé entre
25 et 30°C, la production de CLP optimale est constatée à 12°C. Des analyses génomiques seront
donc menées pour identifier le(s) système(s) de régulation mis en jeux.
Ce projet ambitieux comporte à la fois un intérêt fondamental (études des peptides non-
ribosomiaux, de leur voie de biosynthèse et de régulation et écologie chimique de bactéries
marines), mais également un important potentiel biotechnologique à différent niveaux :
(i) renouvellement des antibiotiques en médecine humaine ou vétérinaire : le
phénomène de multi-résistance aux antimicrobiens chez les bactéries menace la santé publique.
(prévision de 10 millions de morts/an en 2050). Le développement de nouveaux antibiotiques est
devenu vital. Les CLP de Pseudoalteromonas sont des lipopeptides, une classe de composés utilisée
en antibiothérapie humaine depuis de nombreuses années (colistine) ou très récemment
(Daptomycine).

4
(ii) production enzymatique d’un nouveau monomère pour la synthèse peptidique en
phase solide : la production maîtrisée de nouveaux monomères exotiques tels que la
HO-Dab
comporte un fort potentiel d’application en synthèse peptidique en phase solide. En effet, le marché
florissant des peptides est annoncé à 25.8 milliard $ en 2018 alors qu’il était de 11 milliard $ en 2011.
(iii) exploration métabolomique dirigée : l’utilisation des outils moléculaires définis
dans ce projet (domaine d’adénylation
HO-Dab et
- hydroxylase) va permettre d’accéder à une
nouvelle chimiodiversité et d’explorer les activités biologiques de ces peptides non ribosomiaux
exotiques.
Ces travaux ont été initiés à travers un stage de M2 (financement Stage transverse et
thématique 2017, IUEM), un programme blanc de Biotechnologies (IUEM 2017) et une collaboration
a été établie avec le Dr Y. Li (UMR CNRS-MNHN, Paris). Compte-tenu de l’importance du programme
du projet BREx6, il est probable que nous soyons amenés à privilégier les étapes progressant le plus
rapidement.
Profil du candidat (compétences scientifiques et techniques requises) :
Le candidat devra posséder une formation de niveau M2 ou équivalent en Biochimie,
Biologie moléculaire, Microbiologie ou Biotechnologie. Le bon déroulement du projet implique que le
candidat devra posséder des compétences techniques à la fois en microbiologie (techniques
culturales principalement), en biochimie (techniques de purification de peptides (HPLC notamment)
et d’extraction de biomolécules) et Biologie Moléculaire (PCR, Clonage, ….).
En supplément, le projet impliquant un travail en collaboration avec d’autres sites et unités de
recherche, des qualités d’adaptation, d’autonomie, d’organisation, d’initiative, de curiosité
scientifique, d’esprit de synthèse et de communication à l’oral comme à l’écrit sont recherchées.
Positionnement et environnement scientifique dans le contexte régional, et le cas échéant, national
et international :
Le positionnement du LBCMubo est à l’interface des peptides antimicrobiens et des
bactéries marines. L’environnement scientifique académique et industriel en microbiologie marine
est particulièrement riche dans la région Bretagne. En revanche, peu d’équipes étudient les
lipopeptides antimicrobiens en Bretagne et en France. Nous participons à différentes réseaux dédiés
aux peptides antimicrobiens (GDR CNRS 3625 « Multifonction des Peptides Antimicrobiens », Groupe
Français des Peptides et Protéines, Société françaises des Peptides antimicrobiens et European
Peptide Society). Ce projet est mené en étroite concertation avec la SATT Ouest Valorisation.

5
CV Alexis BAZIRE
Maître de conférences CNU64 à l’Université de Bretagne Sud depuis 2007.
2005 : Doctorat à l’Université de Bretagne Sud sur la régulation et la production des
rhamnolipides chez P. aeruginosa.
2005-2006 : ATER à l’Université de Bretagne Sud sur l’implication du facteur sigma AlgU dans
la formation des biofilms de P. aeruginosa.
2006-2007 : Post-doctorat à l’Université Technique du Danemark sur les transferts de
plasmides au sein des biofilms.
2015 : Habilitation à diriger des recherches.
6 encadrements de thèses (4 soutenues et 2 en cours) dont 2 en collaboration avec des
laboratoires de l’IUEM -(LEMAR, LM2E).
4 supervisions de post-doctorants dont 2 ATER, 6 encadrements de MASTER 2.
Prime d’excellence scientifique 2011-2015 et Prime d’encadrement doctoral et de
recherche 2016-2020.
Directeur des études de L3 Biotechnologies (UBS)
Responsable du cycle préparatoire aux études de médecine (UBS)
Membre élu au conseil de l’UFR sciences de l’UBS et au conseil du département SET.
24 articles dans des journaux internationaux de rang A avec comité de lecture dont les 5
derniers :
1. Rodrigues S., Paillard C., Le Pennec G., Dufour A., Bazire A. Vibrio tapetis, the Causative Agent of
Brown Ring Disease, Forms Biofilms with Spherical Components. 2015. Frontiers in Microbiology 6,
1384 (IF 4)
2. Rosay T., Bazire A., Diaz S., Clamens T., Blier A.S., Mijouin L., Hoffmann B., Sergent J.A.,
Bouffartigues E., Boireau W., Vieillard J., Hulen C., Dufour A., Harmer N.J., Feuilloley M.G.J.,
Lesouhaitier O. 2015. Pseudomonas aeruginosa expresses a functional human natriuretic peptide
receptor ortholog: involvement in biofilm formation. mBio 6, e01033-15 (IF 6.786)
3. Doghri I., Rodrigues S., Bazire A., Dufour A., Akbar D., et al. 2015. Marine bacteria from the French
Atlantic coast displaying high forming-biofilm abilities and different biofilm 3D architectures. BMC
Microbiology, 15, 231 (IF 3.1)
4. Rodrigues S., Paillard C., Dufour A., Bazire A. 2015. Antibiofilm activity of the marine bacterium
Pseudoalteromonas sp. 3J6 against Vibrio tapetis, the causative agent of Brown Ring Disease.
Probiotics and Antimicrobial Proteins 7, 45-51
5. Bazire A. and Dufour A. 2014. The Pseudomonas aeruginosa rhlG and rhlAB genes are inversely
regulated and RhlG is not required for rhamnolipid synthesis. BMC Microbiology 14,160 (IF 3.10)
1
/
5
100%