synapses

Université Dr Moulay Tahar-Saida
Faculté des Sciences&Technologies
Département de Biologie
1. Neurones
2. Transmissions nerveuses
Pr.SLIMANI.M
mslimani20@yahoo.fr

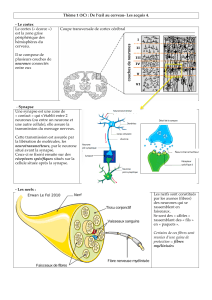
Le neurone
Les cellules nerveuses (neurones) sont les unités fonctionnelles du SNC et
forment un réseau qui s’étend dans tout l’organisme.
le système nerveux possède 10% de neurones pour 90% de cellules gliales .
Ce sont des cellules post-mitotique et excitable. En effet on sait aujourd’hui que
certains neurones peuvent être produits au niveau de l’hippocampe. Leur
excitabilité est due à un changement d’état très rapide qui est déterminé par un
facteur extérieur. Les cellules nerveuses peuvent modifier leur anatomie et
possèdent une grande longévité. Elles sont très sensibles à l’hypoglycémie et à
l’hypoxie. En effet elles consomment presque exclusivement du glucose qui leurs
est fournit par les cellules gliales.
Les neurones sont indépendants les uns des autres, n’établissant que des
contacts fonctionnels spécifiques appelés synapses.
Les neurones étant des cellules post-mitotique, elles ne peuvent pas être source
de tumeur. Ainsi les tumeurs neuronales n’existent pas, mais attention les tumeurs
cérébrales existent (cellules gliales).

•Constitution d’un neurone : véhicule l’information
Dendrites (réception des
signaux)
Corps cellulaires
Cône d’implantation
Axone Gaine de myéline
Nœud de Ranvier
Arborisation terminale
Terminaisons axoniques
(boutons synaptiques)


Le soma ou corps cellulaire
Le noyau contient un grand nucléole riche en chromatine .
Le périkaryon : cytoplasme environnant contient toutes les structures nécessaires pour
la synthèse des protéines, phospholipides et tous les constituants nécessaires au
fonctionnement et au renouvellement du neurone.
•Mitochondries : fournissent l'énergie (métabolisme oxydatif)
•Réticulum endoplasmique
•Ribosomes, polysomes (corps de Nissl en microscopie optique
•Appareil de Golgi : modification post-translationnelle des protéines
•Vésicules synaptiques : synthèse protéique ;Lysosomes
•Neurofilaments (100 Å), microtubules (250 Å) orientent les flux antérograde et
rétrograde: Transport axonal
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
1
/
60
100%