Leishmaniose viscérale : de nouveaux mécanismes impliqués

COMMUNIQUÉ DE PRESSE NATIONAL I PARIS I 16 MAI 2013
Des chercheurs du CNRS, de l’Université Toulouse III - Paul Sabatier et de l’IRD viennent
d’élucider de nouveaux mécanismes moléculaires impliqués dans la résistance à la
leishmaniose viscérale, une grave infection parasitaire. Ils ont montré que les récepteurs
Dectine-1 et Mannose participent à la protection contre le parasite incriminé dans cette
infection, en déclenchant une réponse inflammatoire, tandis que le récepteur DC-SIGN
favorise la pénétration du pathogène et sa prolifération dans les macrophages1. Ces
travaux, réalisés chez la souris et l’homme, ouvrent de nouvelles perspectives pour la
prévention et le traitement de cette maladie. Ils sont publiés le 16 mai 2013 dans la revue
Immunity.
La leishmaniose compte parmi les plus graves infections parasitaires mortelles au monde : 1,5 à 2 millions
de personnes infectées sont recensées chaque année, dont 500 000 cas de leishmaniose viscérale. Cette
maladie chronique constitue un problème de santé publique en Amérique latine, en Asie, en Afrique et
plus récemment dans le sud de l’Europe.
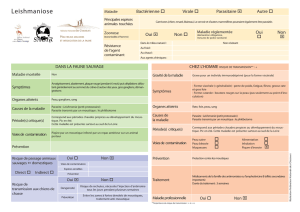
Leishmania, le parasite responsable de l’infection se réfugie et prolifère dans les macrophages. Dectine-1,
Mannose et DC-SIGN sont trois récepteurs de la famille des lectines de type-C, présents à la surface des
macrophages. Selon leur état de différenciation, ces derniers peuvent contribuer à éliminer le parasite, ou
au contraire favoriser sa prolifération en détournant les mécanismes de défense du macrophage à son
avantage et ainsi provoquer l’infection. Ces cellules représentent donc une cible majeure dans la défense
de l’hôte vis-à-vis du pathogène.
Ces travaux menés par des équipes de recherche du laboratoire Pharmacochimie et pharmacologie pour
le développement (Université Toulouse III - Paul Sabatier/IRD) et de l’Institut de pharmacologie et de
biologie structurale (CNRS/Université Toulouse III - Paul Sabatier), ont d’abord été réalisés chez la souris
puis sur des cellules humaines. Ils montrent que les récepteurs Dectine-1 et Mannose ont un effet
inhibiteur sur le parasite. En effet, ils déclenchent la production de radicaux libres oxygénés2 et de
médiateurs inflammatoires, permettant l’élimination du parasite. Les chercheurs mettent aussi en évidence
1 Un macrophage est une cellule du système immunitaire, localisée dans les tissus pouvant être soumis à des infections ou à une
accumulation de débris à éliminer (foie, poumons, ganglions lymphatiques, rate, etc.), et possédant notamment une fonction de
phagocytose, à savoir la capacité d'ingérer et de détruire des parasites, bactéries, levures, débris cellulaires, etc.
2 Les radicaux libres oxygénés sont des espèces chimiques produites par les macrophages qui ont la propriété de détruire les
pathogènes.
Leishmaniose viscérale : de nouveaux mécanismes
impliqués dans la résistance à l’infection

le rôle inverse du récepteur DC-SIGN qui participe à la phagocytose de Leishmania et favorise sa
prolifération en inhibant l’activité microbicide des macrophages.
Ces résultats, confirmés chez l’homme, montrent également pour la première fois que les lectines de type-
C contrôlent la balance entre les médiateurs lipidiques pro-inflammatoires et anti-inflammatoires,
contribuant à l’orientation de la défense anti-parasitaire.
Cette découverte constitue une avancée pour les maladies infectieuses et pourrait être à l’origine de
nouveaux médicaments.
Bibliographie
Divergent roles for C-type lectin receptors in the modulation of host cell response to Leishmania
infantum. Lefèvre L, Lugo-Villarino G, Meunier E, Valentin A, Olagnier D, Authier H, Duval C, Dardenne
C, Bernad J, Lemesre JL, Auwerx J, Neyrolles O, Pipy B, & A Coste, Immunity, 16 mai 2013
Contacts
Chercheur l Agnès Coste l T 05 61 32 28 12 l agne[email protected]
Presse CNRS l Piu Ornella l T 01 44 96 43 90 l ornella.piu@cnrs-dir.fr
1
/
2
100%