PEC - Free

Différenciation endothéliale et
processus angiogéniques
Pr Philippe NGUYEN
EA3801 et Laboratoire d’Hématologie
Université de Reims
Champagne Ardenne CHU de Reims
EA3801

Cellule endothéliale
Cellules aplaties
(L:100 µm-l:10 µm
Épaisseur :0,3 µm)
disposées en mosaïque
-Corps de Weibel Palade (ME)
- Facteur Willebrand
- PECAM1 (CD31) / VE-Cadhérine (CD144)
- Synthèse de NO (eNOS)
- JAMS/Esélectine/VEGFR2
1 à 6 10 13 cellules
Poids total : 1 kg
Surface : 1 à 7 m2

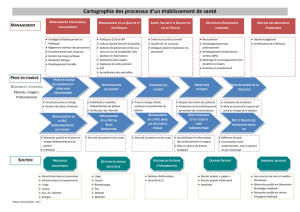
Angiogénèse
ANGIOGENESE POST-EMBRYONNAIRE, NON TUMORALE :
•angiogénèse : prolifération capillaire, favorisant le flux sanguin
•vasculogénèse : à partir de progéniteurs endothéliaux
•artériogénèse : développement des réseaux collatéraux (résistance)
Hypoxie Migration / Prolifération
Différenciation
HIF-1aFacteurs de croissance/Cytokines
VEGF, FGF, IGF…

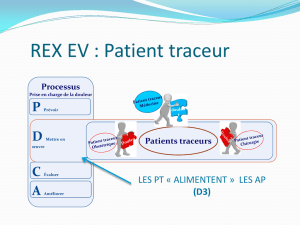
•Cellule progénitrice endothélial :
–endothelial progenitor cell (PEC)
– Différenciation et acquisition d’un phénotype
endothélial à partir d’une cellule souche
hématopoïétique CD34+ [Asahara, 1997]
–Circulating bone marrow-derived endothelium
progenitor cells (CEPCs) [Rafii, 1998] :
•CD34+
•Marqueurs phénotypiques : facteur von
Willebrand, Dil-Ac-LDL.

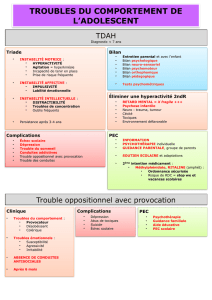
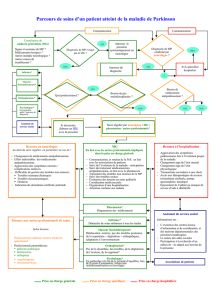
Sang de cordon
1. Isolement des PBMC
3.Tri immuno-magnétique des cellules CD34 positives
2. Élimination des cellules
adhérentes
4.Mise en culture dans des « conditions endothéliales » (VEGF …)
Isolement des cellules CD34+
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
1
/
27
100%