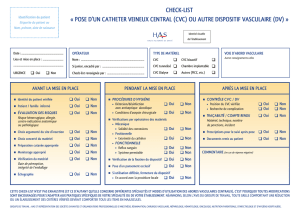
Infections liées aux cathéters veineux centraux

INFECTIONS LIEES AUX
CATHETERS
VEINEUX CENTRAUX
Diagnostic & traitement
A. de LASSENCE - hôpital Louis Mourier

INTRODUCTION
•en hématologie et unité de nutrition parentérale
–cathétérisme de longue durée
•en réanimation
–cathétérisme de courte durée
–concerne environ 69% des patients (EPIIC study)
Vincent JL JAMA 1995; 274:639-644
Tout dépend de quoi on parle
Population (pedia, réa, idp…)
Indication: l'administration de traitements médicamenteux,
produits sanguins, l'alimentation parentérale, le monitorage
hémodynamique, l’abord vasculaire en urgence
Site, matériel (silicone, polyuréthanne..),
Critères diagnostiques

L'infection est la principale complication
des cathéters vasculaires.
Les infections liées aux cathéters
représentent 18 à20% des infections
nosocomiales. (12% - EPIC)
Johnson A and al. J Hosp Infect 1992;20 :67-78
CSQ: mortalité (10-20%), DMS, coùt…
Pittet JAMA 1994; 271: 1560-98

DEFINITION
Présence de micro-organismes à la
surface interne et/ou externe du cathéter
responsables d'une infection locale et/ou
générale
XIIème Conférence de consensus en réanimation et médecine d'urgence, 24 Juin 1994 :
Infections liées aux cathéters veineux centraux en réanimation. Réan Urg 1994, 3 (3 bis): 321-330.
Infections liées aux CVC

PHYSIOPATHOLOGIE
L’infection est précédée par la colonisation de
l’extrémité distale du cathéter par des micro-
organismes.
Infections liées aux CVC
3 VOIES DE CONTAMINATION
Fcutanée
Fendoluminale
Fhématogène
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
1
/
46
100%