Equilibre A.B

Equilibre acido-basique
2. TROUBLES DE L’EQUILIBRE ACIDO-BASIQUE
Thierry PETITCLERC
Biophysique du milieu intérieur
PCEM1 –Université Paris 6
Généralités
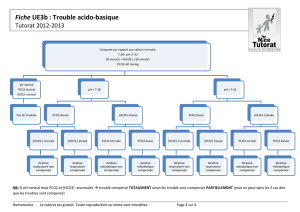
Diagramme de Davenport
Troubles d’origine respiratoire
Troubles d’origine métabolique

Définition : anomalie de la concentration en acides
fixes et/ou volatil :
trouble respiratoire : anomalie de la concentration
[CO2dissous] (= a PCO2) en acide volatil :
-excès (PCO2 > 42 mmHg) : acidose respiratoire
-défaut (PCO2 < 36 mmHg) : alcalose respiratoire
trouble métabolique : anomalie de la concentration en
acides fixes :
- excès : acidose métabolique
-défaut : alcalose métabolique
NB : la conc. en acides fixes n’est pas mesurable. Seule la
variation (excès ou défaut) est mesurable par le laboratoire.
Troubles acido-basiques

acidémie : pH < 7,38 alcalémie : pH > 7,42
trouble pur : l’anomalie de la concentration ne porte que sur une seule
classe d’acides (soit fixes, soit volatil)
trouble compensé : la variation de la concentration d’une classe d’acides
est compensée par une variation dans le sens opposé de l’autre classe.
La compensation est totale si elle permet d’obtenir un pH normal
(compensation partielle sinon).
trouble mixte : les concentrations des deux classes d’acides ont varié dans
le même sens (et aggravent donc leur effet sur le pH).
trouble aigu : début brutal (duré généralement peu de temps)
trouble chronique : dure longtemps (début souvent progressif)
Troubles acido-basiques : définitions

Henderson-Hasselbach :
Diagramme utilisable pour toute solution contenant le tampon
HCO3-/ CO2ouvert.
Le point N (pH normal et bicarbonate normal donc PCO2
normale) représente l'équilibre acido-basique normal. Tous les
autres points correspondent à un trouble de l'équilibre acido-
basique.
Pour se déplacer sur ce diagramme,
il faut faire varier la concentration
des acides fixes et/ou volatils.
+
24
7,40
N
pH
[HCO3-]
mmol/L
Diagramme de Davenport
CO2
3
aP
HCO
log6,1pH

a) Variation isolée de la concentration en acides fixes
sans modification de la concentration [CO2dissous] (= a PCO2) en acide
volatil
Henderson-Hasselbach : [HCO3-] = a PCO2 10pH - 6,1
PCO2 = cste → [HCO3-] = k 10pH - 6,1
+
24
7,40
N
PCO2 = 60 mmHg
PCO2 = 40 mmHg
PCO2 = 30 mmHg
pH
[HCO3-]
mmol/L
D’où une famille de
courbes exponentielles
correspondant à différentes
PCO2 et appelées isobares
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
1
/
20
100%