Cours n°1 : Biomarqueurs dans les maladies du système nerveux

UE2 Histologie
Pr Hugon
Le 05/12/2012 à 10h30
Ronéotypeur : Amine Latreche
Ronéolecteur : Fabrice Labbe
Cours n°1 : Biomarqueurs dans les maladies du système nerveux
Ronéo n°11

SOMMAIRE
I/ La maladie d’Alzheimer
II/Biopathologies
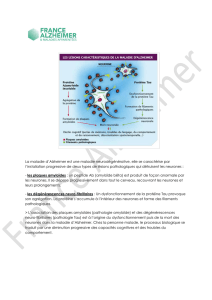
1) Les plaques séniles
2) La dégénérescence neurofibrilla ire
3) L’angiopathie amyloïde
4) La perte neuronale
III/ Biologie de la maladie d’Alzheimer
IV/Biomarqueurs
1) Les plaques séniles
2) L’Apolipoprotéine E
3) Biomarqueurs du liquide Céphalo-Rachidien
V/ Conclusion
Ronéo n°11

Tout d’abord, petite introduction du prof qui nous parle de l’interêt des biomarqueurs
dans le diagnostic de plusieurs pathologies tels que la trisomie 21, l’infarctus du
myocarde, les maladies du muscle,etc…
De notre côté, nous allons étudier la maladie d’Alzheimer et les biomarqueurs qui
ont révolutionné les manières dont on fait les diagnostics et les traitements de cette
maladie.
I/ La maladie d’Alzheimer
En Europe, il y a à peu près un quart de la population actuelle qui est âgée de plus
de 60 ans. On a pu projeter que d’ici 2050, 20 % de la population mondiale (à part
l’Afrique) aura plus de 60 ans, ce qui aura pour conséquence une forte augmentation
des maladies liées au vieillissement (Alzheimer, Parkinson, diabète, cancer,…)
On remarque que l’impact des troubles cognitifs (ici la démence) évolue de manière
croissante en fonction de l’âge, en effet il est quasi nul (5%) avant 60 ans mais un
sujet sur 5 est touché à partir de 85 ans.
Cette prévalence est importante du point de vue de la santé publique, car certaines
maladies liées à l’âge n’ont pas encore de traitement efficace.
Cependant, les anomalies liées à la démence (Alzheimer par exemple) peuvent être
détectées à partir de 50 ans, avant même que la maladie ne se déclare (aucun signe
clinique observé) grâce aux biomarqueurs (qui détectent les anomalies moléculaires
asymptomatiques).
En termes d’épidémiologie, en 2000 l'estimation pour 2005 était de 300 000 cas, en
janvier 2006 il y avait en réalité 850 000 cas de patients déments avec 165 000
nouveaux diagnostics par an.
Les dernières estimations montrent qu’un million de personnes sont touchées par
des maladies de démence avérée en France. Aujourd’hui 15% des déments ont
moins de 65 ans, la maladie d’Alzheimer représentant 70% de ces démences. L’âge
de début tourne autour de 68 ans, et diminue de plus en plus car les diagnostics se
font de plus en plus précocément.
La démence de type maladie d’Alzheimer est un trouble cognitif établi sur un examen
clinique et confirmé par des tests neuropsychologiques ( mémoire, intelligence,
langage,…) où l’on teste les fonctions de notre cerveau. Si deux de ces fonctions ne
sont pas dans les normes, on peut parler de syndrome démentiel. Il faut également
que ces perturbations entraînent des modifications sur les activités de la vie
quotidienne (courses, ménage, répondre au téléphone…).
On remarque une atrophie cérébrale progressive au cours des examens.
Ronéo n°11

Les Américains ont décrit au début des années 2000 un tableau concernant les MCI
(Mind Cognitive Imperment) : ce sont des personnes chez qui l’on note la présence
d’un seul déficit d’une fonction cognitive, et même si cela ne se répercute presque
pas sur leur vie quotidienne, elles peuvent représenter une forme débutante de
maladie d’Alzheimer. Les biomarqueurs ont un rôle important chez ces patients.
On peut classer cette maladie en deux grandes catégories : la forme familiale et la
forme sporadique.
Forme familiale : transmission parents-enfant par mutation hétérozygote d’un gène
codant pour l’APP, PS1 et PS2. Cela concerne 1 à 3% des cas d’Alzheimer avec un
début précoce (vers 30-40 ans). C’est pour cela que lorsque que l’on suspecte un
cas d’Alzheimer précoce, il y a une enquête génétique qui est faite.
Forme sporadique : représente à peu près 97% des cas. Le risque d’avoir la maladie
est lié à l’âge (fréquence augmente avec l’âge), au polymorphisme de l’APO E
(Apolipoprotéine E) et à une douzaine d’autres gènes qui peuvent favoriser les
maladies mais d’une manière certes moindre. Il y a enfin des facteurs liés à
l’environnement avec des facteurs de vulnérabilité (exemple : traumatismes crâniens
chez boxeurs et footballeurs qui font beaucoup de têtes (ZIZOOUUU ‼))
II / Biopathologies
En neuropathologie, on retrouve quatre types de liaisons dans le cerveau :
- Les plaques séniles
- La dégénérescence neurofibrillaire
- L’angiopathie amyloïde
- Les pertes neuronales
Quelque soit la forme de la maladie (sporadique ou familiale), on retrouve la même
histopathologie chez les patients.
1) Les plaques séniles
En coloration argentique, on peut observer la présence d’une couronne et d’une
partie noire. Cette plaque sénile est faite de l’accumulation d’un peptide amyloïde (β)
qui provient de la coupure de l’APP ; c’est une lésion extracellulaire.
2) La dégénérescence neurofibrillaire
Elle est liée à l’accumulation intracellulaire de la protéine tau impliquée dans le
transport avec les microtubules ; la protéine tau est ici hyperphosphorylée.
Ces deux caractéristiques pathologiques sont spécifiques de la maladie d’Alzheimer.
Ronéo n°11

3) L’angiopathie amyloïde
En coloration immunohistochimique, quand on prend un anticorps anti-amyloïde, le
cœur est fait d’une plaque très dense et l’amylose se diffuse tout autour. Il s'agit donc
de l'accumulation de plaques de peptide β dans les vaisseaux. Quand on prend un
anticorps anti-protéine tau, on observe qu’en plus de s’accumuler dans les neurones,
elle vient se loger toute autour de la plaque sénile voire à l’intérieur de la couronne
amyloïde.
4) La perte neuronale
Elle est précédée d’une perte synaptique. La densité synaptique est progressivement
réduite autour des plaques séniles et aussi de façon diffuse. On a alors une
accumulation de dendrites suite à la dégénération de ces derniers. La cause de cette
perte synaptique n’est pas connue (toxicité de la β ?)
La mort neuronale est plus marquée chez les patients, quand on observe au scan un
cerveau on s’aperçoit que 50 à 90% des neurones peuvent avoir disparus. On a une
dégénération de neurones dans l’hippocampe, le noyau de Meynert, le cortex
cérébral,… Seuls les neurones du cervelet restent intacts.
Nous n’avons que peu de connaissance sur le mécanisme et la cause précise de la
mort neuronale.
Les premiers neurones cibles sont les neurones cholinergiques (précocement
atteints), puis les sérotoninergiques, noradrénergiques, somatostatinergiques et
autres.
Ronéo n°11
 6
6
 7
7
 8
8
 9
9
1
/
9
100%