La maladie d`Alzheimer… 100 ans après.

Le 3 novembre 1906, au 37e congrès de la Société des
psychiatres de l’Allemagne de l’Ouest à Tübingen, Aloïs
Alzheimer décrivit les symptômes cliniques et les
caractéristiques neuropathologiques d’une maladie à laquelle
Emil Kraepelin donna le nom de maladie d’Alzheimer. Le
cas présenté était celui d’Auguste D. souffrant de pertes de
mémoire, de psychose et d’hallucinations. L’examen
histologique du cerveau par imprégnation à l’argent selon
Bielschowsky révéla les altérations caractéristiques de la
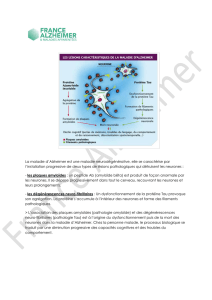
maladie : les plaques séniles et les enchevêtrements
neurofibrillaires. Depuis, et surtout au cours des 25 dernières
années, l’essentiel de la recherche a visé à définir les
composantes majeures de ces altérations et leurs agents
causaux, responsables de la dégénérescence cérébrale. On
compte actuellement plus de 20 millions de cas de maladie
d’Alzheimer dans le monde !
Les enchevêtrements neurofibrillaires résultent de
l’hyperphosphorylation de la protéine tau, associée aux
microtubules. Ils sont aussi présents dans d’autres maladies
neurodégénératives, comme la maladie de Pick. Six
isoformes de la protéine tau sont produits à partir d’un seul
gène, par épissage alternatif de l’ARNm. Ces six isoformes
sont présentes en même proportion dans le cerveau normal et
le cerveau Alzheimer. La relation entre la dysfonction de la
protéine tau et la maladie reste énigmatique. Une piste
possible est la présence de mutations du gène de la protéine
tau dans la démence fronto-temporale et la maladie de
Parkinson héréditaire liée au chromosome 17. En fonction du
type de mutation, la représentation des isoformes peut varier
et toucher les neurones seulement ou les neurones et la glie.
Les plaques séniles sont faites de protéine β-amyloïde. Cette
protéine comporte de 40 à 42 acides aminés et résulte du
clivage d’une protéine précurseur transmembranaire de
fonction encore inconnue, l’APP. Trois enzymes peuvent
cliver la protéine : la β-secrétase du côté N-terminal, la γ-
secrétase du côté C-terminal et l’α-secrétase entre les
positions 16 et 17, initiant la formation de la protéine β-
amyloïde. La forme d’amyloïde à 42 acides aminés est
déposée la première. Les dépôts sont faits de fibrilles
d’amyloïde dans lesquelles la région 1-17 est désordonnée,
tandis que la région 18-42 forme des feuillets β plissés
parallèles. Le lien entre l’APP, l’amyloïde β et le
chromosome 21 a été établi à partir d’observations faites
chez les trisomiques âgés, les patients souffrant
d’amyloïdose de type hollandais, et des cas familiaux
d’Alzheimer. Actuellement une vingtaine de mutations du
gène de l’APP ont été décrites, de même qu’une duplication
du gène. Ces mutations ne concernent qu’une minorité des
cas de maladie d’Alzheimer de type familial. Dans la
majorité des situations, la maladie est associée à des
mutations (plus de 160 identifiées) des gènes des
présénilines 1 et 2 localisés sur le chromosome 14. Les
présénilines sont des protéines membranaires qui
interviennent dans le clivage de l’APP par les γ-secrétases.
Ces mutations favorisent le dépôt de la forme à 42 acides
aminés d’amyloïde.
La plupart des cas de maladie d’Alzheimer sont sporadiques,
les formes héréditaires représentant moins de 1% du total. La
transmission de l’allèle ε4 de l’apolipoprotéine E (apoE4) est
le seul risque génétique actuellement connu d’Alzheimer
sporadique conduisant à un dépôt accru d’amyloïde. La
maladie d’Alzheimer est corrélée à l’âge. Les
enchevêtrements neurofibrillaires apparaissent d’abord dans
le cortex entorhinal, puis envahissent l’hippocampe,
l’amygdale et le néocortex. Les dépôts d’amyloïde
apparaissent ensuite dans le néocortex. Les premières
dégénérescences nerveuses débuteraient 20 à 30 ans avant
l’apparition des premiers symptômes cliniques (les troubles
cognitifs légers ou MCI). Cette longue période
présymptomatique ouvre la perspective de développer des
stratégies préventives qui restent cependant à définir.
En ce qui concerne les approches thérapeutiques, les
inhibiteurs de cholinestérase sont actuellement utilisés pour
combattre les altérations des neurones cholinergiques tandis
que la mémantine réduit la sur-stimulation des récepteurs
NMDA et donc l’excitotoxité. Par ailleurs, plusieurs
substances, actuellement en cours d’essai, visent à réduire les
dépôts d’amyloïde, tel le LY450139, inhibiteur de la γ-
secrétase. Certains anti-inflammatoires non-stéroïdiens, qui
limitent son action font également l’objet d’investigations.
L’immunisation contre la protéine amyloïde β 42 semble
réduire les dépôts dans certaines régions cérébrales…mais
entraîne le développement d’encéphalites méningées. Les
statines semblent aussi diminuer le risque d’Alzheimer.
Enfin, plusieurs substances sont actuellement testées pour
combattre les effets de l’apoE4, l’hyperphosporylation de la
protéine tau ou encore le stress oxydatif. Face à l’éventail
des altérations, une seule voie thérapeutique apparaît
illusoire et un consensus semble se dégager pour envisager
des approches multiples.
Af 447-2006 ©2006 Successful Aging SA
La maladie d’Alzheimer… 100 ans après.
Philippe van den Bosch de Aguilar
Université Catholique de Louvain, Louvain la Neuve
Goedert M, Spillantini MG. A century of Alzheirmer’s disease. Science. 2006;314:777-781.
Robertson ED, Mucke L. 100 years and counting: prospects for defeating Alzheimer’s disease.
Science. 2006;314:781-784.
1
/
1
100%