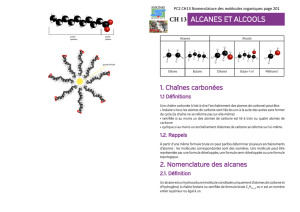
ALCANES ET ALCOOLS

1
ère
S Comprendre 7 : Alcanes et Alcools page 1/3
A
LCANES ET
A
LCOOLS
1 Chaînes carbonées
On appelle squelette carboné ou chaîne carbonée, l'enchaînement des
atomes de carbone d'une molécule liés entre eux par des liaisons covalentes
Lorsque chaque atome de carbone du squelette carboné n'est lié qu’à deux
autres atomes de carbone au plus, on parle de chaîne chaîne linéaire
Lorsqu’au moins un atome de carbone est lié à plus de deux autres atomes de
carbone, on parle de chaîne chaîne ramifiée
Lorsque le squelette carboné se referme sur lui-même, on parle de chaîne
cyclique
2 Alcanes
2.1 Définition
Les alcanes sont des hydrocarbures saturés de formule brute C
n
H
2n+2
où n est
un entier supérieur ou égal à 1
Remarques :
Ils ne contiennent que des liaisons simples, tous les carbones sont tétraédriques.
2.2 Nomenclature
Le nom d'un alcane est constitué d’un préfixe dépendant de l'enchaînement
carboné suivi de la terminaison ane
Alcanes à chaîne linéaire :
Le préfixe d'un alcane à chaîne linéaire est lié au nombre d’atomes de carbone
de la chaîne.
Les quatre premiers préfixes sont des noms consacrés :
méth- (pour 1 carbone) ; éth- (pour 2) ; prop- (pour 3) ; but- (pour 4)
Les autres sont des préfixes numéraux :
pent- (pour 5) ; hex- (pour 6) ; hept- (pour 7) ;
oct- (pour 8) ; non- (pour 9) ; dec- (pour 10).
Ainsi : CH
4
: méthane C
2
H
6
: éthane C
3
H
8
: propane
C
4
H
10
: butane C
5
H
12
: pentane C
6
H
14
: hexane
Groupes alkyles
Le nom d’un groupe alkyle (C
n
H
2n+1
) est constitué du préfixe lié au nombre
d'atomes de carbone suivi de la terminaison yle
ex : CH
3
méthyle
C
2
H
5
éthyle
C
3
H
7
propyle
1
ère
S Comprendre 7 : Alcanes et Alcools page 2/3
Alcanes à chaîne ramifiée
Le nom d’un alcane ramifié est constitué du nom de l’alcane linéaire
correspondant à la chaîne principale (la plus longue)
Devant ce nom, on place dans l’ordre alphabétique le nom des ramifications
alkyles précédées de leurs indices de position
Remarques :
Dans le nom de l’alcane ramifié, le "e" terminal de l’alkyle est supprimé.
La somme des indices de positions doit être la plus petite possible.
Si il y a plusieurs groupes alkyles identiques, on utilise les préfixes : di- (2) ; tri- (3) ;
tétra- (4)
3 Alcools
3.1 Définition
Les alcools possèdent un groupe hydroxyle
OH lié à un carbone
tétraédrique (que des liaisons simples)
La formule générale est : ROH
Remarques :
Comme pour les alcanes, la chaîne carbonée peut être linéaire, ramifiée ou cyclique.
3.2 Nomenclature
Le nom d’un alcool découle du nom de l’alcane correspondant (même
chaîne carbonée) avec les spécificités suivantes :
• la chaîne principale doit contenir le carbone fonctionnel
• le nom se termine par –ol (qui remplace la terminaison "e" de l’alcane)
• cette terminaison est précédée, si nécessaire, de l’ndice de position du
carbone fonctionnel qui doit être plus petit possible
3.3 Classes d’alcool
Les classes d’alcool : La classe d’un alcool est définie par le nombre
d’atomes de carbone lié au carbone fonctionnel.
• Si le carbone fonctionnel est lié à un seul atome de carbone (ou aucun),
l’alcool est primaire
• Si le carbone fonctionnel est lié à deux autres atomes de carbone,
l’alcool est secondaire
• Si le carbone fonctionnel est lié à trois autres atomes de carbone,
l’alcool est tertiaire
carbone fonctionnel
fonction alcool
C
OH

1
ère
S Comprendre 7 : Alcanes et Alcools page 3/3
4 Propriétés physiques des alcanes et des alcools
4.1 Températures de changement d’état
4.1.1 Cas des alcanes linéaires
L’intensité des interactions de Van Der Waals et de ce fait les températures de
fusion et d’ébullition des alcanes linéaires augmentent avec la longueur de la
chaîne carbonée des molécules.
Remarques :
On retrouve ce même résultat pour les alcools
4.1.2 Cas des alcanes ramifiés
Pour des alcanes isomères, la température d’ébullition θ
eb
est d’autant plus
basse que l’isomère est ramifié.
Remarques :
On retrouve ce même résultat pour les alcools
4.1.3 Cas des alcools
Les alcools ont des températures de changement d’état plus élevées que
celles des alcanes correspondant.
Ceci est du à la liaison hydrogène
4.2 Miscibilité avec l’eau
Deux liquides sont miscibles s’ils forment un mélange homogène
Les alcanes sont des molécules insolubles dans l’eau
Les alcools de courte chaîne carbonée sont miscibles avec l’eau.
Lorsque la longueur de la chaîne carbonée d’un alcool augmente, sa
solubilité dans l’eau diminue
La miscibilité avec l’eau des alcools ramifiés est plus grande que celle des
alcools linéaires de même nombre de carbone.
C’est la liaison hydrogène qui permet la solubilité dans l’eau, alors que la chaîne
carboné elle ne l’est pas.
4.3 Distillation fractionnée
La distillation fractionnée est une technique de séparation de liquides
miscibles ayant des températures d’ébullition différentes.
Remarques :
Pour que la séparation puisse se faire il faut que les températures d’ébullition soit
nettement différentes (au moins 15 °C)
Le premier liquide récupéré est le plus volatil (température d’ébullition la plus faible)
Le liquide récupéré après distillation est appelé le distillat, celui qui reste dans le ballon
est appelé le résidu
1
/
2
100%