Lire la suite - Etudiant

FMC 847
LA REVUE DU PRATICIEN MÉDECINE GÉNÉRALE l TOME 29 l N° 952 l DECEMBRE 2015
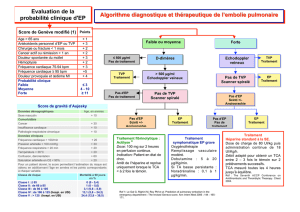
La thrombose veineuse profonde (TVP) et l’embolie pulmo-
naire (EP) sont les principales expressions cliniques de la
maladie thrombo-embolique veineuse (MTEV), affection
fréquente, grave (jusqu’à 25 % de décès en cas d’EP non traitée)
et multifactorielle. Son incidence augmente avec l’âge (jusqu’à
1 %/habitant/an après 75 ans).1 Le traitement anticoagulant
(AC), à dose curative, est à débuter avant même la confirmation
diagnostique en cas de forte probabilité clinique.2 Les AC ont
permis de quasiment faire disparaître les décès par embolie
pulmonaire. Cet article se focalise sur le suivi à moyen et à long
termes après la phase aiguë (premier mois).
PARCOURS DE SOINS
Il n’y a pas de recommandation spécifique.2-4 La gestion de la
MTEV doit être idéalement collégiale, impliquant le médecin
traitant, qui a un rôle de coordinateur des soins, et un spécia-
liste des maladies vasculaires (médecin vasculaire le plus sou-
vent, cardiologue, interniste ou pneumologue si le patient a fait
une EP). Une enquête récente a montré que si les généralistes
connaissent bien la prise en charge globale de la MTEV (utili-
sation quasi systématique d’un AC à posologie curative), près
de la moitié déclarent ne pas adapter la durée du traitement
au type d’atteinte et à la situation clinique.5 Dans la pratique,
plus des deux tiers des MTEV avérées sont soignées de façon
collaborative.5, 6
Une fois la phase aiguë passée, les objectifs du suivi à moyen
et long termes sont :
– éduquer le patient : informations sur la maladie, le risque de
récidive, la prise en charge ;
– réaliser un éventuel bilan étiologique ;
– surveiller le traitement anticoagulant : observance, adaptation
posologique, efficacité (absence de récidive) et tolérance (pas
de complication hémorragique) ;
– déterminer la durée du traitement anticoagulant de la MTEV ;
– dépister les éventuelles séquelles.
Rythme du suivi : une consultation à 1 ou 3 mois puis annuelle
ou plus précoce en cas d’événement intercurrent (complication
hémorragique ou récidive TE, arrêt de l’AC…) ou d’adaptation
thérapeutique : relais héparine-antivitamine K décalé (chez un
patient d’emblée à risque hémorragique ou nécessitant des ex-
plorations invasives initiales, en cas notamment de suspicion de
cancer), adaptation posologique du rivaroxaban à J21, etc.
GESTION DE L’ANTICOAGULATION
Quelle durée optimale ?
C’est un des sujets les plus débattus, notamment en cas de mala-
die idiopathique. La décision doit tenir compte d’une part du
risque de récidive à l’arrêt et d’autre part du risque hémorra-
gique et de la préférence du patient (tableau).
Après une TVP proximale (poplitée ou supra-poplitée) ou une
EP, il est recommandé de traiter au minimum 3 mois ;2-4 en effet,
des durées plus courtes exposent à un sur-risque de récidive
thrombo-embolique à l’arrêt. Cette règle ne s’applique ni en cas
de contre-indication aux anticoagulants (risque hémorragique
principalement) ni à la TVP distale (infra-poplitée, tableau),
DURÉE DE TRAITEMENT ANTICOAGULANT
APRÈS UN ÉPISODE DE MTEV
TVP distale TVP proximale ou EP
1er épisode
avec FF transitoire*
6 semaines AC 3 mois AC
1er épisode
idiopathique ≥ 3 mois AC selon contexte ≥ 6 mois AC (± au long
cours si bonne tolérance)
Facteur de risque
persistant**
≥ 3 mois AC selon contexte ≥ 6 mois AC (prolongé tant
que facteur persiste)
TVP récidivante ≥ 3 mois AC selon contexte Traitement AC prolongé
si récidive idiopathique
Risque hémorragique
élevé,
contre-indication AC
Surveillance clinique
et échographique
Traitement AC ou filtre cave
si extension proximale
Filtre cave, traitement AC
une fois risque
hémorragique/contre-
indication AC levés
AC : traitement anticoagulant à dose curative ; FF : facteur favorisant. * alitement,
chirurgie récente, immobilisation plâtrée ou fracture de membre. ** cancer non guéri,
syndrome des antiphospholipides ou thrombophilie majeure (hors mutation facteur II et V
hétérozygotes).
TABLEAU
Suivi de la maladie veineuse
thrombo-embolique
Coordonné par le MG, il implique idéalement un spécialiste des maladies vasculaires.
Par Jean-Philippe Galanaud, Isabelle Quéré, service de médecine interne et maladies vasculaires, CHU-hôpital Saint-Éloi,
34295 Montpellier Cedex 5. jp-galanaud@chu-montpellier.fr
!847!_MG952_FMC_Galanaud.indd 847 10/12/2015 12:48
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN MEDECINE GENERALE

FMC
848
LA REVUE DU PRATICIEN MÉDECINE GÉNÉRALE l TOME 29 l N° 952 l DECEMBRE 2015
pour laquelle la place des AC et leur posologie restent discutés.
Si une TVP ou une EP survient sous pilule estroprogestative, le
traitement anticoagulant n’est pas habituellement prolongé au-
delà de 6 mois (contraception par DIU au cuivre ou progestative
pure recommandée chez ces patients).
Choix de la molécule
En théorie, elle a déjà été choisie au cours du 1er mois (HBPM,
fondaparinux, AVK, anticoagulant oraux directs [AOD]). Sous
AVK (warfarine, Coumadine ; fluindione, Préviscan ; acénocou-
marol, Sintrom, Minisintrom), si l’INR est bien équilibré (com-
pris entre 2 et 3 ; INR cible = 2,5), il faut le surveiller au moins
1 fois par mois. Si un médicament pouvant interférer avec l’anti-
coagulant (antibiotiques par exemple) est prescrit, les contrôles
doivent être plus rapprochés pour adapter la posologie de l’AVK.
Il n’y a pas lieu de lui substituer un AOD en cas de bon équilibre.
Quatre AOD sont ou seront bientôt disponibles dans la prise en
charge de la MTEV : rivaroxaban, Xarelto ; apixaban, Eliquis ;
dabigatran, Pradaxa ; edoxaban, Lixiana). Seul le Xarelto est
actuellement remboursé dans cette indication.
Le contrôle régulier de l’hémostase n’est pas nécessaire mais il
est impératif de surveiller la fonction rénale (au moins 2 fois/an
si clairance < 60 mL/min).
Quand arrêter ?
La durée prévisionnelle peut évoluer en fonction des résul-
tats du bilan étiologique (lors de la découverte d’un cancer par
exemple, il est prolongé tant que ce dernier n’est pas guéri et
que le rapport bénéfice/risque est favorable), de la tolérance et
de la préférence du patient. Un traitement à long terme doit être
réévalué régulièrement.
En cas de décision d’arrêt, il faut informer le malade des
risques et des signes de récidive (douleur ou œdème unilatéral
de membre en cas de TVP ; dyspnée, douleur thoracique, tachy-
cardie en cas d’EP) et des mesures thromboprophylactiques à
respecter (si hospitalisation, chirurgie, plâtre : avertir le méde-
cin de l’antécédent de MTEV ; lors d’un voyage en avion : bonne
hydratation, déambulation fréquente, compression élastique,
voire anticoagulant préventif).
Le médicament peut être interrompu d’emblée, sans dé-
croissance de doses. À son arrêt, il faut réaliser un écho-doppler
veineux des membres inférieurs chez les patients ayant fait une
TVP, afin de dépister d’éventuelles séquelles thrombotiques
(diagnostic différentiel d’une récidive) ; en cas d’EP, scanner tho-
racique et scintigraphie de référence ne sont pas recommandés
en règle générale, en raison de leur caractère irradiant.
COMPRESSION ÉLASTIQUE
Elle est prescrite pour diminuer l’œdème et la douleur de la TVP
aiguë et éviter la survenue d’un syndrome post-thrombotique
(SPT). Les résultats, débattus, d’un essai récent (étude SOX) ont
remis en cause son utilisation à long terme à visée préventive.
En pratique, au-delà de la phase aiguë, le bénéfice est incer-
tain et, chez les patients ne se plaignant d’aucun signe/symp-
tôme d’insuffisance veineuse et ayant une bonne reperméation
sans reflux à l’écho-doppler, le port d’une compression élastique
pendant 2 ans pour prévenir le SPT ne se justifie plus. Cela ne
concerne que les TVP proximales (manque de données dans la
TVP distale ou après survenue d’un EP sans TVP).
En revanche, en cas d’insuffisance veineuse avérée, primaire
(varices) ou secondaire à la TVP, elle est indispensable (bas ou
chaussettes, classe 3 idéalement ou classe 2 si cela favorise l’ob-
servance) du lever au coucher pour soulager le patient et préve-
nir l’aggravation des symptômes et les complications cutanées :
sclérose cutanée, dermite ocre, ulcère variqueux de jambe.
BILAN ÉTIOLOGIQUE
Si aucun facteur déclenchant n’est retrouvé, ce bilan est utile
pour déterminer (et éradiquer) la cause et adapter éventuelle-
ment l’anticoagulant (durée, type).
Le dépistage des cancers après un épisode de MTEV idiopa-
thique n’est pas encadré par une recommandation spécifique.
En pratique, il faut rechercher à l’interrogatoire des antécédents
personnels et familiaux de MTEV et des facteurs de risque de
cancer et examiner le patient de façon exhaustive (bilan derma-
tologique, toucher pelvien, palpation des aires ganglionnaires).
Outre les tests biologiques standard (hépatique, électrophorèse
des protéines plasmatiques, hémogramme, etc.) sont réalisés une
imagerie thoraco-abdomino-pelvienne (scanner/radio/écho), un
dosage du PSA chez l’homme et un bilan gynécologique (frottis,
mammographie) chez la femme. Les autres examens (colo-
scopie…) ne se justifient qu’en cas de point d’appel clinique.
Le bilan de thrombophilie, à réaliser idéalement à distance
de la phase aiguë, en dehors de tout traitement anticoagulant,
recherche une forme constitutionnelle, fréquente (mutations des
facteurs II et V), ou rare via les dosages de l’antithrombine III,
des protéines C et S, la détection d’un syndrome des antiphos-
pholipides ou SAPL (lupus anticoagulant, anticorps anticardio-
lipines et anti-bêta2-GP1).
Sinus sigmoïde
Veine jugulaire externe
Veine jugulaire interne
Veine thyroïdienne inférieure
Artères pulmonaires
Cœur
Veine cave inférieure
Veines hépatiques
Veine fémorale profonde
Veine fémorale (superficielle)
Tronc tibio-péronier
Veine fibulaire
Veine tibiale antérieure
Veine tibiale postérieure
Veine subclavière
Veine thoracique interne
Veine axillaire
Veine céphalique
Veines brachiales
Veines intercostales
Veine basilique
Veine toraco-épigastrique
Veine céphalique
Veine ulnaire
Veine antébrachiale médiane
Veine épigastrique inférieure
Arcade palmaire profonde
Arcade palmaire superficielle
Veines digitales
Veine cubitale médiane
Veine cave inférieure
Veine poplitée
Creux poplité
Veine iliaque externe
Veine iliaque interne
Veine iliaque commune
Veine fémorale commune
v. gastrocnémiennes
v. soléaires
V. musculaires
V. jambières
v. profondes proximales
et tronc tibio-péronier
v. distales profondes
Fig. 1 – Réseau veineux profond des membres inférieurs.
!847!_MG952_FMC_Galanaud.indd 848 10/12/2015 12:48
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN MEDECINE GENERALE

FMC 849
LA REVUE DU PRATICIEN MÉDECINE GÉNÉRALE l TOME 29 l N° 952 l DECEMBRE 2015
S’assurer de la bonne tolérance du traitement anticoagulant, de son observance.
En fixer la durée : au moins 3 mois en cas de TVP proximale ou d’EP.
Faire le bilan étiologique de la MTEV et dépister ses complications chroniques (récidive,
syndrome post-thrombotique ou cœur pulmonaire chronique post-embolique).
À RETENIR
Liens d’intérêts : JP Galanaud : Bayer HealthCare, Daiichi Sankyo.
I Quéré : Aspen, Bayer HealthCare, Daiichi Sankyo, LEO Pharma, Thuasne.
Il peut être demandé si :
– 1er épisode de TVP proximale ou d’EP idiopathiques chez les
moins de 50 ans ou la femme en âge de procréer ;
– 1er épisode de TVP proximale de site inhabituel (cérébral…) ;
– toute récidive de MTEV dont le 1er épisode est survenu avant
50 ans ;
– TVP distale idiopathique récidivante dont le 1er épisode est
survenu avant 50 ans.
L’étude génétique est interdite chez les mineurs. La découverte
d’une thrombophilie faiblement thrombogène (mutation hété-
rozygote des facteurs II ou V) n’a aucun impact sur la prise en
charge. La découverte d’un SAPL, à confirmer par un 2e dosage à
3 mois, impose le maintien de l’anticoagulation.
DÉPISTAGE DES SÉQUELLES
Syndrome post-thrombotique
C’est le développement d’une insuffisance veineuse secondaire
par destruction valvulaire (mécanisme de reflux) ou obstruction
résiduelle.7 Facteurs de risque : caractère proximal de la TVP
(30 à 40 % des patients font un SPT ; ilio-fémoral > poplité >
sural), antécédent de TVP ipsilatérale, obésité, insuffisance vei-
neuse préexistante.
Le diagnostic est clinique : signes d’insuffisance veineuse sur
un membre ayant été le siège d’une TVP. Afin de le distinguer
d’une TVP aiguë, il est à rechercher à partir de 3 mois après la
thrombose. Il n’existe aucun traitement curatif validé. La pré-
vention après une TVP est donc cruciale : elle repose en premier
lieu sur un traitement anticoagulant bien conduit pendant les
premiers 3 mois ; la compression élastique (au moins force 2, au
mieux force 3) soulage la symptomatologie et prévient les com-
plications graves (ulcère variqueux). Devant un SPT sévère lié
à un syndrome obstructif de localisation ilio-fémorale, on peut
proposer une désobstruction avec angioplastie-stenting.
Cœur pulmonaire chronique
post-embolique
Une HTAP chronique (par opposition à celle de l’EP aiguë) peut
être due à l’obstruction artérielle résiduelle responsable d’une
fibrose vasculaire occlusive.4 Complication rare mais grave de
l’EP (1 à 4 % des patients), ses manifestations cliniques ne sont
pas spécifiques : dyspnée progressive, moindre capacité à l’ef-
fort. L’auscultation cardiopulmonaire est volontiers normale.
Le diagnostic repose sur la mesure d’une PA pulmonaire
moyenne ≥ 25 mmHg, en dehors d’un épisode thrombo-embo-
lique aigu au cathétérisme cardiaque. L’angioscanner thoracique
peut mettre en évidence des thrombi à l’origine d’obstructions
vasculaires partielles ou complètes. L’analyse du parenchyme
pulmonaire permet d’exclure d’autres causes responsables de
la symptomatologie respiratoire. La scintigraphie montre des
défects de perfusion avec ventilation conservée. Ces 2 derniers
examens orientent vers l’étiologie post-embolique de l’HTAP et,
lorsqu’elle est très symptomatique, évaluent l’indication de la
chirurgie (endartériectomie pulmonaire dans un centre expert),
seul traitement curatif (uniquement en cas de thrombi proxi-
maux). Le riociguat (Adempas) est préconisé en cas d’échec ou
d’inaccessibilité de la chirurgie. Compte tenu de la fragilité de
ces patients et du risque élevé d’EP mortelle en cas de récidive,
le maintien de l’anticoagulant au long cours est recommandé.
Diurétiques et oxygénothérapie sont indiqués. Le dépistage par
échographie cardiaque, à partir du 3e mois après l’EP aiguë, est
justifié en cas de suspicion clinique mais peut être proposé de
façon systématique après une EP grave avec dysfonction ventri-
culaire droite initiale. l
RÉFÉRENCES
1. Galanaud JP, Messas E, Blanchet-Deverly A, et al. Management of venous
thromboembolism : a 2015 update. Rev Med Interne 2015;36:746-52.
2. Kearon C, Akl EA, Comerota AJ, et al. Antithrombotic therapy for VTE
disease: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed:
American College of Chest Physicians Evidence-Based Clinical Practice
Guidelines. Chest 2012;141(2 suppl):e419S-94S.
3. Mismetti P, Baud JM, Becker F, et al. [Guidelines for good clinical
practice: prevention and treatment of venous thromboembolism in
medical patients]. J Mal Vasc 2010;35:127-36.
4. Konstantinides S, Torbicki A, Agnelli G, et al. 2014 ESC Guidelines on
the diagnosis and management of acute pulmonary embolism. Eur Heart J
2014;35:3033-69.
5. Almosni J, Meusy A, Frances P, Pontal D, Quéré I, Galanaud JP. Practice
variation in the management of distal deep vein thrombosis in primary vs.
secondary cares: a clinical practice survey. Thromb Res 2015;136:526-30.
6. Ternisien-Payerols A, Meusy A, Terminet A, et al. [Home care for acute
pulmonary embolism: feasibility and general practitioner acceptability].
J Mal Vasc 2015;40:223-30.
7. Galanaud JP, Kahn SR. Postthrombotic syndrome: a 2014 update. Curr
Opin Cardiol 2014;29:514-9.
Fig. 2 – Thrombose veineuse profonde. Examen échographique : la veine
poplitée n'est pas dépressible.
CompressionBasal
!847!_MG952_FMC_Galanaud.indd 849 10/12/2015 12:48
TOUS DROITS RESERVES - LA REVUE DU PRATICIEN MEDECINE GENERALE
1
/
3
100%