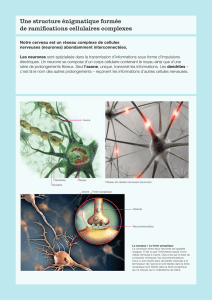
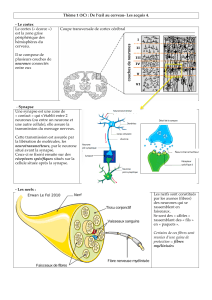
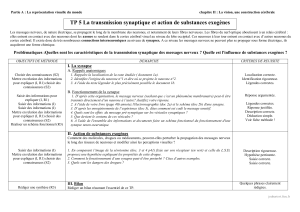
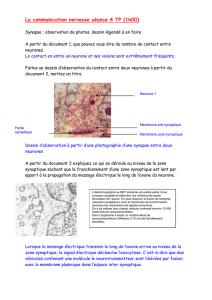
B. Synapse Chimique

Plan
•A Cyto-architecture du neurone
– I. Introduction générale
– II. Organites non spécifiques du neurone
– III. Organites spécifiques des neurones
– IV. Classification des neurones
– V. Les cellules gliales
•
B. Synapse Chimique
•
B. Synapse Chimique
– I. Les différents types de synapses
– II. Ultrastructure et fonctionnement d’une synapse chimique
– III. Synapses cholinergiques
– IV. Synapses glutamatergiques
– V. Synapses Gabaergiques
– VI. Neuropharmacologie
– Lien http://perso.univ-rennes1.fr/francois.tiaho
Dossier NER 2014

I. Introduction générale
• 1. Localisation, nombre et fonction des
neurones
• 2. Configuration en réseau et plasticité
synaptique
synaptique
• 3. Pathologies neuro-dégénératives et
accidents vasculaires cérébraux.
• 4. Les neurones sont des cibles de
psychotropes
•http://perso.univ-rennes1.fr/francois.tiaho
• Dossier: NER2014

1. Localisation, nombre et fonctions
des neurones
• Système nerveux central et périphérique
• 1012 neurones représentant 10% dans le
SNC
SNC
• Fonctions:
– Vie de relation (perception, Motricité)
– Homéostasie du milieu intérieur
– Cognition en générale (Langage, mémoire,
raisonnement etc.)

2. Configuration en réseau et
plasticité synaptique
• Les neurones ne sont pas isolés. Ils
forment des réseaux connectés par des
synapses.
synapses.
• Les connexions synaptiques (1000 par
neurone) sont modifiées au cours des
différents apprentissages
• Régénération très limitée en cas
d’accident ou pathologie dégénérative.

3. Pathologies neuro-dégénératives
et accidents vasculaires cérébraux.
• Les neurones ne se divisent pas.
•
Cancer du cerveau implique: gliomes
•
Cancer du cerveau implique: gliomes
• Nécessité de comprendre les mécanismes
de prolifération, migration, différenciation,
guidage axonal pour pallier aux AVC et
maladies neuro-dégénératives
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
1
/
59
100%