Modalités d`échappement au système immunitaire de l`hôte

Modalités d'échappement au système immunitaire
de l'hôte: exemple de Plasmodium
Catherine BRAUN-BRETON

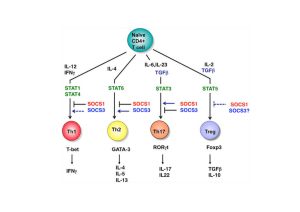
La réponse immunitaire contre Plasmodium
Réponse innée
DCs : rôle central dans la
présentation d’Ag et
l’activation des T
monocytes/macrophages :
présentation d’Ag et
phagocytose y compris sans
opsonisation (clairance,
molécules inflammatoires)
Tγδ : rôle essentiel dans la
clairance des stades sanguins
via cytokines pro-
inflammatoires, augmentation
de l’activation des DCs via un
mécanisme IFNγ dépendant
NK : source importante
précoce d’IFNγ, interaction
avec les DCs
Réponse adaptative
Lymphocytes B et
anticorps : la production
d’Ab spécifiques en qualité,
niveau et largeur est un
élément clé de la réponse
protectrice mais cette
production est lente à se
développer et n’est pas
maintenue de manière
efficace
Immunité à médiation
cellulaire : importance de
l’IFNγ et du TNFα pour la
production de molécules
inflammatoires capables de
tuer le parasite mais une
réponse excessive contribue
à la pathologie. Implication
de T-CD4+, T-CD8+ et
Treg
Lymphocytes T-CD4+
mémoire : elles déclinent
progressivement en absence
d’infection

d’après Urban et al. 1999
Système immunitaire inné et paludisme
Les érythrocytes infectés peuvent se lier à la surface des
érythrocytes sains, des cellules endothéliales, des DCs
et des lymphocytes T via l’adhésine PfEMP1

Système immunitaire inné et paludisme
Composés immunologiquement actifs
- GPI / TLR2
- hémozoïne
* pro- et anti-inflammatoire
* accumulation (macrophages, DCs…)
* pourrait entraîner la paralysie des DCs, état de
tolérance, via TLRs
* délivre ADN du parasite au TLR9 (aussi une
protéine impliquée dans le complexe)
- profilin-like protein/TLR11
mais TLR11 chez souris pas chez l’Homme
- érythrocyte infecté
* liaison des GRP aux macrophages et DCs par
CD36
* peut-être aussi NK (IL18R)
* CD36 récepteur de PfEMP1
Coban et al, TRENDS Microbiol. 2007

 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
1
/
22
100%