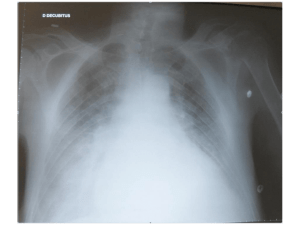
Hypophosphatémie et FGF23 élevé

CAS CLINIQUE
Rhumatos • Mars 2015 • vol. 12 • numéro 105 61
L’hypophosphatémie est
définie par une phos-
phatémie le matin à
jeun inférieure à 0,8mmol/l. Dé-
couverte de manière « fortuite »
sur une analyse de sang ou dans le
cadre d’un bilan d’ostéopathie fra-
gilisante, ses étiologies sont nom-
breuses.
Une anamnèse précise, un examen
physique rigoureux et une analyse
stricte des données biologiques
permettent souvent d’en com-
prendre l’origine et de proposer un
traitement adapté.
Nous rapportons ici une cause rare
d’ostéomalacie hypophosphaté-
mique liée au FGF23.
CAS CLINIQUE
Une patiente de 57 ans est adressée
en mars 2014 dans notre service
pour avis sur une polyarthralgie.
Elle présente comme principaux an-
técédents un asthme, une maladie
de Rendu-Osler compliquée d’une
anémie ferriprive et un déficit im-
munitaire commun variable.
Son traitement comprend salbu-
tamol à la demande, immunoglo-
bulines humaines sous-cutanées
tous les 10 jours (Hizentra®) et
carboxymaltose ferrique injec-
table (Ferinject®) tous les mois.
Les douleurs ont commencé en
2012, progressivement, avec un
rythme mécanique, intéressant le
rachis lombaire puis les hanches,
les genoux et les pieds, sans gon-
flement. Le bilan biologique n’a
pas révélé de syndrome inflam-
matoire ni d’auto-anticorps. La
scintigraphie osseuse a permis
de retrouver une fixation anor-
male des 2 calcanéums et d’un
plateau tibial et l’IRM de la che-
ville montrait un œdème osseux
calcanéen postérieur sans enthé-
sopathie achilléenne. Devant ce
tableau, une spondyloarthrite a
été évoquée. La patiente a alors
été placée sous une faible dose de
prednisone (la maladie de Rendu-
Osler contre-indiquant les AINS)
sans ecacité franche. Devant
l’absence d’amélioration et afin de
conforter le diagnostic, une IRM
des sacro-iliaques et du rachis
lombaire est demandée et a mis
en évidence un œdème osseux de
l’aileron sacré gauche évoquant
une fracture, confirmée au scan-
ner, sans sacro-iliite ou anomalie
rachidienne inflammatoire. À la
densitométrie osseuse, le T-score
était à -1,5 au col et -0,2 au rachis
(chez une patiente ayant une
arthrose lombaire). Devant cette
fracture pathologique, le bilan
d’ostéopathie fragilisante retrou-
vait comme seule anomalie une
hypophosphatémie à 0,42mmol/l
mise sur le compte d’un déficit en
vitamineD (25(OH)D à 15 ng/ml).
La patiente a été supplémentée en
vitamineD et traitée par une perfu-
sion d’acide zolédronique. Malgré
cela, le diagnostic de rhumatisme
inflammatoire a été maintenu et la
prednisone augmentée à 30mg/j.
Les douleurs s’aggravent rapide-
ment et la patiente est alors adres-
sée dans notre service pour avis.
À l’entrée, elle rapporte des dou-
leurs mécaniques des membres
inférieurs et du bassin associées
à des myalgies prédominantes
Hypophosphatémie et FGF23 élevé
Ce n’est pas toujours un diabète
phosphaté oncogénique
n
L’hypophosphatémie est une situation rare mais classique en rhumatologie de l’adulte. À travers
un cas clinique exposant une cause exceptionnelle d’hypophosphatémie liée au fibroblast growth
factor 23 (FGF23), nous décrirons les principes de la démarche diagnostique face à un patient
présentant une phosphatémie basse. Nous soulignerons également la fréquence des erreurs
diagnostiques auxquelles cette anomalie biologique, trop souvent méprisée, peut conduire et
l’importance de demander son dosage et de vérifier sa normalité.
Dr Nicolas Poursac*
*Service de Rhumatologie, CHU Pellegrin, Bordeaux

62 Rhumatos • Mars 2015 • vol. 12 • numéro 105
CAS CLINIQUE
aux cuisses. On note un relevé
myopathique et une marche dou-
loureuse avec bascule latérale
du bassin (marche dandinante).
Le diagnostic d’ostéomalacie est
évoqué. L’analyse des précédents
bilans biologiques retrouve une
hypophosphatémie à 0,40mmol/l
apparue en janvier 2012, alors
qu’elle était normale sur les bilans
de 2011. Le diagnostic de rhuma-
tisme inflammatoire est écarté et
une ostéomalacie d’origine hypo-
phosphatémique est évoquée.
Un premier bilan biologique, afin
de préciser l’origine de l’hypo-
phosphatémie, retrouve:
• créatininémie = 54 μmol/l ;
• clairance CKD-Epi = 101 ml/
min/1,73m2;
• calcémie = 2,28mmol/l ;
• phosphatémie = 0,36mmol/l;
• calciurie/24 h = 2,96mmol ;
• phosphaturie/24 h = 30,9mmol ;
• créatininurie/24 h = 12mmol;
• volume urinaire = 1 850 ml;
• uricémie = 270 μmol/l ;
• HCO3- = 24mmol/l ;
• glycosurie = négative;
• PTH = 80 pg/ml (N: 12-88);
• 25-(OH)-vitamineD = 25ng/ml ;
• 1,25-(OH)-vitamineD = 54,9pg/ml;
• FGF23 = 3 fois la limite supé-
rieure à la normale.
DÉMARCHE
DIAGNOSTIQUE
BIOLOGIQUE
La
figure 1
résume la démarche dia-
gnostique biologique que nous
proposons devant une hypophos-
phatémie en rhumatologie.
Voici son application à notre pa-
tiente:
• 1re étape : préciser l’origine
digestive ou rénale. Clairance
du phosphate = 87 ml/min (N <
15 ml/min), taux de réabsorption
du phosphate (TRP) = 61 % (N >
85 %). Conrmation de l’origine
rénale.
• 2e étape : éliminer un syndrome
de Fanconi. Uricémie normale,
bicarbonates normaux, pas de gly-
cosurie. Pas d’argument pour un
syndrome de Fanconi.
• 3e étape : évaluer le couple
PTH/calcémie. Calcémie = nor-
male, PTH = normale. Il ne s’agit
donc pas d’une hyperparathyroï-
die primaire.
• 4e étape : évaluer la calciurie. La
calciurie est normale chez notre
patiente. Il s’agit donc d’une forme
liée au FGF23.
• 5e étape: dosage du FGF23= 3N.
Notre bilan conclut donc à une hypo-
phosphatémie sur diabète phospha-
té médié par le FGF23. L’absence de
retard de croissance ainsi que l’appa-
rition brutale et tardive permettent
d’éliminer un rachitisme. L’hypo-
thèse d’un diabète phosphaté onco-
génique est donc retenue.
La seconde partie du bilan consiste
alors à rechercher la tumeur res-
ponsable de l’hypersécrétion de
FGF23, entraînant une diminu-
tion de la réabsorption rénale de
phosphate.
D’un point de vue clinique, l’exa-
men a noté des lésions cutanées
évocatrices d’histiocytofibromes
ainsi qu’un nodule sous-cutané
de la cuisse gauche. Une TEP au
18-FDG corps entier ne met pas
en évidence de fixation patholo-
gique. En deuxième intention, une
scintigraphie aux analogues de la
somatostatine ne montre pas non
plus de fixation pathologique. En-
fin, une IRM corps entier est sans
anomalie.
Devant l’absence de tumeur iden-
tifiable au scanner, l’ablation des
lésions cutanées a été proposée,
avec, sur chacune, une recherche
de FGF23. Sept lésions cutanées
Hypophosphatémie
Clairance du phosphate < 15 ml/min
= cause digestive
- Alcoolisme
- Diarrhée chronique
- Anti-acides
- Carence ou résistance à la vitamine D
- Chirurgie duodéno-jéjunale
Clairance du phosphate > 15 ml/min
= cause rénale
Signes de Fanconi ?
- Bicarbonates bas ?
- Uricémie basse ?
- Glycosurie ?
Absence de
signes de Fanconi
Couple
PTH/calcium
adapté
Calciurie des 24 h
diminuée :
- Carence en
vitamine D
- Rachitisme
vitaminorésistant
type 1 ou type 2
Calciurie des 24 h normale
= élévation FGF23
- Diabète phosphaté
oncogénique
- Rachitisme lié à l'X
- Rachitisme
autosomique dominant
ou récessif
- Fer IV
Calciurie des 24 h élevée :
- Rachitisme
hypophosphatémique
hyercalciurique
- Sécrétion de PTHrp
Couple PTH/calcium
inadapté =
hyperparathyroïdie primaire
Syndrome
de Fanconi
Figure 1 - Algorithme diagnostique d’une hypophosphatémie.

HypopHospHatémie et FGF23 élevé
Rhumatos • Mars 2015 • vol. 12 • numéro 105 63
au total ont été enlevées : 6 his-
tiocytofibromes et un lipome.
L’analyse du FGF23 sur pièce s’est
révélée négative et le tableau clini-
co-biologique ne s’est pas amélioré.
Le diagnostic de diabète phos-
phaté a donc été retenu et, en
l’absence d’identification de
l’origine de l’hypersécrétion du
FGF23, un traitement sympto-
matique par phosphore per os et
calcitriol per os a été prescrit, ne
permettant qu’une stabilisation
de la phosphatémie autour de
0,5mmol/l sans amélioration sur
les douleurs.
En février 2015, lors d’une revue
de la littérature sur les hypophos-
phatémies, nous découvrons un
article japonais de 1982 rappor-
tant 9 cas d’hypophosphatémies
induites par du fer injectable (1, 2).
Ceci nous évoquant notre pa-
tiente, nous décidons d’arrêter ses
perfusions de fer injectable. Ce
traitement avait été mis en place
avant 2010 dans le cadre d’une
anémie ferriprive secondaire à sa
maladie de Rendu-Osler. Le trai-
tement initial de la patiente était
du fer per os (hydroxysaccharide
ferrique), puis a été remplacé par
du Ferinject® en janvier 2012.
L’évolution de la phosphatémie est
donnée en
figure 2
.
En mars 2015, à 2 mois de l’arrêt
du Ferinject®, les douleurs ont dis-
paru, la marche s’est totalement
normalisée et le phosphate est re-
monté à 0,9 mmol/l. Le principal
problème reste son anémie ferri-
prive qui, pour le moment, est trai-
tée par transfusions itératives et
pour laquelle nous envisageons la
reprise du fer per or sous surveil-
lance étroite de la phosphatémie.
DISCUSSION
Ce cas clinique soulève plusieurs
points importants.
D’abord, la confusion diagnostique
à laquelle peut parfois conduire
une hypophosphatémie. Eective-
ment, lorsque le tableau n’est pas
aussi franc qu’une ostéomalacie,
l’hypophosphatémie peut entraî-
ner une polyalgie avec un examen
clinique pauvre qui peut parfois,
à tort, faire porter le diagnostic de
fibromyalgie ou de spondyloar-
thrite (3, 4).
Par ailleurs, il nous semble im-
portant de souligner la nécessité
de conduire un interrogatoire et
un examen physique précis ainsi
qu’une analyse stricte du bilan
biologique afin de conclure à 1ou
2hypothèses diagnostiques.
Le diabète phosphaté oncogé-
nique est une cause, mais non la
seule, d’hypophosphatémie asso-
ciée à une élévation du FGF23.
Parmi les autres étiologies, un
rachitisme vitaminorésistant lié
à l’X, autosomique dominant ou
autosomique récessif, doit être
évoqué, même chez l’adulte, sur-
tout devant une petite taille. Ces
rachitismes sont liés à une ano-
malie congénitale du FGF23,
soit un excès de production,
soit une résistance de celui-ci à la
protéolyse (5). Comme cause rare,
il faut également, devant des lé-
sions cutanées évocatrices, penser
à un syndrome du nævus linéaire
sébacé (6).
L’hypophosphatémie induite par
le fer injectable est une cause rare
et probablement sous-diagnosti-
quée d’ostéomalacie. La première
description a été rapportée en 1982
(1). Depuis, une vingtaine de cas
ont été décrits. Au début des an-
nées 1980, avant que le FGF23 ne
soit identifié, Okada et al. consta-
taient que cette hypophospha-
témie était bien d’origine rénale
mais non liée à la PTH puisque
celle-ci ainsi que la calcémie
étaient normales (1). En 1994, Sato
et Shiraki ont montré que le com-
plexe associé au fer jouait un rôle
important: le fer chélaté à la chon-
droïtine sulfate n’entraînait pas
de diminution de la réabsorption
tubulaire du phosphate, contrai-
rement à l’hydroxysaccharide
de fer (7). Ils ont également mis
en évidence une diminution de la
0,3
0,4
0,5
0,6
0,7
0,8
0,9
10/01/11
01/01/12
04/01/12
07/01/12
10/01/12
01/01/13
04/01/13
07/01/13
10/01/13
01/01/14
04/01/14
07/01/14
10/01/14
01/01/15
Phosphatémie
Début Ferinject®
Arrêt Ferinject®
Figure 2 - Évolution de la phosphatémie dans le temps.

64 Rhumatos • Mars 2015 • vol. 12 • numéro 105
CAS CLINIQUE
1-alpha-hydroxylase, responsable
d’une diminution du calcitriol, ré-
versible à l’arrêt des perfusions de
fer. La normalité du calcitriol dans
notre observation pourrait être
liée au fait que son dosage a été ré-
alisé à 4semaines de la perfusion
de fer, juste avant la suivante.
Ces dernières années, la mise en
évidence du FGF23 a permis de
mieux comprendre le métabolisme
du phosphate (5, 8). Cette phos-
phatonine est responsable d’une
inhibition de la 1-alpha-hydroxy-
lase et d’une diminution de la
réabsorption tubulaire du phos-
phate. En 2009, 2équipes ont mis
en évidence l’élévation du FGF23
chez des patients recevant du
fer injectable, expliquant ainsi la
diminution du TRP et la baisse du
calcitriol constatées précédem-
ment (8, 9). Le mécanisme de l’élé-
vation du FGF23 dans ces circons-
tances reste cependant inconnu. n
1. Okada M, Imamura K, Iida M et al. Hypophosphatemia induced by intra-
venous administration of saccharated iron oxide. Klin Wochenschr 1983 ;
61 : 99-102.
2. Okada M, Imamura K, Fuchigami T et al. 2 cases of nonspecific multiple
ulcers of the small intestine associated with osteomalacia caused by long-
term intravenous administration of saccharated ferric oxide. Nihon Naika
Gakkai Zasshi 1982 ; 71 : 1566-72.
3. Jin J, Sun F, Wang G et al. The clinical characteristics of 26 cases of hypo-
phosphatemia osteomalacia misdiagnosed as spondyloarthritis. Zhon-
ghua Nei Ke Za Zhi 2014 ; 53 : 847-51.
4. Xian-Ling W, Jian-Ming B, Wen-Wen Z et al. Osteomalacia caused by tu-
mors in facies cranii mimicking rheumatoid arthritis. Rheumatol Int 2012 ;
32 : 2573-6.
5. Consortium A. Autosomal dominant hypophosphataemic rickets is
associated with mutations in FGF23. Nat Genet 2000 ; 26 : 345-8.
6. Fukumoto S. Diagnostic modalities for FGF23-producing tumors in pa-
tients with tumor-induced osteomalacia. Endocrinol Metab (Seoul) 2014 ;
29 : 136-43.
7. Sato K, Shiraki M. Saccharated ferric oxide-induced osteomalacia in Japan:
iron-induced osteopathy due to nephropathy. Endocr J 1998 ; 45 : 431-9.
8. Schouten BJ, Hunt PJ, Livesey JH et al. FGF23 elevation and hypophos-
phatemia after intravenous iron polymaltose: a prospective study. J Clin
Endocrinol Metab 2009 ; 94 : 2332-7.
9. Shimizu Y, Tada Y, Yamauchi M et al. Hyposphosphatemia induced by
intravenous administration of saccharated ferric oxide: another form of
FGF23-related hypophosphatemia. Bone 2009 ; 45 : 814-6.
BiBliographie
Mots-clés :
Hypophosphatémie, FGF23, Fer
RENDEZ-VOUS DE L’INDUSTRIE
BIOSIMILAIRES
Remsima® : le biosimilaire de
l’infliximab, lancé par Biogaran
Le laboratoire Biogaran a annoncé le lancement
d’un biosimilaire de l’infliximab, Remsima®
100 mg, autorisé par l’EMA en septembre 2013.
C’est un anticorps monoclonal de type IgG1 produit dans des
cellules hybridomes murines par la technique de l’ADN recombi-
nant. Son mécanisme d’action est identique à celui de l’inflixi-
mab d’origine. Remsima® est indiqué dans le traitement :
• des maladies inammatoires (polyarthrite rhumatoïde,
spondyloarthrite ankylosante, rhumatisme psoriasique);
• de la maladie de Crohn de l’adulte et de l’enfant (de 6 à
17ans);
• de la rectocolite hémorragique de l’adulte et de l’enfant (de
6à 17ans);
• du psoriasis en plaques.
Ce biosimilaire est développé en partenariat avec le laboratoire
coréen Celltrion. Remsima® est déjà prescrit dans 12pays.
Les biosimilaires offrent les mêmes garanties de qua-
lité, d’efficacité, et de sécurité que les médicaments bio-
logiques d’origine, mais à moindre coût, permettant ainsi
de favoriser l’accès de certains patients à des thérapies
innovantes coûteuses.
La projection d’économies grâce aux biosimilaires pour
les systèmes de santé en Europe est évaluée entre 11 et
33 milliards d’euros avec des économies majeures pour la
France, l’Allemagne et l’Angleterre. n
Pour en savoir plus: www.biogaran.fr et www.celltrion.com
ACTIVITÉ PHYSIQUE
Promouvoir la reprise du sport chez les
sédentaires et les malades chroniques
La Fédération française
Sport pour Tous a lancé
la charte "Club sport santé
bien-être", avec le soutien
de Pierre Fabre Médicament. Dans les clubs et associa-
tions sportives qui souhaitent adhérer, la charte met en
place 10engagements afin de développer des programmes
sportifs adaptés aux personnes sédentaires ou ayant des
maladies chroniques, notamment grâce à des éducateurs
sportifs diplômés, des conseils spécifiques et des tarifs
accessibles à tous. L’objectif est de promouvoir la reprise
d’une activité sportive, l’inactivité physique étant respon-
sable de 10 % des décès en Europe d’après l’OMS. n
Pour en savoir plus: www.sportspourtous.org
1
/
4
100%