Mai 2011

/¡."*t33
peutique adaptée. Au-delà du
bilan initial l’écho d’effort permet
de suivre l’évolution des symp-
tômes, de leur cause, et donc
l’efficacité de la thérapeutique.
L’écho d’effort permet, comme
l’épreuve d’effort conventionnelle,
de juger de l’adaptation tension-
nelle et de la survenue de troubles
du rythme, et a donc un intérêt
pronostic. Elle permet enfin d’ap-
précier la capacité fonctionnelle
du patient.
Les indications qui en découlent
sont donc:
- bilan initial
- recherche de la cause d’un
symptôme inexpliqué
Le bilan de la cardiomyopathie hypertrophique (CMH) repose de façon
classique sur l’ECG, le Holter ECG, l’Epreuve d’effort et l’Echocardio-
graphie de repos1.
De nos jours, l’IRM cardiaque et l’échocardiographie d’effort viennent
compléter ce bilan. L’intérêt de l’échocardiographie d’effort est
particulièrement évident dans cette cardiopathie complexe où les symp-
tômes ont de multiples causes.
L’échocardiographie d’effort trouve son utilité non seulement dans le bilan
initial mais également lors du suivi des patients.
Echocardiographie
d’effort et CMH
Thierry LE TOURNEAU
C.H.U. de NANTES, Institut du Thorax
FICHE PRATIQUE FICHE PRATIQUE FICH
E
Indications de l’écho-
cardiographie d’effort
L’échocardiographie d’effort
est un examen physiologique qui
associe les avantages de l’épreuve
d’effort conventionnelle et d’une
échocardiographie réalisée pen-
dant l’effort. L’échocardiographie
d’effort devrait en ce sens être
systématique lors du bilan initial
de toute CMH. L’écho d’effort va
permettre de juger du caractère
symptomatique ou asymptoma-
tique du patient porteur de CMH,
de déterminer l’origine des symp-
tômes et va par conséquent gui-
der la mise en place d’une théra-
- évaluation pronostique
- suivi clinique ou
thérapeutique.
Contre-Indications
de l’échocardiographie
d’effort
- Patient en insuffisance car-
diaque stade IV de la NYHA
- Obstruction sous aortique
sévère symptomatique
- Troubles du rythme ventricu-
laires sévères à l’effort
Le simple port d’un défibrillateur
ne constitue pas en soi une contre-
indication à la réalisation d’une écho-
cardiographie d’effort. Le défibrillateur
devra être inhibé si le patient réalise
une échocardiographie d’effort sans
traitement bradycardisant.
Modalités pratiques de
réalisation de l’échocar-
diographie d’effort
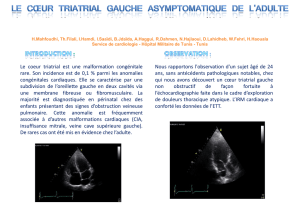
(Fig. 1)
- L’examen sera réalisé sans
traitement chez les nouveaux
patients, mais sous leur traitement
habituel chez les autres patients, sauf
indication particulière.
L’écho d’effort
est un examen
clé dans la
CMH
Figure 1
Echocardiographie d’effort. Le patient est
installé sur un cyclo-ergomètre en position
semi-couchée, incliné vers la gauche,
l’échocardiographiste étant situé à la gauche
du patient. Une surveillance par ECG 12
dérivations est réalisée pendant tout l’effort. La
mesure de la TA à l’effort devra être manuelle.

34t."*/¡
- Un ECG complet sera réalisé
régulièrement pendant toute la durée
de l’effort. Les électrodes seront
positionnées de façon à ne pas gêner
l’examen échocardiographique.
- Tension artérielle: la TA pourra
être prise initialement de façon auto-
matique mais devra être mesurée
manuellement dès que l’effort
devient important du fait du manque
de fiabilité de la plupart des tensio-
mètres automatiques à l’effort.
- Une échocardiographie de
repos complète sera réalisée idéale-
ment en décubitus. Le patient sera
ensuite installé le plus confortable-
ment possible sur un cyclo-ergo-
mètre en position semi-couchée,
incliné vers la gauche pour permettre
un examen plus aisé en échocardio-
graphie pendant l’effort. L’écho-
cardiographiste se placera en géné-
ral à gauche du patient et travaillera
donc de la main gauche.
- L’analyse de la fonction VG
pourra faire appel à un logiciel de
stress. Les autres paramètres étu-
diés pourront être capturés en sor-
tant transitoirement du programme
de stress.
- L’effort sera débuté à une
charge modérée (30-50 W) pendant
3 minutes avec une incrémentation
moyenne de 10 W par minute ensuite
chez la plupart des patients (paliers
de 10 W/min ou 20 W/2 min par
exemple). Une incrémentation plus
rapide pourra être proposée chez
certains patients.
- L’effort sera arrêté lorsque le
patient est épuisé, ou en cas de
douleur thoracique, de malaise, ou
encore de trouble du rythme ventri-
culaire.
Paramètres étudiés
par l’échocardiographie
d’effort. (Tableau)
- Evolution de la tension artérielle
(TA) à l’effort. Une augmentation de
la TA < 20 mm Hg entre le début et
le pic de l‘effort, ou une diminution
de la TA ≥ 20 mmHg entre la valeur-
FICHE PRATIQUE FICHE PRATIQUE FICHE PR
maximale de TA en cours d’effort et
la fin de l’effort est un facteur pro-
nostic péjoratif2.
- Fréquence et rythme car-
diaque. La fréquence cardiaque est
souvent limitée par le traitement
béta-bloquant. La survenue de
troubles du rythme supra-ventricu-
laire ou ventriculaire (TV) est rare au
cours de l’échocardiographie d’effort.
Parmi 263 patients porteurs de CMH
ayant réalisé un test d’effort 3% des
patients ont présenté un trouble du
rythme supra-ventriculaire en cours
d’effort, 4,2% des patients une TV
non soutenue, et seulement 0,4% (1
patient) une TV soutenue3.
- L’analyse de la repolarisation et
en particulier la recherche d’un sous-
décalage du segment ST est d’intérêt
discuté. Il pourrait être associé à un
profil péjoratif des patients porteurs
de CMH. Par contre la constatation
d’un sous-décalage de ST est claire-
ment pathologique et aura une
grande valeur diagnostic dans un
contexte d’hypertrophie chez un
sportif.
- La capacité fonctionnelle du
patient sera appréciée par la puis-
sance maximale atteinte (en Watts).
Cette puissance maximale est généra-
lement inférieure de 10 à 20 W à celle
observée en position debout ou assise.
Elle permet de juger du retentisse-
ment fonctionnel de la cardiopathie.
- Les symptômes au pic de l’ef-
fort, et en particulier le motif d’arrêt
de l’effort déterminé par le patient,
sont importants à considérer. La rai-
son d’arrêt de l’effort sera au mieux
cotée sur une échelle de 1 à 10 par le
patient lui-même en évaluant séparé-
ment la dyspnée et la fatigue des
membres inférieurs.
- L’adaptation du ventricule
gauche (VG) à l’effort sera évaluée
comme dans toute cardiopathie, à la
recherche d’anomalies de cinétique
segmentaire pouvant signer une
atteinte des gros troncs coronaires ou
une atteinte microvasculaire. Une
altération globale de la cinétique VG à
l’effort témoigne d’un défaut de
réserve contractile liée soit à l’altéra-
tion intrinsèque de la contractilité
myocardique soit à l’existence d’une
obstruction sous aortique.
- En l’absence d’obstruction de
repos, la survenue d’une obstruction sous
aortique et/ou médio-VG sera systémati-
quement recherchée à l’effort chez tout
patient porteur de CMH. Le diagnostic
d’obstruction repose sur l’enregistrement
d’un gradient maximal ≥ 30 mmHg1 avec
un aspect de pic tardif. L’existence d’un
mouvement systolique antérieur incom-
plet de la valve mitrale (SAM) prédit le
développement d’une obstruction d’effort
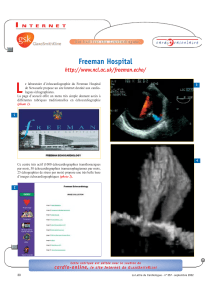
(Fig. 2)4.
ECG:
-Fréquence cardiaque
-Rythme
-Sous décalage de ST
Profil TA d’effort
VG
-Cinétique segmentaire
-FE VG
Obstruction
-Siège
-Gradient max
-Moment de survenue (effort, récupération)
-Evolution de l’obstruction
Insuffisance Mitrale
-Mécanisme
-Grade
Pression pulmonaire systolique
Capacité fonctionnelle
Symptômes, Cause d’arrêt de l’effort
Figure 2
L’existence d’un SAM
valvulaire ou sous-
valvulaire incomplet au
repos (flèche) prédit le
développement d’une
obstruction significative
à l’effort. Une obstruc-
tion significative d’effort
peut cependant appa-
raître en l’absence de
tout SAM ou anomalie
mitrale au repos.

/¡."*t35
Une obstruction significative d’ef-
fort peut cependant apparaître en
l’absence de tout SAM ou anomalie
mitrale au repos (Fig.3). Cette obs-
truction peut survenir pendant l’effort,
mais peut apparaître ou atteindre son
pic en récupération précoce. Elle
devra donc être recherchée pendant
toute la durée de l’effort et durant 6
minutes en récupération. Des don-
nées récentes ont démontré que
l’obstruction sous aortique est un
élément majeur de la CMH, retrouvé
chez 50 à 70% des patients à l’effort
contre seulement 30 à 35% au repos.
Cette obstruction d’effort ou obstruc-
tion latente est responsable de dys-
pnée, lipothymie, syncope ou dou-
leurs thoraciques5,6. La mesure du
gradient d’obstruction est difficile à
l’effort et sera réalisée par voie api-
cale 5 cavités ou 3 cavités. Il existe
fréquemment une superposition à
l’effort entre le flux d’obstruction sous
aortique et un jet de régurgitation
mitrale passant sous la valve anté-
rieure pour venir longer le septum
inter-atrial. Le flux d’obstruction pré-
sente un pic plus tardif que le jet de
régurgitation mitrale et n’excède pas
en général 7 m/s (Fig.4).
-Une insuffisance mitrale sévère
est retrouvée chez moins de 10% des
patients porteurs de CMH.
L’insuffisance mitrale est le plus sou-
vent liée à l’obstruction sous aortique
et au mouvement systolique antérieur
de la valve mitrale (SAM). Cette insuf-
fisance mitrale est aggravée à l’effort
mais n’est pas prédictive de la capa-
cité fonctionnelle et n’est pas asso-
ciée au risque de décès ou d’insuffi-
sance cardiaque. L’insuffisance
mitrale est en général excentrée,
longeant la face atriale de la valve
postérieure puis la paroi inféro-laté-
rale de l’oreillette gauche. Il peut
exister un second jet, moins impor-
tant mais très fréquent à l’effort pas-
sant sous la valve antérieure et lon-
geant le septum inter-atrial.
-Enfin la pression pulmonaire
systolique sera évaluée à l’effort par
le flux de régurgitation tricuspide et la
compliance de la veine cave infé-
rieure.
ATIQUE FICHE PRATIQUE FICHE PRATIQUE
Figure 4
Superposition des flux d’obs-
truction sous aortique et d’insuf-
fisance mitrale.
Figure 3
Patient de 23 ans présentant des anomalies de l’ECG de repos. A) Aspect d’hypertrophie apico-latérale (*), absence de SAM au repos
(flèche). B) Apparition d’un SAM typique à l’effort (flèche) avec une obstruction sévère (gradient maximal 100 mm Hg).
RÉFÉRENCES
.BSPO#+.D,FOOB8+%BOJFMTPO(,FUBM"NFSJDBO$PMMFHFPG$BSEJPMPHZ&VSPQFBO
4PDJFUZPG$BSEJPMPHZDMJOJDBMFYQFSUDPOTFOTVTEPDVNFOUPOIZQFSUSPQIJDDBSEJPNZPQB
UIZ " SFQPSU PG UIF "NFSJDBO $PMMFHF PG $BSEJPMPHZ 'PVOEBUJPO 5BTL 'PSDF PO $MJOJDBM
&YQFSU $POTFOTVT %PDVNFOUT BOE UIF &VSPQFBO 4PDJFUZ PG $BSEJPMPHZ $PNNJUUFF GPS
1SBDUJDF(VJEFMJOFT+"N$PMM$BSEJPM
4BEPVM/1SBTBE,&MMJPUU1.FUBM1SPTQFDUJWFQSPHOPTUJDBTTFTTNFOUPGCMPPEQSFT
TVSFSFTQPOTFEVSJOHFYFSDJTFJOQBUJFOUTXJUIIZQFSUSPQIJDDBSEJPNZPQBUIZ$JSDVMBUJPO
%SJOLP+,/BTI1+-FWFS).FUBM4BGFUZPGTUSFTTUFTUJOHJOQBUJFOUTXJUIIZQFSUSPQIJD
DBSEJPNZPQBUIZ"N+$BSEJPM
;ZXJDB,+FOOJ31FMMJLLB1"FUBM%ZOBNJDMFGUWFOUSJDVMBSPVUGMPXUSBDUPCTUSVDUJPO
FWPLFECZFYFSDJTFFDIPDBSEJPHSBQIZQSFWBMFODFBOEQSFEJDUJWFGBDUPSTJOBQSPTQFDUJWF
TUVEZ&VS+&DIPDBSEJPHS
.BSPO .4 0MJWPUUP * ;FOPWJDI "( FU BM )ZQFSUSPQIJD DBSEJPNZPQBUIZ JT QSFEPNJ
OBOUMZBEJTFBTFPGMFGUWFOUSJDVMBSPVUGMPXUSBDUPCTUSVDUJPO$JSDVMBUJPO
4IBI+4&TUFCBO.55IBNBO3FUBM1SFWBMFODFPGFYFSDJTFJOEVDFEMFGUWFOUSJDVMBS
PVUGMPXUSBDUPCTUSVDUJPOJOTZNQUPNBUJDQBUJFOUTXJUIOPOPCTUSVDUJWFIZQFSUSPQIJDDBS
EJPNZPQBUIZ)FBSU
1
/
3
100%