Document

LES ANTI-ÉPILEPTIQUES : PLAN
A – ÉPILEPSIES :
A1 – HISTORIQUE
A2 – CLASSIFICATION
A3 – CAUSES
A4 – MÉCANISMES CELLULAIRES et MOLÉCULAIRES
A5 – ÉVOLUTION et PRONOSTIC
B – MÉDICAMENTS ANTI-ÉPILEPTIQUES :
B1 – HISTORIQUE
B2 – CLASSIFICATION
B3 – FORMULE GÉNÉRALE et RELATIONS STRUCTURE-ACTIVITÉ
B4 – COMPOSÉS UTILISÉS EN THÉRAPEUTIQUE
B4 - 1 – AC CONVENTIONNELS (1ère GÉNÉRATION) :
a) Phénytoïne, Carbamazépine, A.valproïque
b) Benzodiazépines, Phénobarbital
c) Éthosuximide
B4 - 2 – NOUVEAUX AC (2ème génération) :
a) Felbamate, Oxcarbazépine, Lamotrigine
b) Vigabatrin, Gabapentine,Tiagabine
c) Topiramate
C – EFFETS INDÉSIRABLES
D – CONCLUSION : PERSPECTIVES d’AVENIR

A - LES ÉPILEPSIES
A1 – HISTORIQUE
A2 – CLASSIFICATION
peuvent se produire dans différentes parties du cerveau
RAPPELS : la crise épileptique = résultat de décharges électriques excessives
soudaines
brèves dans un groupe de neurones
les neurones = cellules qui communiquent entre-elles par des micro courants électriques
manifestations cliniques variables
fonction de des cellules touchées
la localisation
la fonction
P
P
Po
o
ou
u
ur
r
r
c
c
co
o
om
m
mp
p
pr
r
re
e
en
n
nd
d
dr
r
re
e
e
l
l
le
e
es
s
s
i
i
in
n
nd
d
di
i
ic
c
ca
a
at
t
ti
i
io
o
on
n
ns
s
s
d
d
de
e
es
s
s
A
A
A.
.
.C
C
C,
,
,
i
i
il
l
l
e
e
es
s
st
t
t
i
i
im
m
mp
p
po
o
or
r
rt
t
ta
a
an
n
nt
t
t
d
d
de
e
e
c
c
co
o
on
n
nn
n
na
a
aî
î
ît
t
tr
r
re
e
e
l
l
la
a
a
c
c
cl
l
la
a
as
s
ss
s
si
i
if
f
fi
i
ic
c
ca
a
at
t
ti
i
io
o
on
n
n
i
i
in
n
nt
t
te
e
er
r
rn
n
na
a
at
t
ti
i
io
o
on
n
na
a
al
l
le
e
e
d
d
de
e
es
s
s
é
é
ép
p
pi
i
il
l
le
e
ep
p
ps
s
si
i
ie
e
es
s
s
a) Les CRISES PARTIELLES ou FOCALES (60% des épilepsies) :
Certaines parties du cerveau sont atteintes
Symptômes en rapport avec les fonctions du cortex cérébral intéressé par la décharge épileptique :
Simples (sans modification de l’état de conscience) ou complexes (altération de l’état de conscience, soit immédiate, soit
secondaire)
Caractérisées par des mouvements musculaires répétitifs avec altération des 5 sens
Peuvent rester localisées ou s'étendre à l'ensemble du cerveau.
b) Les CRISES GÉNÉRALISÉES : la décharge paroxystique intéresse les 2 hémisphères cérébraux
Crises Non Convulsives : absences ou crises de Petit Mal, absences atypiques
Crises Convulsives : crises cloniques/ myocloniques, toniques, atoniques, crise tonico-clonique (GRAND MAL)
L'état de mal épileptique corrrespond à un état de crises permanentes

A3 – CAUSES : voir cours pharmaco
A4 – MÉCANISMES CELLULAIRES et MOLÉCULAIRES :
Les phénomènes convulsifs résultent d’une rupture d’équilibre entre des médiateurs stimulants et inhibiteurs :
éléments stimulants : médiateurs adrénergiques / cholinergiques / acide glutamique [HOOC-(CH2)2-CH (NH2)-COOH]
éléments inhibiteurs : sérotonine / glycine / GABA [acide -aminobutyrique = H2N-(CH2)3-COOH]
les médicaments peuvent réduire l'hyperexcitabilité neuronale en agissant sur le(s) mécanismes dont elle résulte :
- soit en augmentant le tonus inhibiteur (dépendant de l'acide -aminobutyrique)
- soit en diminuant l'influx excitateur (dépendant du glutamate)
Au plan cellulaire : 3 mécanismes de base sont reconnus :
- modulation des canaux ioniques potentiel-dépendants (Na+, Ca2+, K+),
- augmentation de la neurotransmission inhibitrice médiée par le GABA,
- blocage de la neurotransmission excitatrice médiée par le glutamate
Au niveau du GABA ?
CRISES ? quand le GABA ne remplit pas correctement sa fonction
quand déficit en GABA (d’où chronicité des décharges dans un site neuronal quelconque)
TRAITEMENT ? utiliser des molécules qui l’action de GABA
augmenter la concentration en GABA dans la région concernée
GABA
1) inhiber la GABA-transaminase :
NH2(CH2)3COOH NH2CH
COOH
COOH(CH2)2
A.Glutamique
gaba
transaminase
2) stimuler la GABA-décarboxylase :
NH2(CH2)3COOH
GABA
NH2CH
COOH
COOH(CH2)2
A.Glutamique vitamine B 6
dépendante

GABA
NH2(CH2)3COOH NH2CH
COOH
COOH(CH2)2
A.Glutamique
gaba
transaminase
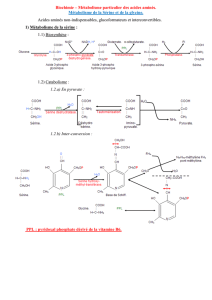
Sous l’action de la GABATRANSAMINASE, le GABA se transforme en Acide Glutamique
qui se convertit à son tour en Aldéhyde Hémosuccunique
Aldéhyde hémosuccinique
A.Glutamique décarboxylation
métabolique CO2 +
CH
COOH
COOH(CH2)2
H2N
COOH(CH2)2
H2NCH2
OH
désamination oxydative
C
H
COOH(CH2)2
O
N
H
H..
H
(
NH3
+
O = (CH2)2COOHCH

B - LES MÉDICAMENTS ANTI-ÉPILEPTIQUES
B1 – HISTORIQUE :
B2 – CLASSIFICATION :
Pas de classification officielle des anti-épileptiques :
classement selon leur structure chimique (inadapté aux nouvelles molécules de structures diverses)
- composés pentagonaux
- composés azépiniques
- composés pyrimidiques
- dérivés de l’acide valproïque ? dérivés du GABA ?
classement en fonction du mécanisme d’action reconnu comme prédominant
- les sodiques
- les GABAergiques ou GABAmimétiques
- les glutamatergiques
- les calciques
classement actuel en 3 grands groupes
les AC conventionnels ( 1ère génération
les nouveaux AC de 2ème génération
les AC de 3ème génération (2000)
But de ces nouveaux produits :
Diminuer les 25% d'épilepsies pharmacorésistantes, vouées à la chirurgie
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
1
/
20
100%