L`interleukine 13 : une nouvelle pièce dans le puzzle - iPubli

884
SYNTHÈSE
L
« »
IL 4,

y.

886
Eets paagés
avec
Eets diérents de
.
+
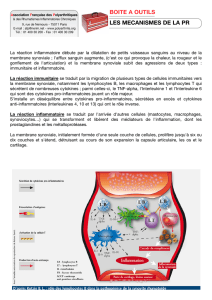
Activités de L 13 sur les monocytes et les macrophages.
=

W.
r
Leu
887

888
·
f
!
A
1
/
5
100%