Piles et accumulateurs Problème du « stockage » de l`énergie

Piles et accumulateurs
Problème du « stockage » de l'énergie électrique.
Une réponse : sous forme chimique avec les piles et
accumulateurs.
I_ Les piles
1°) Constitution d'une pile
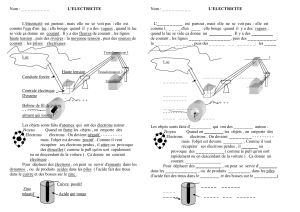
Elle est constituée de deux demi-piles comportant chacune une
électrode plongeant dans une solution contenant des ions (un
électrolyte). Les deux compartiments contenant les solutions sont
reliées par une jonction assurant le passage des ions.
2°) Transformations chimiques dans une pile
Le sens du courant donné par l'ampèremètre permet de déterminer
A
pont
salin
Métal 1 Métal 2
Electrolyte 1 Electrolyte 2
Demi-pile 1 Demi-pile 2
A
Paroi poreuse

le sens de circulation des électrons dans le circuit extérieur.
Si le courant I va du métal 1 au métal 2, les électrons se déplacent
en sens inverse.
Des électrons sont produits par le métal 2 et consommés par le
métal 2.
Le pôle positif de la pile consomme des électrons, le pôle négatif en
produit.
Exemples : la pile Daniell (voir TP) :
Le courant i va de la lame de cuivre (pôle +) vers la lame de zinc
(pôle -). Les électrons sont produits par la lame de zinc et
consommés par la lame de cuivre.
La pile à combustible doc. 8 p. 284
Les accumulateurs : piles rechargeables (batteries).
3°) Rôle de la jonction entre les demi-piles
Elle permet le transfert des ions d'une demi-pile à l'autre pour
assurer la neutralité électrique de chaque solution.
II_ Réactions d'oxydoréduction
Les réactions se produisant sur les lames métalliques consistent en
un transfert d'électrons entre espèces chimiques : elles sont
appelées réactions d'oxydoréduction.
1°) Oxydation et réduction
Exemple de la pile Daniel
La lame de cuivre reçoit des électrons qui sont captés par les ions
Cu2+ qui deviennent des atomes de cuivre Cu et se déposent sur la
lame. La lame de cuivre constitue la cathode : il y a réduction
Le ions Cu2+ ont subi une réduction (gain d'électrons).
Cu2+ (aq) + 2 e- Cu(s)
Le zinc (métal) subit une oxydation (perte d'électrons) :
Zn(s) Zn2+ (aq) + 2 e-
La lame de zinc constitue l'anode : il y a oxydation.
2°) Oxydant et réducteur
Les ions cuivre II ont captés des électrons : c'est un oxydant.
Le métal zinc a cédé des électrons : c'est un réducteur.
L'oxydant est réduit, le réducteur est oxydé.
3°) Couple oxydant/réducteur

Le cuivre Cu et l'ion cuivre II Cu2+ liés par l'échange de deux
électrons dans l'équation bilan Cu2+ (aq) + 2 e- Cu(s) forment un
couple oxydant/réducteur noté Cu2+/Cu.
On a aussi le couple Zn2+/Zn.
Exemple de couples oxydant/réducteur doc. 13 p. 287
Pour un couple Ox/Red on pourra écrire:
Ox + n e- Red : réduction
et
Red Ox + n e- : oxydation
4°) Réaction d'oxydoréduction
Une réaction d'oxydoréduction (ou réaction rédox) résulte de
l'échange d'électrons entre deux couples oxydant/réducteur (ou
couples rédox): Ox1/Red1 et Ox2/Red2
Exemple: réaction entre Ox1 et Red2
Ox1 + n e- → Red1
Red2 → Ox2 + p e-
Les électrons échangés n'apparaissent pas dans l'équation bilan:on
multiplie la première demi-équation par p et la deuxième par n:
p Ox1 + p.n e- → p Red1
n Red2 → n Ox2 + n.p e-
En ajoutant membre à membre:
p Ox1 + nRed2 p Red1 + n Ox2
1
/
3
100%