Forme familiale de la non compaction isolée du ventricule gauche

Annales
de
Cardiologie
et
d’Angéiologie
62
(2013)
56–59
Fait
clinique
Forme
familiale
de
la
non
compaction
isolée
du
ventricule
gauche
;
cas
d’une
mère
et
de
son
fils
observés
au
Gabon
Family
form
of
isolated
left
ventricular
noncompaction;
case
of
a
mother
and
her
son
observed
in
Gabon
J.B.
Mipindaa,∗,
J.
Ibabab,
D.D.
Nkoghec,
P.A.
Kombilaa
aService
de
cardiologie,
centre
hospitalier
de
Libreville,
B.P.
6392
Libreville,
Gabon
bService
de
médecine
interne,
centre
hospitalier
de
Libreville,
Libreville,
Gabon
cCentre
de
recherche
médicale
de
Franceville,
Gabon
Rec¸u
le
16
mars
2009
;
accepté
le
17
avril
2011
Disponible
sur
Internet
le
10
mai
2011
Résumé
Il
s’agit
du
cas
d’une
jeune
femme
gabonaise
ayant
présenté
un
œdème
aigu
du
poumon
sur
une
suspicion
de
cardiomyopathie
du
péripartum.
Les
investigations
ultérieures
ont
révélé
une
non
compaction
isolée
du
ventricule
gauche.
La
même
affection
a
été
décelée
chez
son
fils
de
neuf
ans
ayant
présenté
une
décompensation
gauche.
Nous
soupc¸onnons
donc
une
forme
familiale
et
c’est
la
première
description
en
Afrique
subsaharienne.
Le
caractère
héréditaire
de
cette
nouvelle
forme
de
cardiomyopathie
liée
à
une
mutation
génétique
sur
le
chromosome
X
est
bien
connu.
Le
mode
d’expression
peut
être
une
insuffisance
cardiaque,
une
complication
thromboembolique
ou
un
trouble
du
rythme
ventriculaire
grave.
Les
moyens
diagnostiques
sont
l’échocardiographie
Doppler
et
la
résonance
magnétique
nucléaire.
En
Afrique,
l’accès
à
ces
techniques
d’imagerie
reste
un
privilège.
Ainsi
la
découverte
de
la
maladie
est
souvent
tardive
et
les
enquêtes
familiales
sont
exceptionnelles.
Le
traitement
à
notre
portée
est
celui
de
l’insuffisance
cardiaque.
L’implantation
de
défibrillateur
automatique
en
cas
de
trouble
du
rythme
grave
reste
illusoire.
La
transplantation
cardiaque
indiquée
dans
les
formes
sévères
ne
peut
être
réalisée
en
Afrique
centrale.
Ainsi
le
pronostic
de
nos
patients
demeure
réservé
sauf
dans
les
formes
asymptomatiques.
L’équipement
des
nos
structures
hospitalières
et
la
formation
des
spécialistes
africains
aux
nouvelles
techniques
devrait
améliorer
la
prise
en
charge
de
tels
patients.
©
2011
Elsevier
Masson
SAS.
Tous
droits
réservés.
Mots
clés
:
Non
compaction
isolée
;
Ventricule
gauche
;
Forme
familiale
;
Gabon
Abstract
We
describe
a
case
report
of
a
young
Gabonese
lady
who
presented
an
acute
pulmonary
oedema
and
we
suspected
a
paripartum
cardiomyopathy.
Subsequent
investigations
showed
isolated
left
ventricular
noncompaction.
A
few
months
later,
the
same
disease
was
disclosed
at
her
9
year-old
son
who
presented
a
cardiac
insufficiency.
Therefore,
we
suspect
a
family
form
of
left
ventricular
noncompaction.
And
it
is
the
first
description
in
subsaharan
Africa.
The
hereditary
character
of
this
new
form
of
cardiomyopathy
linked
to
a
genetic
mutation
on
the
X
chromosome
is
well
known.
This
disease
is
associated
with
heart
failure,
high
incidence
of
systemic
thromboembolism
complications
or
ventricular
arrhythmia.
The
echocardiography
and
the
cardiac
magnetic
resonance
imaging
has
been
reported
to
be
tools
for
diagnosis.
In
Africa,
access
to
these
techniques
remains
a
privilege.
So
the
discovery
of
illness
is
often
late
and
the
family
screening
are
special.
In
our
area,
the
therapeutic
management
is
the
medical
treatment
of
heart
failure.
Implatable
cardioverter
defibrillator
or
heart
transplantation
are
not
available.
So
long-term
prognosis
of
our
patients
with
congestive
heart
failure
stays
poor.
With
best
equipment
in
our
hospitals
and
good
training
of
African
cardiologists,
we
should
improve
the
management
of
our
patients.
©
2011
Elsevier
Masson
SAS.
All
rights
reserved.
Keywords:
Isolated
noncompaction;
Left
ventricular;
Family
form;
Gabon
∗Auteur
correspondant.
Adresse
e-mail
:
(J.B.
Mipinda).
0003-3928/$
–
see
front
matter
©
2011
Elsevier
Masson
SAS.
Tous
droits
réservés.
doi:10.1016/j.ancard.2011.04.007

J.B.
Mipinda
et
al.
/
Annales
de
Cardiologie
et
d’Angéiologie
62
(2013)
56–59
57
La
non
compaction
isolée
du
ventricule
gauche
demeure
une
pathologie
de
diagnostic
rare
et
difficile
surtout
en
milieu
tropi-
cal.
En
effet,
le
manque
de
moyen
d’investigation
fiable,
telle
la
résonance
magnétique
nucléaire
et
la
multitude
des
cardiomyo-
pathies
d’origine
indéterminée
ne
facilitent
pas
l’identification
de
cette
nouvelle
entité
nosologique.
Il
s’agit
d’une
affection
myocardique
congénitale
caractérisée
par
une
hypertrophie
avec
ou
sans
dilatation
du
ventricule
gauche
qui
comporte
de
pro-
fondes
trabéculations
et
des
recessus
intertrabeculaires.
Elle
serait
secondaire
à
un
retard
enregistré
dans
la
ventriculoge-
nèse.
Elle
peut
se
manifester
dès
le
jeune
âge
sous
forme
de
tableau
d’insuffisance
cardiaque
gauche,
voire
globale.
Les
complications
les
plus
redoutables
sont
représentées
par
le
risque
thromboemboliques
et
la
survenue
de
troubles
du
rythme
res-
ponsable
parfois
de
la
mort
subite.
La
description
de
forme
familiale
a
été
rarement
rapportée
à
travers
le
monde.
Il
s’agit
d’une
première
observation
en
Afrique
subsaharienne.
Nous
rapportons
ici
le
cas
d’une
jeune
patiente
de
30
ans,
de
race
noire,
sans
facteur
de
risque
cardiovasculaire
connu,
admise
en
soins
intensifs
de
cardiologie
pour
prise
en
charge
d’un
œdème
aigu
du
poumon
survenu
dans
le
postpartum
immé-
diat.
En
effet,
trois
jours
après
avoir
accouché
par
voie
basse,
la
patiente
a
présenté
une
dyspnée
aiguë
de
stade
III
selon
la
NYHA
avec
l’existence
d’un
galop
protodiastolique
gauche
et
des
râles
crépitant
des
bases
pulmonaires
à
l’examen
clinique.
La
radio-
graphie
effectuée
en
urgence
objectivait
une
cardiomégalie
avec
un
rapport
cardiothoracique
à
0,73
et
des
opacités
floconneuses
parahilaires.
L’électrocardiogramme
montrait
une
tachycar-
die
sinusale
à
124
par
minute
avec
des
signes
d’hypertrophie
ventriculaire
gauche
électrique
de
type
surcharge
systolique.
C’est
à
l’échocardiographie
Doppler
que
l’on
retrouvait
une
hypertrophie
dilatation
du
ventricule
gauche
avec
un
diamètre
télédiastolique
à
65
mm
et
surtout
un
comblement
de
l’apex
ainsi
que
de
la
paroi
postero-latérale
par
de
proéminentes
tra-
béculations
(Fig.
1
et
2).
On
notait
une
hypokinésie
pariétale
globale
et
une
altération
profonde
de
la
fonction
systolique
ven-
triculaire
gauche
avec
une
fraction
d’éjection
évaluée
à
27
%.
L’hypothèse
de
départ
était
celle
d’une
cardiomyopathie
du
péri-
partum
s’exprimant
sous
un
mode
d’œdème
aigu
du
poumon.
La
patiente
a
bénéficié,
outre
du
repos
en
hospitalisation
et
de
la
restriction
hydrosodée,
d’un
traitement
aux
diurétiques
de
l’anse
associé
aux
inhibiteurs
de
l’enzyme
de
conversion,
aux
dérivés
nitrés
et
à
la
prévention
thromboembolique.
L’évolution
sur
le
plan
fonctionnel
a
été
rapidement
favorable
avec
le
passage
de
la
dyspnée
du
stade
III
au
stade
II
de
la
NYHA.
La
patiente
a
été
libérée
après
une
semaine
d’hospitalisation
tout
en
conservant
un
traitement
au
long
cours
à
base
d’inhibiteur
de
l’enzyme
de
conversion
(captopril
50
mg/j)
associé
à
de
faible
dose
de
furo-
sémide
(20
m/j)
et
d’acide
acétylsalicylique
(160
mg/j).
Nous
avons
attendu
deux
semaines
avant
l’introduction
de
faible
dose
de
bêtabloquant
(carvedilol
à
6,25
mg/j).
Une
fois
stabilisée,
la
patiente
a
profité
d’un
séjour
en
Europe
pour
effectué
un
bilan
étiologique
de
sa
cardiopathie.
Elle
a
bénéficié
d’une
corona-
rographie
qui
s’est
avéré
normale.
Une
résonance
magnétique
nucléaire
a
donc
été
demandée.
Ce
dernier
examen
a
objectivé
un
ventricule
gauche
dilaté
d’aspect
spongieux
avec
d’importantes
trabéculations
et
un
rapport
des
zones
non
compactées
et
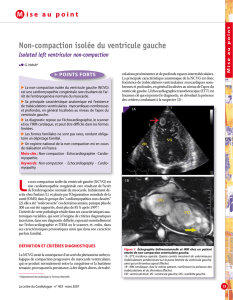
Fig.
1.
Échocardiographie
en
incidence
long
axe
(patient
no1).
Importantes
trabéculations
apicales
et
postéro-latérales
avec
recessus
intertrabéculaires.
compactées
supérieur
à
2,5.
Un
hypersignal
était
observé
au
sein
des
zones
non
compactées
lors
des
séquences
T2.
Le
diagnos-
tic
de
non
compaction
du
ventricule
gauche
a
donc
été
évoqué.
L’attitude
thérapeutique
demeurait
inchangée.
Quelques
mois
après
son
retour,
la
patiente
nous
a
amené
son
fils
âgé
de
neuf
ans
chez
lequel
une
cardiomégalie,
avec
un
rapport
cardiotho-
racique
évalué
à
0,60
a
été
descellée
dans
le
cadre
du
bilan
d’un
syndrome
bronchique
avec
dyspnée
de
stade
II
de
la
NYHA.
Nous
avons
donc
complété
le
bilan
par
un
électrocardiogramme
et
une
échocardiographie
Doppler.
Ce
dernier
examen
a
mis
en
évidence
un
aspect
très
particulier
du
myocarde
du
ventricule
gauche
qui
était
dilaté
pour
son
âge
avec
un
diamètre
télédias-
tolique
évalué
à
53
mm
et
qui
comportait
surtout
d’importantes
trabéculations
et
de
profonds
recessus
intertrabeculaires
avec
comme
un
plan
de
clivage
entre
le
myocarde
sous
endocardique
et
la
couche
sous-épicardique
(Fig.
3).
Par
ailleurs
au
Doppler
couleur
on
observait
un
remplissage
intertrabeculaire
par
le
flux
sanguin.
La
fonction
systolique
ventriculaire
gauche
était
alté-
rée
avec
une
fraction
d’éjection
ventriculaire
gauche
évaluée
à
34
%
par
la
méthode
Simpson.
L’enfant
a
été
stabilisé
sur
le
plan
fonctionnel
grâce
à
un
traitement
diurétique
associé
aux
inhibi-
teurs
de
l’enzyme
de
conversion
et
à
la
digitoxine.
L’évolution
à
long
terme
chez
l’enfant
était
favorable
avec
une
amélioration
clinique.
Nous
avons
toutefois
conservé
le
traitement
de
fond
à
base
d’inhibiteurs
d’enzyme
de
conversion.
1.
Discussion
La
non
compaction
isolée
du
ventricule
gauche
est
une
affec-
tion
encore
ignorée
en
Afrique
subsaharienne.
De
nombreuses
cardiomyopathies
dilatées
demeurent
d’étiologie
indéterminée
du
fait
d’une
description
échographique
incomplète.
En
effet,
peu
d’équipes
disposent
d’échographes
performants
et
le
mode
Doppler
couleur
est
parfois
inexistant.
La
résonance
magné-
tique
nucléaire
reste
inaccessible
pour
la
grande
majorité
de
nos
patients.
D’ailleurs
très
peu
de
capitales
en
Afrique
centrale
possèdent
cette
technique
d’imagerie
médicale.

58
J.B.
Mipinda
et
al.
/
Annales
de
Cardiologie
et
d’Angéiologie
62
(2013)
56–59
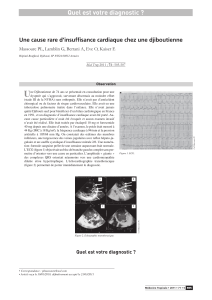
Fig.
2.
Échocardiographie
en
coupe
apicale
quatre
cavités
(patiente
no1).
Dilata-
tion
du
ventricule
gauche.
Hypokinésie
globale.
Endocarde
épais
non
compacté.
Il
s’agit
d’une
affection
à
caractère
héréditaire
et
qui
se
transmet
sous
un
mode
autosomique
dominant
[1].
Le
premier
gène
en
rapport
avec
ce
morphotype
est
le
gène
G4.5
isolé
sur
le
chromosome
X
en
position
Xq28
[2].
Elle
est
susceptible
d’être
retrouvée
chez
les
sujets
d’une
même
famille
sur
plu-
sieurs
générations.
C’est
ainsi
que
Matsuda
et
al.
[3]
ont
décrit
plusieurs
cas
dans
une
famille
japonaise
et
sur
trois
générations.
La
non
compaction
du
ventricule
gauche
était
souvent
décrite
en
association
avec
d’autres
malformations
congénitales
dans
le
cadre
du
microphtalmia
with
linear
skin
defects
(MLS)
syn-
drome
qui
regroupe
une
dysmorphie
faciale,
une
microcéphalie
et
une
microphtalmie.
[4].
Ce
n’est
qu’en
1984
qu’elle
a
été
retenue
comme
une
cardiopathie
à
part
entière
lorsque
les
autres
anomalies
ont
été
exclues.
Sur
le
plan
embryologique,
c’est
l’interruption
de
la
matura-
tion
du
myocarde
entre
la
cinquième
et
la
huitième
semaine
chez
le
fœtus
qui
explique
la
persistance
des
espaces
inter-
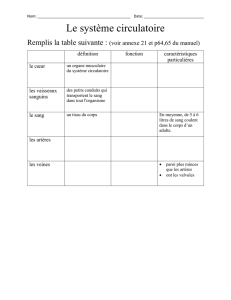
Fig.
3.
Échocardiographie
en
incidence
apicale
quatre
cavités
(patient
no2).
Proéminentes
trabéculations
apicales
et
latérales.
Aspect
non
compacté
du
ven-
tricule
gauche.
trabéculaires
destinés
en
temps
normal
à
la
formation
des
capillaires.
Sur
le
plan
anatomique,
on
distingue
alors
le
myocarde
sous
épicardique
constitué
par
une
couche
fine
bien
compacté
et
le
myocarde
sous
endocardique
deux
à
trois
fois
plus
épaisse
non
compactée
avec
parfois
des
plages
de
nécrose
ou
des
troubles
de
la
microcirculation.
[5].
La
découverte
se
fait
soit
lors
d’une
décompensation
car-
diaque
classique
et
cela
a
été
le
cas
chez
nos
deux
patients.
Parfois
au
décours
d’une
mort
subite
[6].
Les
complications
rythmiques
telles
que
la
fibrillation
auriculaire
retrouvée
dans
25
%
des
cas
constituent
l’un
des
modes
révélateurs
de
la
mala-
die.
Il
en
est
de
même
des
accidents
ischémiques
occasionnés
par
la
migration
d’emboles
se
constituant
dans
les
espaces
inter-
trabéculaires
surtout
en
cas
de
dilatation
des
cavités
cardiaques
associée
à
une
altération
de
la
fonction
systolique
ventriculaire
gauche.
C’est
ainsi
que
chez
nos
patients,
nous
avons
instauré
une
prophylaxie
thromboembolique
dès
l’admission
du
fait
de
l’aspect
de
cardiomyopathie
dilatée
avec
hypokinésie
segmen-
taire
et
parfois
très
diffuse.
L’approche
diagnostique
reste
incertaine
dans
notre
sous
région.
Nous
rapportons
ici
pour
la
première
fois
une
forme
familiale.
Mais
nous
soulignons
que
le
premier
diagnostic
évo-
qué
était
celui
d’une
cardiomyopathie
du
péripartum.
C’est
grâce
à
la
réalisation
d’une
résonance
magnétique
nucléaire
en
France
que
le
diagnostic
d’une
non
compaction
isolée
du
ventricule
gauche
a
été
évoqué.
C’est
par
manque
d’expérience
que
nous
n’avons
pas
pu
poser
le
diagnostic
sur
la
base
d’une
échocardio-
graphie
Doppler.
Cet
examen
est
en
effet
largement
suffisant
en
appliquant
les
critères
de
Jenni
et
al.
[7],
à
savoir
l’observation
de
proéminentes
trabéculations
avec
des
espaces
intertrabéculaires.
L’épaisseur
de
la
couche
sous-endocardique
non
compactée
doit
être
deux
fois
supérieure
à
celle
de
la
couche
sous-épicardique
compactée.
Au
Doppler
couleur,
le
flux
sanguin
doit
remplir
les
recessus
intertrabéculaires.
Et
on
ne
doit
pas
observer
d’autres
anomalies
d’allure
congénitale
associées.
On
peut
ainsi
faire
la
distinction
avec
les
autres
cardiomyopathies
surtout
les
formes
dilatées
et
hypertrophiques
souvent
rencontrées
chez
les
hyper-
tendus
de
grade
élevés
arrivant
d’ailleurs
dans
un
tableau
de
décompensation
globale.
L’électrocardiogramme
n’apporte
pas
d’élément
spécifique.
Toutefois
on
retrouve
chez
la
majorité
des
patients
des
troubles
conductifs
ou
des
troubles
du
rythme
supraventriculaires
en
cas
de
dilatation
de
l’oreillette
gauche.
Le
risque
de
complication
thromboembolique
est
alors
majoré
surtout
en
cas
de
fibrillation
auriculaire.
La
résonance
magnétique
nucléaire
est
d’une
aide
précieuse
dans
la
confirmation
du
diagnostic.
En
effet
lorsqu’elle
est
disponible,
elle
permet
de
mieux
localiser
les
trabéculations
et
surtout
de
bien
distinguer
la
couche
non
compactée
de
la
couche
compactée
et
de
déterminer
le
rapport
des
épaisseurs
des
deux
couches.
Cet
indice
est
considéré
comme
significa-
tif
lorsqu’il
dépasse
2,3
[8].
Cet
examen
nous
a
donc
permis
de
poser
le
diagnostic
de
non
compaction
isolée
du
ventricule
gauche
pour
la
première
fois
au
Gabon.
Les
premières
obser-
vations
africaines
ont
été
faites
par
Paule
et
al.
en
2007
[9].
Toutefois
la
résonance
magnétique
nucléaire
vient
en
complé-

J.B.
Mipinda
et
al.
/
Annales
de
Cardiologie
et
d’Angéiologie
62
(2013)
56–59
59
ment
de
l’échocardiographie
doppler
transthoracique.
C’est
fort
de
cette
expérience
que
nous
nous
sommes
contentés
de
l’échographie
pour
évoquer
le
même
diagnostic
chez
le
second
patient.
Nous
avons
aussi
effectué
une
enquête
familiale
pour
soulever
l’hypothèse
de
la
probable
forme
familiale.
L’approche
thérapeutique
dépendra
effectivement
du
tableau
clinique
présenté
par
le
malade
et
des
facteurs
de
risque
associés.
Le
traitement
en
cas
d’insuffisance
cardiaque
associe
toujours
les
inhibiteurs
de
l’enzyme
de
conversion,
les
diurétiques,
les
anticoagulants
pour
la
prévention
thrombo
embolique
surtout
en
présence
de
contrast
spontané
à
l’intérieur
des
cavités
dilatées.
Toutefois
la
poursuite
de
ce
traitement
anticoagulant
en
ambu-
latoire
par
l’usage
des
anti-vitamines
K
reste
un
sujet
à
débattre.
En
effet,
il
existe
des
difficultés
de
comprendre
les
exigences
et
les
précautions
à
prendre
chez
les
patients
sous
anticoagu-
lants.
Surtout
en
milieu
rural
ou
chez
les
patients
non
scolarisés.
Cet
état
des
choses
nous
amène
souvent
à
nous
contenter
de
la
prescription
d’anti-agrégant
qui
à
la
lumière
des
grandes
études
n’assurent
pas
une
prévention
efficace
du
risque
thromboembo-
lique.
Devant
les
troubles
du
rythme
ventriculaires
d’allure
maligne,
l’indication
d’un
défibrillateur
automatique
implantable
reste
discutable.
En
effet,
il
s’agit
d’une
affection
rencontrée
chez
les
sujets
relativement
jeune
et
même
chez
les
enfants
comme
dans
cette
forme
familiale
que
nous
décrivons
ici.
De
plus,
le
coût
d’implantation
et
de
surveillance
de
pacemaker
reste
inaccessible
dans
notre
pays
où
il
n’existe
pas
d’unité
de
sti-
mulation
cardiaque.
Il
en
est
de
même
pour
la
transplantation
cardiaque
préconisée
par
certaines
équipes
chez
les
sujets
jeunes
qui
présentent
des
paramètres
de
mauvais
pronostic.
Le
pronos-
tic
dépend
du
stade
évolutif
de
la
maladie,
des
complications
thromboemboliques
et
rythmiques
associées
et
bien
sur
des
traitements
institués.
Nombreux
sont
les
jeunes
patients
qui
restent
longtemps
asymptomatiques
et
chez
lesquels
le
pro-
nostic
demeure
satisfaisant.
Mais
l’apparition
des
symptômes
d’insuffisance
cardiaque
et
surtout
la
survenue
de
troubles
du
rythme
marquent
l’altération
du
pronostic
du
malade
[10].
Dans
notre
observation,
nous
ne
disposons
pas
encore
assez
de
recul
pour
juger
de
l’évolution
à
long
terme
de
nos
patients.
Toutefois
nous
avons
préconisé
la
poursuite
du
traitement
de
l’insuffisance
cardiaque
chez
les
deux,
l’adjonction
de
bêtabloquants
chez
la
mère
qui
par
ailleurs
a
été
mise
sous
contraceptifs
afin
de
limiter
les
grossesses
qui
sont
susceptibles
de
décompenser
sa
cardio-
pathie.
L’enfant
sera
suivi
simultanément
par
les
pédiatres
et
les
cardiologues.
C’est
lui
qui
nous
permettra
de
surveiller
le
pro-
nostic
d’un
jeune
patient
porteur
d’une
forme
familiale
de
non
compaction
du
ventricule
gauche.
2.
Conclusion
Parmi
les
cardiomyopathies
d’origine
indéterminée
et
de
description
limitée
rencontrée
en
Afrique
subsaharienne,
la
non
compaction
isolée
du
ventricule
gauche
occupe
sans
nul
doute
une
place
non
négligeable.
Malgré
l’absence
des
tech-
niques
d’imagerie
modernes
comme
la
résonance
magnétique
nucléaire,
l’usage
de
l’échocardiographie-Doppler
transthora-
cique
s’avère
largement
suffisant
pour
évoquer
le
diagnostic.
La
découverte
d’un
cas
devrait
mener
à
effectuer
une
enquête
fami-
liale
afin
de
dépister
d’autres
membres
affectés.
Ces
patients
nécessitent
un
suivi
spécialisé
et
rapproché
afin
de
desceller
à
temps
la
survenue
d’une
complication.
En
effet,
le
pronostic
à
court
et
long
terme
dépendra
certainement
de
l’application
des
moyens
thérapeutiques
adaptés
et
modernes
allant
du
traitement
médicamenteux
de
l’insuffisance
cardiaque
au
défibrillateur
automatique
implantable,
voire
la
transplantation
cardiaque.
Pour
améliorer
la
prise
en
charge
des
patients,
les
cardio-
logues
africains
doivent
s’informer
sur
la
nouvelle
classification
des
cardiomyopathies
et
se
former
aux
nouvelles
techniques
d’imagerie
médicale.
Déclaration
d’intérêts
Les
auteurs
déclarent
ne
pas
avoir
de
conflits
d’intérêts
en
relation
avec
cet
article.
Références
[1]
Sasse
Klassen
S,
Gerull
B,
Oechslin
E,
Jenni
R,
Thierfelder
L.
Isolaled
noncompaction
of
left
ventricular
myocardium
in
the
adult
is
an
auto-
somal
dominant
disorder
in
the
majority
of
patients.
Am
J
Med
Genet
2003;119:162–7.
[2]
Ishida
F,
Tsubata
S,
Bowles
KR,
Haneda
N,
Uese
K,
Miyawaki
T.
Novel
gene
mutations
in
patients
with
left
ventricular
noncompaction
or
Barth
syndrome.
Circulation
2001;103:1256–63.
[3]
Matsuda
M,
Tsukahara
M,
Kondoh
O,
Mito
H.
Familial
isolated
noncom-
paction
of
left
ventricular
myocardium.
J
Hum
Genet
1999;44:126–8.
[4]
Kherbaoui-Redouani
L,
Eschard
C,
Bednarek
N,
et
al.
Aplasie
cutanée
congénitale,
défaut
de
compaction
du
ventricule
gauche
et
troubles
du
rythme
cardiaques
graves
:
un
nouveau
cas
de
syndrome
MLS
(microph-
talmia
with
linear
skin
defects).
Arch
Pediatr
2003;10:224–6.
[5]
Weiford
BC,
Subbarao
VD,
Mulhern
KM.
Non-compaction
of
the
ventri-
cular
myocardium.
Circulation
2004;109:2965–71.
[6]
Thuny
F,
Philip
E,
Caucino
K,
et
al.
Non-compaction
isolée
du
ventricule
gauche.
Arch
Mal
Cœur
Vaiss
2003;96:339–43.
[7]
Jenni
R,
Oechslin
E,
Schneider
J,
et
al.
Echocardiographic
and
pathoana-
tomical
characteristics
of
isolated
left
ventricular
non-compaction:
a
step
towards
classification
as
a
distinct
cardiomyopathy.
Heart
2001;86:666–71.
[8]
Duncan
RF,
Brown
MA,
Worthley
SG.
Increasing
identification
of
isolated
left
ventricular
non-compaction
with
cardiovascular
magnetic
resonance:
a
mini
case
series
highlighting
variable
clinical
presentation.
Heart
Lung
Circ
2008;17(1):9–13.
[9]
Paule
P,
Bræm
L,
Mioulet
D,
et
al.
La
non
compaction
du
ventricule
gauche,
une
cardiomyopathie
du
sujet
jeune
:
premières
observations
africaines.
Med
Trop
2007;67:587–93.
[10]
Oechsline
E,
Attenhoefer
Jost
CH,
Rojas
JR,
et
al.
Long-term
follow-
up
of
34
adults
with
isolated
left
ventricular
noncompaction:
a
distinct
cardiomyopathy
with
poor
prognosis.
J
Am
Coll
Cardiol
2000;36:
493–500.
1
/
4
100%