Partie 2/2 : Du mécanisme à la loi de vitesse

!"#$%&'()*)+),-.#/%01(0)'-#.&%2//(30))))))))))4!567)
)
8)
!9:46;<=)*)+),=!:>65,=5)<=:!;6?>>=@5)
Partie'2/2':'Du'mécanisme'à'la'loi'de'vitesse'
)
Dans% les% exemples% ci-après,% les% indices% «%t%»% ne% seront% pas% toujours% indiqués% pour% alléger% l’écriture.% Mais% les%
concentrations%dépendent%toujours%du%temps%a%priori.%
'
A/()'-#.&%2/)0()B-'2C3()(/)D-/-'#3)(/)$3C0%(C'0)#.&(0)-3-1(/&#%'(0E):F%/)B().21$'(/B'()3(0)'-#.&%2/0)."%1%GC(0)H(&)
$2CI2%') %/F3C(') 0C') 3(C') B-'2C3(1(/&JK) 2/) ."('."() L) établir' leur' mécanismeK) .M(0&) L) B%'() L) B-&('1%/(') 3(0) #.&(0)
-3-1(/&#%'(0)0C..(00%F0)GC%).21$20(/&)3#)'-#.&%2/E))
42C') valider' le' mécanisme)$'2$20-) $2C') C/() '-#.&%2/K) %3) F#C&) GC() .(3C%N.%) $('1(&&() B() '(/B'() .21$&() B(0)
.#'#.&-'%0&%GC(0)2O0('I-(0)$2C').(&&()'-#.&%2/)+)0-3(.&%I%&-K)%/F3C(/.()BC)023I#/&P)(&)loi'de'vitesseE))
63) F#C&) B2/.) comparer' la' loi' de' vitesse' théorique,' déduite' du' mécanisme' proposé,' à' celle' obtenue'
expérimentalement'(cf'chapitre'10).)5%)(33(0).2/.2'B(/&K)#32'0)3()1-.#/%01()$'2$20-)(0&)possibleE))
)
@M2OQ(.&%F)B().()$#'#D'#$"()(0&)BM(R$'%1(')3#)32%)B()I%&(00()#&&(/BC()$2C')C/()'-#.&%2/)L)$#'&%')B()02/)1-.#/%01(E))
)
Par%exemple,%comment%retrouver%la%loi%de%vitesse%expérimentale%v(t)%=%k[NO2]2%de%la%réaction%%
NO2(g)%+%CO(g)%
à
%NO(g)%+%CO2(g)%
Connaissant%son%mécanisme%:%
2%NO2(g)%
à
%NO3(g)%+%NO(g)% %
NO3(g)%+%CO(g)%
à
%NO2(g)%+%CO2(g)% ?%
)
6E)=S4<=556?>)T=) @:)U6;=55=) T=)V?<,:;6?>) TMA>=) =54=!=) :44:<:655:>;)T:>5)
4@A56=A<5):!;=5)=@=,=>;:6<=5)
)
Exemple%:%Dans%le%même%bécher%ont%lieu%les%réactions%:%%
%% % % %
Comment.exprimer.la.vitesse.volumique.de.formation.de.A.?..
Nous%cherchons%à%exprimer%la%vitesse%volumique%de%formation%de%A,%le%volume%du%réacteur%étant%considéré%constant,%%
soit%:% E) La% variation% de% la% concentration%de% A% est% due% aux% trois% réactions%:% A% disparaît% dans% les%
réactions%(1)%et%(3)%et%apparaît%dans%la%réaction%(2).)
On%a%donc%:%
ϑ
f,A(t)=d[A]t
dt =d[A]t
dt
!
"
#$
%
&
réaction1
+d[A]t
dt
!
"
#$
%
&
réaction2
+d[A]t
dt
!
"
#$
%
&
réaction3
)
?'K)par%définition,%la%vitesse%volumique%de%la%réaction%i%s’écrit%:))
ϑ
i(t)=1
ν
A,i
d[A]t
dt
!
"
#$
%
&
réaction)i
%donc%%%%
d[A]t
dt
!
"
#$
%
&
réaction)i
=
ν
A,i⋅
ϑ
i(t)
)
(1) 2A k1
! →! 2B+C
(2) D+3E k2
! →! A
(3) 3A+F k3
! →! G+2H
#
$
%
&
%
ϑ
f,A(t)=d A
[ ]
t
dt

!"#$%&'()*)+),-.#/%01(0)'-#.&%2//(30))))))))))4!567)
)
W)
Par%exemple%: )B2/.) %
On%en%déduit%donc%:% E%
'Généralisation)+)42C')C/()(0$X.():)%/&('I(/#/&)B#/0)$3C0%(C'0)'-#.&%2/0)#Y#/&)3%(C)B#/0)3()1Z1()'-#.&(C')
H$#') (R(1$3() B#/0) $3C0%(C'0) #.&(0) -3-1(/&#%'(0) BMC/) 1Z1() 1-.#/%01(JK) 3#) I%&(00() I23C1%GC() B() F2'1#&%2/) B() :)
0M-.'%'#)+) 2[) (0&)3#)I%&(00()I23C1%GC()B()3#)'-#.&%2/)%)(&) 3().2(FF%.%(/&)0&\."%21-&'%GC()
#3D-O'%GC()B():)B#/0).(&&()'-#.&%2/E))
'
Exemple%:%Pour%ce%mécanisme%en%deux%actes%élémentaires%:%%
(1)%2%NO2(g)%
à
%NO3(g)%+%NO(g)%%
(2)%NO3(g)%+%CO(g)%
à
%NO2(g)%+%CO2(g)%
Exprimer%la%vitesse%de%formation%de%NO2.%
)
)
)
)
66E)@?6)T=)U6;=55=)TMA>):!;=)=@=,=>;:6<=)
'
Propriété':'A/)#.&()-3-1(/&#%'()admet'toujours'un'ordre)(&)0C%&)3#)loi'de'Van’t'Hoff'+))
42C')C/)#.&()-3-1(/&#%'(K)3(0)2'B'(0)$#'&%(30)02/&)-D#CR)#CR).2(FF%.%(/&0)0&\."%21-&'%GC(0))
H(&)3M2'B'()D32O#3)(0&)B2/.)-D#3)L)3#)123-.C3#'%&-JE'
Exemple%:%Exprimer%la%loi%de%vitesse%des%actes%élémentaires%(1)%et%(2)%du%mécanisme%ci-dessus.%)
)
)
)
)
)
)
)
)
)
)
=&)(/0C%&()])>2C0)."('."2/0)L)(R$'%1(')3#)32%)B()I%&(00()B().(&&()'-#.&%2/E)TM#$'X0)3M-GC#&%2/)O%3#/K)2/)#)H$#')
(R(1$3(J)+))
! " # $ %&'( )
%" # *!+" $ !(,"-)
@(0)B(CR)#.&(0)-3-1(/&#%'(0)0C%I#/&)3#)32%)B()U#/M&)92FFK)2/)#)B2/.)+))
! " # $ %&'( )
%" # *.+&'(($ .(/&'01/2'1)
)
>?7)(0&) C/) intermédiaire' réactionnel'+) 2/) /() .2/&'^3() $#0) 0#) .2/.(/&'#&%2/E) !(&&() 32%) B() I%&(00() /M(0&) $#0)
#..($&#O3()+)%3)F#C&)."('."(')L)3#)12B%F%('E)?/)I#)#32'0)F#%'()#$$(3)L)B(0)approximations.)
ϑ
1(t)=−1
2(
d A
[ ]
t
dt )réaction)1
(
d A
[ ]
t
dt )réaction 1 =−2.
ϑ
1(t)
ϑ
f,A(t)=d A
[ ]
t
dt =−2.
ϑ
1(t)+
ϑ
2(t)−3.
ϑ
3(t)
ϑ
f,A(t)=
ν
i.
i
∑
ϑ
i(t)
ϑ
i(t)
ν
i

!"#$%&'()*)+),-.#/%01(0)'-#.&%2//(30))))))))))4!567)
)
7)
666E):44<?S6,:;6?>)T=5)=;:;5)_A:56)5;:;6?>>:6<=5)H:=_5J)
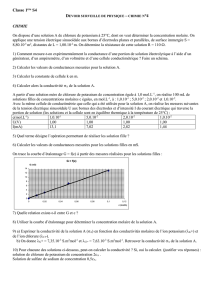
=&CB%2/0)3#)&'#/0F2'1#&%2/)B():)(/)!)H`%3#/)+):à!J)0(32/)3()1-.#/%01()0C%I#/&)+)%
)
!() 1-.#/%01() F#%&) #$$#'#a&'() un' intermédiaire' réactionnel' BE) =/) '-023I#/&K) L) 3M#%B() B() 4Y&"2/K) 3(0) -GC#&%2/0)
B%FF-'(/&%(33(0)B2/&)02/&)023C&%2/0)3(0).2/.(/&'#&%2/0)b:c&K)b`c&)(&)b!c&K)2/)$(C&)&'#.(')b:c&K)b`c&)(&)b!c&)(/)F2/.&%2/)BC)
&(1$0E))
4#'#1X&'(0)+))
• b:cd)e)dK8)123E@N8)f)b`cd)e)b!cd)e)d)
• !2C'O()#)+)g8)e)h)1%/N8)f)gW)e)8)1%/N8)
• !2C'O()O)+)g8)e)8)1%/N8)f)gW)e)id)1%/N8)
)))))))))))))) )
Cas.a...........Cas.b.
5C')3#).2C'O()H#JK)2/))'(1#'GC()GC()3M%/&('1-B%#%'()
'-#.&%2//(3)`)(0&)F2'1-K)$C%0).2/0211-E)
T#/0)3().#0)HOJK)`)(0&)formé'difficilement)H.2/0&#/&()B()
I%&(00()F#%O3()$2C')3#)$'(1%X'()'-#.&%2/K).(33()GC%)F2'1()`J)(&)
consommé'facilement)H.2/0&#/&()B()I%&(00()O(#C.2C$)$3C0)
D'#/B()$2C')3#)B(CR%X1()'-#.&%2/K).(33()GC%).2/0211()`JE))
?/)'(1#'GC()#32'0)GC()0#).2/.(/&'#&%2/)reste'très'faible)H`)
(0&).2/0211-)BX0)GCM%3)(0&)F2'1-J)(&)constante)+) E))
?/)B%&)GC()`)(0&)dans'un'état'quasi-stationnaire.)
)
)
'Approximation'des'états'quasi-stationnaires'(AEQS)':''
5%) C/) %ntermédiaire' réactionnel)6<) (0&) formé' difficilement)H$#') C/() '-#.&%2/) BM-/('D%() BM#.&%I#&%2/) -3(I-(J) (&)
consommé'facilement)H$#')C/()'-#.&%2/)BM-/('D%()BM#.&%I#&%2/)F#%O3(J)#32'0)2/)$(C&).2/0%B-'(')GC()3#).2/.(/&'#&%2/)
B()6<)reste'constante*')H6<)(0&).2/0211-)#C00%&^&)GCM%3)(0&)F2'1-K)%3)(0&)B#/0)un'état'quasi'stationnaireJ)+))
345 6
36 # 7'
)
*%Ceci%n’est%pas%vrai%au%tout%début%de%la%réaction,%il%faut%une%courte%période%d’induction%pour%que%s’établisse%cet%état%
quasi-stationnaire.%
.
.
Ak1
! →! B
Bk2
!→!C
d[B]
dt =0

!"#$%&'()*)+),-.#/%01(0)'-#.&%2//(30))))))))))4!567)
)
h)
Exercice.d’application%:%Etablir%la%loi%de%vitesse%de%la%réaction%d’hydrobromation%du%propène.%
Bilan.:. %
Mécanisme.:.Ce%mécanisme%fait%apparaître%un%intermédiaire%réactionnel%qui%est%un%carbocation%(encadré).%Il%sera%noté%C+.%%
)
Remarque%:%On%note%sur%chaque%flèche%la%constante%de%vitesse%associée%à%l’acte%élémentaire%considéré.%
)
1) !"2%R)B()3#)B-F%/%&%2/)B()! " 8)
?/)."('."()L)(R$'%1(')3#)I%&(00()B()3#)'-#.&%2/K)GC%)$(C&)0M(R$'%1(')B(0)F#j2/0)0C%I#/&(0)HBM#$'X0)3()O%3#/)B()3#)'-#.&%2/J)+))
2C)O%(/)+) )2C)O%(/)+)) )
Attention':''
@(0) &'2%0) (R$'(00%2/0) 2O&(/C(0) /() 02/&) $#0) -GC%I#3(/&(0) #) $'%2'%)+) B#/0) C/) 1-.#/%01() F#%0#/&) #$$#'#a&'() B(0) %/&('1-B%#%'(0)
'-#.&%2//(30K) 3#) B-F%/%&%2/) B() 3#) I%&(00() B() '-#.&%2/) /M(0&) $#0) F2'.-1(/&) C/%I2GC(E) =/) D-/-'#3K) #$'X0) C&%3%0#&%2/) B(0)
#$$'2R%1#&%2/0K).(0)(R$'(00%2/0)0M-D#3%0(/&E),#%0).()/M(0&)$#0)&2CQ2C'0)3().#0E))
):&&(/&%2/)L)O%(/)0C%I'()3(0)%/B%.#&%2/0)B()3M-/2/.-)+)0%)2/)."('."()k)3#)32%)B()I%&(00()B()3#)'-#.&%2/)lK)2/)$2C''#)."2%0%')
n’importe' quelle' définition)H!2/0(%3)+) (/) D-/-'#3K) 3() $3C0) 0%1$3()(0&) B() ."2%0%') 3#) I%&(00() B() F2'1#&%2/) B(0) $'2BC%&0JE)5M%3) (0&)
B(1#/B-)k)3#)I%&(00()B()F2'1#&%2/)B()S)l)2C)k)3#)I%&(00()B()B%0$#'%&%2/)B()m)lK)'(0$(.&(')3#).2/0%D/(E)
.
)
) )
H2C CH CH3HBr H3C CH CH3
Br
Propène Bromopropane
H2C CH CH3HBr H3C CH CH3
H3C CH CH3
Br
Br H3C CH CH3
Br
k1
k-1
k2
ϑ
(t)= + d[bromopropane]
dt
ϑ
(t)=−d[propène]
dt
ϑ
(t)=−d[HBr]
dt

!"#$%&'()*)+),-.#/%01(0)'-#.&%2//(30))))))))))4!567)
)
i)
6UE):44<?S6,:;6?>)T=)@M=;:4=)!6>=;6_A=,=>;)T=;=<,6>:>;=):=!T)
)
1. Mécanisme'par'stade'
)
63)(R%0&() $3C0%(C'0) &Y$(0) B() 1-.#/%01(0E) ;2C&(0) 3(0) '-#.&%2/0) #C) $'2D'#11()B() ."%1%() 2'D#/%GC()0C%I(/&) C/)
1-.#/%01()$#')0&#B(0E)
)
T#/0)C/)1-.#/%01()par'stadesK)3()$#00#D()B(0)'-#.&%F0)#CR)$'2BC%&0)0()F#%&)$#')C/()0C..(00%2/)BM#.&(0)-3-1(/&#%'(0)
H.2/0%B-'-0)'(/I('0#O3(0)2C)/2/J)0()B-'2C3#/&)&2CQ2C'0)B#/0)3()1Z1()2'B'()+))
H8J)<à)6<8)f))HWJ)6<8à6<W)f))H7J)6<Wà6<7)f)P)f)H/J)6</N8à4)
@(0)%/&('1-B%#%'(0)'-#.&%2//(30)02/&)F2'1-0)#C).2C'0)BMC/)#.&()-3-1(/&#%'(K)$C%0)%''-1-B%#O3(1(/&).2/0211-0)#C)
.2C'0)B()3M#.&()-3-1(/&#%'()0C%I#/&E))
)
Exemples%de%mécanismes%par%stade%:%Le%mécanisme%de%la%page%précédente,%le%mécanisme%de%SN1…%
)
!211(/&)I-'%F%(')GCMC/)1-.#/%01()(0&)O%(/)$#')0&#B(0)]))
U-'%F%(') GCM#C.C/) %/&('1-B%#%'() '-#.&%2//(3) /M(0&) F2'1-K) .2/0211-) puis' régénéré' dans' un' acte' élémentaire'
suivant.''
)
2. Approximation'de'l’étape'cinétiquement'déterminante'
=&CB%2/0)3#)&'#/0F2'1#&%2/)B():)(/)T)H`%3#/)+):àTJ)0(32/)3()1-.#/%01()0C%I#/&)+)%
)
?/)#)B-&('1%/-)3(0)I%&(00(0)I8H&JK)IWH&J)(&)I7H&J)#C).2C'0)BC)&(1$0)$2C')+))
• b:cd)e)dK8)123E@N8)
• !#0)#)+)g8)e)h)1%/N8)f)gW)e)8)1%/N8)f)g7)e)W)1%/N8)
• !#0)O)+)g8)e)8)1%/N8)f)gW)e)dKd8)1%/N8)f)g7)e)W)1%/N8)
• !#0).)+)g8)e)dKd8)1%/N8)f)gW)e)8)1%/N8)f)g7)e)W)1%/N8)
)
T#/0)3().#0)H#JK)3(0)I%&(00(0)I8)K)IW)(&)I7)02/&)B%FF-'(/&(0)L)&2C&)%/0&#/&)H(33(0)/M2/&)$#0)B()'#%02/)BMZ&'()-D#3(0)nJE)
?/)'(1#'GC()GC()B#/0)3().#0)HOJK)I7)e)IW)L)&2C&)%/0&#/&)+)3M-&#$()W)#)%1$20-)0#)I%&(00()L)3M-&#$()7E)@(0).2/0&#/&(0)B()
I%&(00()12/&'(/&)GC()B#/0).().#0)3M-&#$()W)(0&)O(#C.2C$)$3C0)3(/&()GC()3(0)#C&'(0)-&#$(0E)
T#/0)3().#0)H.JK)I7)e)IWe)I8)L)&2C&)%/0&#/&)+)3M-&#$()8)#)%1$20-)0#)I%&(00()L)&2C&(0)3(0)-&#$(0)0C%I#/&(0E)?/)'(1#'GC()
.(&&()F2%0N.%)GC()3M-&#$()8)(0&)O(#C.2C$)$3C0)3(/&()GC()3(0)-&#$(0)W)(&)7E)
Ak1
! →! B
Bk2
!→!C
Ck3
! →! D
'
t(min)'
0'
0,5'
1'
1,5'
2'
2,5'
3'
4'
Cas'a'
(mol.L-1.min-1)
'
v1(t)
'
hKdE8dN8)
iKhE8dNW)
*K7E8dN7)
oKoE8dNh)
8K7E8dNh)
8KpE8dNi)
WKiE8dNq)
hKiE8dNp)
v2(t)
'
d)
qK7E8dNW)
hK*E8dNW)
WKoE8dNW)
8KpE8dNW)
8K8E8dNW)
qKqE8dN7)
WKhE8dN7)
v3(t)
'
d)
7KWE8dNW)
hKqE8dNW)
7KoE8dNW)
WKoE8dNW)
8KoE8dNW)
8KWE8dNW)
WKhE8dNW)
Cas'b'
(mol.L-1.min-1)
'
v1(t)
'
WKi)
oK7E8dNq)
7KiE8dN88)
8K7E8dN8q)
rd)
rd)
rd)
rd)
v2(t)
'
d)
qK7E8dNW)
7KpE8dNW)
WK7E8dNW)
8KhE8dNW)
pKqE8dNW)
iKWE8dN7)
WKdE8dN7)
v3(t)
'
d)
qK7E8dNW)
7KpE8dNW)
WK7E8dNW)
8KhE8dNW)
pKqE8dNW)
iKWE8dN7)
WKdE8dN7)
Cas'c'
(mol.L-1.min-1)
'
v1(t)
'
8KdE8dN8)
qK8E8dNW)
7K*E8dNW)
WKWE8dNW)
8KhE8dNW)
pK7E8dN7)
iKdE8dN7)
8KoE8dN7)
v2(t)
'
d)
qK7E8dNW)
7K*E8dNW)
WK7E8dNW)
8KhE8dNW)
pKiE8dN7)
iKWE8dN7)
8KoE8dN7)
v3(t)
'
d)
qK7E8dNW)
7K*E8dNW)
WK7E8dNW)
8KhE8dNW)
pKiE8dN7)
iKWE8dN7)
8KoE8dN7)
 6
6
 7
7
 8
8
1
/
8
100%