chapitre x : alcanes et alcools

Page 1 sur 9
CHAPITRE X : ALCANES ET ALCOOLS
INTRODUCTION
D’après : Cours de chimie organique de P.Arnaud aux éditions Gauthier-Villars
La tradition a maintenu la division de la chimie en deux disciplines : chimie organique et chimie minérale… La
chimie organique c’est la chimie des composés du carbone, alors que la chimie minérale s’étend à l’étude de
tous les autres éléments chimiques et leurs combinaisons (à quelques exceptions près comme CO, CO2, CO32-
,…).
« Contrairement à ce que l’on pourrait penser de prime abord, le domaine de la chimie minérale est beaucoup
moins vaste que celui de la chimie organique. En effet, le carbone peut se lier à lui-même de façon presque
indéfinie, pour former des enchaînements extrêmement variés, et il suffit de quelques éléments (le plus
souvent H, O et N seulement) pour former avec lui des centaines de milliers de molécules… »
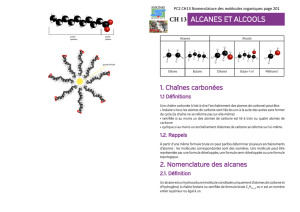
On appelle chaîne carbonée ou squelette carboné l'enchaînement des atomes de carbone constituant une
molécule organique. La formule topologique permet de bien visualiser ce «squelette».
Exemple :
Nous étudierons dans ce cours quelques unes des propriétés de deux familles de composés organiques : les
alcanes et les alcools.
I) LES DIFFERENTS TYPES DE CHAINES CARBONEES
I-1) Chaîne ouverte-Chaîne cyclique
Compléter le tableau ci-dessous :
Chaîne ouverte
Chaîne cyclique
Nom
pentane
cyclopentane
Formule brute
Formule développée
Formule semi-développée
Formule topologique

Page 2 sur 9
I-2) Chaîne linéaire-Chaîne ramifiée
Compléter le tableau ci-dessous :
Chaîne linéaire
Chaîne ramifiée
Définition
Les atomes de carbone sont les uns à
la suite des autres
La chaîne carbonée comporte au
moins une ramification
Nom
butan-1-ol
2-méthylpropan-1-ol
Formule brute
Formule développée
Formule semi-développée
Formule topologique
II) LES ALCANES
II-1) Qu’est-ce qu’un alcane ?
Les alcanes sont des hydrocarbures* exclusivement constitués de liaisons simples C—C et C—H.
*une molécule d’hydrocarbure ne contient que les éléments C et H
N.B. Les alcanes existent en grande quantité sous forme de gisements naturels de gaz ou de pétrole. L’origine
de ces gisements est généralement attribuée à la fermentation de la cellulose des végétaux des temps
préhistoriques, sous l’action des bactéries.
La formule brute d’un alcane à chaîne ouverte comportant n atomes de carbone est : CnH2n+2
La formule brute d’un alcane à chaîne cyclique comportant n atomes de carbone est CnH2n
Exemples : voir § I-1
II-2) Nomenclature des alcanes
La nomenclature des alcanes sert de base à celle de tous les composés de la chimie organique, elle doit donc
être bien maîtrisée.
II-2-1) Les alcanes à chaine linéaire
Le nom des alcanes s’obtient en ajoutant la terminaison –ane à un préfixe d’origine grecque indiquant le
nombre d’atomes de carbone. Les quatre premiers termes ont conservé des noms consacrés par l’usage et
n’appartiennent pas à un système logique.

Page 3 sur 9
Compléter le tableau suivant :
Nombre
d’atomes
de
carbone
préfixe
Nom de l’alcane
Formule
brute
Formule semi développée
1
méth-
2
éth-
3
prop-
4
but-
5
pent-
6
hex-
7
hept-
8
oct-
9
non-
10
déc-
II-2-2) Les alcanes à chaine ramifiée
Comment nommer les ramifications ? Nom des groupes alkyles
En enlevant (par la pensée) un atome d’hydrogène à un alcane on obtient un groupe d’atomes nommé groupe
alkyle. Un groupe alkyle se nomme en remplaçant la terminaison –ane de l’alcane par le suffixe –yle
nom du groupe
alkyle
formule semi-développée
méthyle
éthyle
propyle
isopropyle

Page 4 sur 9
Comment nommer les alcanes à chaîne ramifiée
Un alcane à chaîne ramifiée se nomme en faisant précéder le nom de l’alcane correspondant à la chaîne la plus
longue (nommée chaîne principale) du nom des groupe alkyle correspondant aux ramifications (avec élision de
la lettre e ). On place devant ces noms, en les séparant par un tiret, un nombre indiquant la position du groupe
alkyle sur la chaîne principale numérotée à partir de l’une des ses extrémités. Le sens de numérotation de la
chaîne principale doit être choisi de telle façon que la somme des numéros contenus dans le nom de
l’hydrocarbure soit aussi faible que possible.
Si la chaîne principale porte plusieurs ramifications, on indique le nom des groupes alkyles par ordre
alphabétique.
Si plusieurs ramifications sont identiques on utilise les préfixes di, tri, tétra, …..
Exemples :
Exercice 1
Consulter les fichiers « 1S-Alcanes-Nom-FSD.html » et « 1S-Alcanes.html » et répondez aux questions
suivantes :
1. Nommer les alcanes suivants (virgule entre les nombres, tiret entre un nombre et un nom) :
…………………………………………….. ……………………………………………………
2. Représenter la formule semi-développée et la formule topologique du 3-éthyl-3,4-diméthylhexane.

Page 5 sur 9
II-2-3) Les alcanes cycliques
Le nom d’un alcane cyclique est déduit du nom de l’alcane linéaire correspondant en faisant précéder son nom
du préfixe cyclo.
Exercice 2
1. Donner les formules brutes, semi-développées et topologiques du cyclohexane.
III) LES ALCOOLS
D’après : Cours de chimie organique de P.Arnaud aux éditions Gauthier-Villars
et Wikipédia
Les alcools existent parfois à l’état naturel dans certaines essences végétales. Les alcools peuvent être produits
par fermentation alcoolique, notamment le méthanol à partir du bois et l'éthanol à partir des fruits et des
céréales. L'industrie n'y a recours que dans le cas de l'éthanol pour produire du combustible et des boissons.
Dans les autres cas, les alcools sont synthétisés à partir des composés organiques tirés du gaz naturel ou du
pétrole.
III-1) Formule générale des alcools
La formule d’un alcool dérive de celle d’un hydrocarbure par remplacement d’un atome d’hydrogène par le
groupe caractéristique hydroxyle –OH.
Exemple : L’éthanol de formule générale C2H5—OH résulte du remplacement d’un atome d’hydrogène de
l’éthane C2H6 par un groupe hydroxyle –OH.
III-2) Nomenclature des alcools
Un alcool est nommé en remplaçant le –e final du nom de l’alcane dont il dérive par le suffixe –ol. Ce suffixe est
si nécessaire précédé du numéro de l’atome de carbone porteur du groupe caractéristique hydroxyle –OH. La
chaîne carbonée principale doit obligatoirement contenir le groupe hydroxyle –OH et doit être numérotée de
telle sorte que l’atome de carbone porteur de –OH ait le numéro le plus petit possible.
Exemple :
 6
6
 7
7
 8
8
 9
9
1
/
9
100%