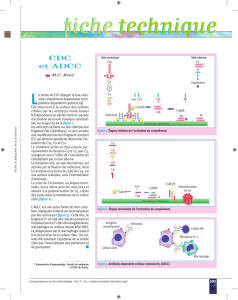
VII. Les autres rôles du complément

Pascal Chaumont
Mélanie Le Hô
31/02/11
Immunologie-Guerric EPRON , [email protected]
Un poly noir&blanc était disponible en amphi. Un poly en couleur sera disponible à la corpo et on espère (pour les
feignants) sur le site des frappes en fichier zip avec le cours.
Le complément
I. Définition du complément
A. Découverte
Le complément a été découvert en 1895 par Jules Bordet de l’Institut Pasteur (Nobel 1919).
L’expérience réalisée est la suivante : il injecte à un lapin une bactérie, l’animal produit alors des
anticorps retrouvés dans son sang. On récupère alors son sérum et on le place in vitro sur une
colonie de bactéries et on remarque que ce sérum tue la bactérie en question.
Le sérum immun est donc bactéricide c'est-à-dire qu’il peut tuer les bactéries.
Mais, si on refait la même expérience avec le sérum immun chauffé les bactéries survivent. Or
on sait que les anticorps sont résistants à la chaleur donc ils n’agissent pas seuls, un élément
thermolabile supplémentaire est nécessaire pour obtenir la réaction immunitaire.
Si on utilise un sérum non-immun, les bactéries survivent donc les anticorps sont
indispensables.
Enfin, si ajoute le sérum immun chauffé et le sérum non-immun, il y a destruction des
bactéries donc élément thermolabile + Anticorps = bactéricide
C’est ainsi que l’on met en évidence l’alexine nommée plus tard le complément. L’alexine est
un élément thermolabile (sensible à la chaleur) du sérum, non spécifique de l’antigène,
capable de « complémenter » les anticorps pour éliminer les bactéries. Pour la lyse bactérienne, il
faut deux choses :
- les anticorps anti-bactériens spécifiquement formés lors de l’immunisation
- une substance thermolabile présente en permanence dans le sérum, l’alexine.
Ce système du complément forme une branche de l’immunité innée.
B. Composition
Le complément est un ensemble de plus de 30 à 35 protéines dont des protéines :
-plasmatiques (5% des protéines sériques)
-de surface cellulaire.
Ces Protéines sont produites par :
– Foie (très majoritairement à l’état basal) surtout les hépatocytes
– Macrophages (production utile dans les organes lymphoïdes secondaires) ( moins important en
quantité mais le plus important).

– Épithéliums muqueux et fibroblastes (faible)
Le complément est inactif dans le sérum à l’état basal. Ces zymogènes (substances
inactives) nécessitent des clivages en cascade qui leur confèrent leurs activités enzymatiques. Il
existe deux types d’activateurs du complément :
complexes immuns = association Ag-Ac (Ac-dépendant et donc de l’antigène également)
sucres associés aux pathogènes par exemple associés aux bactéries (Ac-indépendant)
Il y a 3 voies biochimiques qui activent le complément :
– classique (via Ac)
des lectines (sans Ac et dépendant de sucres)
alterne (sans Ac)
La Finalité du complément est d’assurer la mort mécanique du pathogène :
-directement : par rupture membranaire et choc osmotique
-indirectement : par opsonisation (c’est à dire en entourant le pathogène d’éléments, marqueurs)
pour faciliter sa reconnaissance par le système immunitaire et donc sa phagocytose . Ceci est
important chez les Gram+ chez qui le CAM (complexe d’attaque membranaire cf plus loin) ne peut
se former du fait de la paroi.
II. Nomenclature
Fragments de clivage enzymatique : lettre minuscule « C4a ou b »
Molécule inactive : désignée par i « C3bi ou iC3b »
Formes enzymatiques actives : recouvertes d’une barre horizontale « ».
III. Les voies d’activation
A. La voie classique
Elle nécessite absolument des anticorps.
IgG IgM
La C1 estérase est la première protéine qui agit dans la voie classique d'activation du complément.
Elle est formée de 3 sous unités : C1q, C1r, C1s. Les sérine-protéases C1r et C1s sont activées. La
C1 estérase est calcium dépendante.

La présence d’anticorps spécifiques indique que la réaction contre l’antigène est déjà initiée et qu’il
y a eu reconnaissance du pathogène. C’est la formation du complexe Ag/Ac qui permet l’initiation
de la voie classique du complément.
La C1 estérase se fixe à la partie Fc de complexes immuns, c'est-à-dire à la partie
constante des immunoglobulines du complexe Ag/Ac. C’est la sous-unité C1q qui reconnait l’Ac.
L’activation peut se faire par :
- des complexes immuns à IgM pentamérique (3 sites pour C1)
- des complexes immuns à IgG (1 site pour C1 et donc plusieurs IgG nécessaires).
On a ainsi besoin de plus Ig G pour obtenir la même efficacité qu’un Ig M. Les IgM sont donc 1000
fois plus efficaces que les IgG pour activer C1 (passage d’une forme plane à une forme en agrafe ).
1.activation
- Reconnaissance d’un pathogène par un anticorps spécifique
- Fixation de la partie C1q à l’activateur (anticorps, IgM naturelles …) et donc au complexe
immun
- Cela entraîne un changement conformationnel de la protéine C1
- D’où une activation autocatalytique du proenzyme C1r en (qui devient donc efficace et
fonctionnel)
- convertit C1s en par clivage
- clive C4 en C4a + C4b
- C4b s’ancre dans la membrane cible via son groupement thioester R-S-CO-R’, C4a est
circulant
- Puis liaison du proenzyme C2 à C4b avec formation du complexe C4bC2
- clive ensuite C2 en C2a + C2b
- Transformation du complexe C4bC2 en complexe C4bC2a (Mg2+ dépendante) (+C2b)
- On aboutit au complexe = C3 convertase « classique » qui clive C3 en C3a + C3b
(C3b expose un thioester et s’ancre dans la membrane cible, C3a est circulant).
Groupement thioesterdŽvoilŽ permet
ancrage membranaire
covalent

2.Régulation
C1-inh(dŽtache C1r et C1s du complexe)
L’activation de la voie classique est soumise à différents régulateurs.
Le contrôle de la C1-estérase se fait par la C1-inhibiteur ou C1-inh qui :
- empêche l’activation de C1r en phase liquide. C1r est associé à C1s et C1q, si ce
complexe n’est pas préalablement attaché à un anticorps, il n’y a pas d’activation de
C1r.
- peut inactiver le C1r activé.
La lyse de C3 et C4 libère les ponts thioester de C3b et C4b qui sont hyper-réactifs,
instables. Le pont thioester est hydrolysé en quelques minutes par l’eau s’il n’est pas fixé
rapidement sur la membrane cible de manière covalente. Cela oblige ainsi C3b et C4b à se
lier à la membrane directement à proximité de l’enzyme et les empêchent de diffuser loin de
la cellule cible.
Un complexe instable subit une dissociation spontanée.
Il existe également un contrôle de l’assemblage de la C3 convertase ou :
- C4-bp (binding protein) inhibe l’association C4b/C2
- CD55 = DAF « facteur d’accélération de la dégradation » entraîne la dissociation
C4/C2 (utile pour la protection de l’hôte)
- CR1 (récepteur pour le complément de type 1) ou C3b-R peut titrer le C3-b
- Facteur I : clive C3b en iC3b (c’est un inactivateur de C3b)
Ces dernières protéines limitent l'action du complément sur les cellules autologues afin d'éviter la
destruction de nos propres cellules (par fixation d’auto-anticorps sur nos cellules).
B.La voie des lectines : Ficoline et MBL
La voie des lectines est anticorps indépendante. Son activation se fait via la Mannose Binding
Lectine (MBL) et la Ficoline reconnaissant tous 2 des sucres spécifiques des pathogènes. Nos
propres sucres ne sont pas reconnus.
C’est un mécanisme analogue à la C1 estérase.
Les molécules effectrices de la voie des lectines sont les MBL-Associated Serine Proteases =
MASP (analogues à C1r/s).

1.Activation
- Une bactérie porte un sucre spécifique
- MBL ou Ficoline associés à MASP se fixent sur les sucres cibles
- Les MASP sont clivées, réarrangées et autoactivées (Ca 2+ dépendant).
Le reste des événements suit le même déroulement que la voie classique :
- MASP2 clive C4 en C4a + C4b (ancré dans la membrane via son thioester)
- Puis liaison du proenzyme C2 à C4b (formation du complexe C4bC2)
- MASP2 clive ensuite C2 en C2a + C2b
- Transformation du complexe C4bC2 en complexe C4bC2a (+C2b)
- On aboutit au complexe = C3 convertase qui clive C3 en C3a + C3b (ancré dans la
membrane).
• MASP1 pourrait cliver directement C3 en C3a + C3b
• MASP3 (splicing alternatif de MASP1) : rôle encore flou
• On utilise surtout MASP2
2.Régulation
C3b doit se fixer à un groupe hydroxyle (-OH) de son voisinage immédiat (présent sur un sucre ou
une protéine membranaire de la bactérie). Si il y a absence de fixation, une molécule d’H2O fixe
C3b ce qui empêche sa liaison à une membrane cellulaire. Le but de cette manœuvre est d’éviter
l’accumulation de C3b actif qui pourrait être délétère pour l’hôte (même mécanisme que pour le
C3b issu de la voie classique).
En outre, MBL a une forte affinité pour les sucres
bactériens (levures, virus) :
– Mannose
– N-acétyl-glycosamine
– Fucose
Mais MBL est peu affine pour les sucres de
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%