1. Effets moléculaires

Feat.Sovietik
PAT – Glucocorticoides 1/8
GLUCOCORTICOIDES
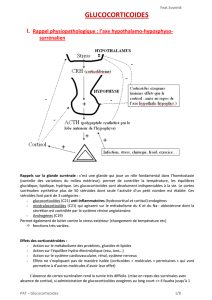
I. Rappel physiopathologique : l’axe hypothalamo-hyposphyso-
surrénalien
Rappels sur la glande surrénale : c’est une glande qui joue un rôle fondamental dans l’homéostasie
(contrôle des variations du milieu extérieur), permet de contrôler la température, les équilibres
glucidique, lipidique, hydrique. Les glucocorticoïdes sont absolument indispensables à la vie. Le cortex
surrénalien synthétise plus de 50 stéroïdes dont seule l’activité d’un petit nombre est établie. Ces
stéroïdes font parti de 3 catégories :
- glucocorticoïdes (C21) anti-inflammatoires (hydrocortisol et cortisol) endogènes
- minéralocorticoïdes (C21) qui agissent sur le métabolisme du K et du Na : aldostérone dont la
sécrétion est contrôlée par le système rénine angiotensine.
- Androgènes (C19)
Permet également de lutter contre le stress extérieur (changement de température etc)
fonctions très variées.
Effets des corticostéroïdes :
- Action sur le métabolisme des protéines, glucides et lipides
- Action sur l’équilibre hydro-électrolytique (eau, ions…)
- Action sur le système cardiovasculaire, rénal, système nerveux
- Effets ne s’expliquant pas de manière isolée (corticoïdes = molécules « permissives » qui vont
permettre à d’autres molécules d’avoir leur effet)
L’absence de cortex surrénalien rend la survie très difficile. (mise en repos des surrénales avec
absence de cortisol, si administration de glucocorticoïdes exogènes au long court => il faudra jusqu'à 1

PAT – Glucocorticoides 2/8
an pour que la production de cortisol se rétablisse) La régulation de la synthèse de glucocorticoïdes est
contrôlée par la sécrétion d’ACTH qui est un polypeptide synthétisé dans l’hypophyse antérieure.
L’ACTH est elle même régulée par rétrocontrôle négatif par le cortisol (qui régule aussi la libération de
CRH) et par rétrocontrôle positif par la CRH (corticotrophin releasing hormone ou corticolibérine)
d’origine hypothalamique. Enfin, une augmentation de sécrétion d’ACTH est possible sous l’influence de
facteurs extérieurs comme : stress, infection, chirurgie, froid, exercice physique.
Le glucocorticoïde exogène a le même effet sur le rétrocontrôle négatif que le cortisol endogène =>
mise au repos des glandes surrénaliennes
Les effets indésirables d’une corticothérapie sont donc notamment une diminution de sécrétion
d’ACTH et de CRH (= freination de l’axe hypothalamo-hypophyso-surrénalien). Leur sécrétion est longue
à se réactiver lors de l’arrêt du traitement, ce qui induit une insuffisance surrénalienne pendant un
certain temps. Un protocole d’arrêt vise à éviter cette insuffisance à l’arrêt du traitement.
La sécrétion des minéralocorticoïdes quant à elle, n’est pas sous contrôle de l’ACTH mais du
système rénine angiotensine.
La glande surrénale suit un rythme circadien : la production d’ACTH n’est pas homogène au cours
de la journée, il existe des pics dont le maximum est à 6h du matin et le minimum à minuit → alternance
veille/sommeil
Le pic d’ACTH entraîne un pic de cortisol ; il est donc nécessaire, lors d’un traitement de mimer ce pic →
prise le matin (voire double prise)
On privilégiera toujours un corticostéroïde dont la durée d’action est longue.
II. Effets pharmacologiques
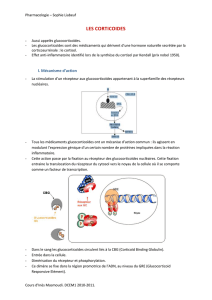
1. Effets moléculaires
Le récepteur aux glucocorticoïdes est un récepteur nucléaire GR (liaison cytosolique mais
translocation vers le noyau) qui agit comme un facteur de transcription : la liaison va entraîner une
augmentation ou une diminution de la transcription des gènes :
- Dimérisation du récepteur et activation du gène
- Fixation sur un autre élément de réponse qui va inhiber la synthèse de protéines
- Le récepteur va se fixer sur un facteur de transcription et inhibe la synthèse de protéines
Il y a environ 600 protéines (1% des protéines totales) dont la transcription est régulée par les
glucocorticoïdes. De plus, les glucocorticoïdes ont de nombreux effets non-génomiques et ont une
action permissive, c’est à dire qu’ils permettent l’action d’autres protéines.
Les glucocorticoïdes ont une action sur de nombreux tissus différents. Il existe des réactions
croisées : possibilité d’avoir en plus des effets sur les récepteurs aux minéralocorticoïdes, à forte dose, à
l’origine d’effets indésirables. A l’inverse, la progestérone est un antagoniste compétitif des récepteurs
aux glucocorticoïdes → résistance aux corticoïdes en fin de grossesse ; peut expliquer l’ostéoporose post
ménopausique aussi (pas de progestérone protectrice).
Il existe un nombre variable de récepteurs aux glucocorticoïdes selon les tissus
→ réponses variables en fonction des tissus. On observe également une diminution de la sensibilité des
récepteurs en vieillissant.
Il existe des variations de sensibilité des récepteurs selon le type cellulaire, ex : sur les LT, les réponses
aux glucocorticoïdes sont plus sensibles que sur les LB, alors que le nombre de récepteur est le même.
2. Effets indépendants du récepteur
Non spécifiques

PAT – Glucocorticoides 3/8
3. Effets métaboliques et cellulaires
Métabolisme glucidique : une exposition prolongée peut conduire à une exagération des effets
pseudodiabétogènes (↑ glycémie et insulinorésistance). Stimulation formation de glucose, diminution
utilisation périphérique et augmentation du stockage
Métabolisme protidique : inhibition de l’incorporation des acides aminés dans les muscles, ↑ relargage
d’acides aminés par le muscle faiblesse musculaire
Métabolisme lipidique : redistribution du tissus adipeux, ↑ lipolyse augmentation des dépôts
graisseux dans la face et le cou, diminution dans les jambes = répartition centripète facio-tronculaire.
Cellules sanguines :
Hématies : ↑ concentration de l’hémoglobine et ↑ hématocrite
Leucocytes : du nombre de leucocytes : environ de 70% des lymphocytes circulants et
de 90% des monocytes circulants (pendant 24 h si administration unique), non dû à une
destruction mais à une redistribution
↑ polynulcléaires dû à une ↑ de leur production
Monocytes : du pouvoir bactéricide, fongicide ; de la phagocytose.
Résistance à l’action des cytokines pro inflammatoires qui vont les stimuler.
Altération du chimiotactisme
Inhibition de la fixation des Ig et de la fraction C3b du complément
anti-inflammatoire + immunosuppresseur
Lymphocytes : LT > LB dû à la sensibilité différente des sous populations de
Récepteurs
4. Effets anti-inflammatoires
Effet très large : les glucocorticoïdes peuvent inhiber l’inflammation due à des causes mécaniques,
chimiques, infectieuses, immunologiques. Il s’agit d’un traitement symptomatique, c’est quand même
un traitement d’intérêt, on peut sauver des gens avec ce genre de traitement. Les glucocorticoïdes
agissent sur les 3 phases de l’inflammation :
- Phase aiguë : action sur la perméabilité capillaire et sur l’œdème
- Phase subaiguë : action sur la migration leucocytaire et l’activité phagocytaire
- Réaction retardée, phase chronique : action sur la croissance des fibroblastes, des capillaires,
sur la cicatrisation (inhibition)
-
Inconvénients : peut masquer des signes cliniques qui pourraient être nécessaires au diagnostic d’une
autre pathologie.
Les mécanismes des effets anti-inflammatoires des glucocorticoïdes ne sont pas tous connus.
Au niveau cellulaire, il s’agirait d’une inhibition de l’arrivée des monocytes et des macrophages
au site de l’inflammation ainsi que d’une inhibition de la synthèse des facteurs de l’inflammation (PG,
cytokines, molécules d’adhésion…) et d’une inhibition de la sensibilité à ces facteurs. Au niveau
moléculaire : inhibition de la synthèse d’acide arachidonique via la synthèse de lipocortine I qui
empêche l’interaction de la PLA2 avec les phospholipides membranaires.
Il y a aussi inhibition de la synthèse de COX-2, mécanisme NFB dépendant.
5. Effet immunosuppresseur :

PAT – Glucocorticoides 4/8
Il est dû à leur action commune sur les globules blancs + sur l’inhibition de la sécrétion de cytokines. Les
glucocorticoïdes ne diminuent pas de façon significative les concentrations en anticorps (les
lymphocytes restent immunocompétents), ils ont une action sur la phase cellulaire mais pas sur la
réponse humorale. C’est surtout les voies de communications entre les cellules qui sont concernées.
Altération de l’immunité des cellules NK, diminution de l’expression des cellules du CMH, altération des
fonctions cytotoxiques des LT, diminution des cytokines, augmentation de l’apoptose des LB.
III. Pharmacocinétique
Absorption :
Le cortisol et ses analogues sont efficaces per os.
Possibilité de les utiliser en IV (rapide), IM (prolongé) ou dans le liquide synovial
Il existe une forte utilisation des glucocorticoïdes en application locale, peau, yeux. (Attention ! Il y a
aussi des effets systémiques possible en application locale, si le traitement est long ou sur une grande
zone !)
Distribution :
90% liés aux protéines plasmatiques de façon réversible sur des protéines spécifiques comme la CBG
(Cortisol Binding Globulin) (= transportine) ou non spécifiques comme l’albumine. Les corticoïdes
exogènes peuvent avoir une fixation différente.
Possibilité de compétition avec les oestrogènes.
Métabolisme : Hépatique (transformation en produit inactif), par réduction de la liaison 2-3. Donne des
composés inactifs.
Elimination : Rénale
La durée d’action des glucocorticoïdes à activité moyenne ou longue dépend de leur demi-vie biologique
malgré une demi-vie plasmatique courte. Il existe 3 familles de glucocorticoïdes selon leur durée
d’action (t ½ biologique) :
- t1/2 courte (8 à 12h) : cortisol, cortisone
- t1/2 moyenne (18 à 36h) : prednisolone, prednisone, triamcinolone
- t1/2 longue (36 à 54h) : bétaméthasone
-
En cas d’hypoalbuminémie, il y a + de fraction libre donc plus d’effets indésirables. Idem en cas
d’insuffisance hépatique.
IV. Effets indésirables
1. Insuffisance surrénalienne aigue :
C’est comme un syndrome de sevrage à l’arrêt : fièvre, douleur musculaire, articulaire, malaises, états
anxieux et agités… Ils existent de moins en moins car il y a des protocoles d’arrêt progressifs dans le cas
de traitements longs qui ont arrêté l’axe hypothalamo-hypophysaire. Le retour à la normale peut
prendre jusqu’à 9 mois.
L’idéal est de faire une supplémentation en cortisol.
2. Effets secondaires a long terme :
accidents digestifs (inhibitions PG => risques ulcérogènes, risques de perforation de l’estomac et
du duodénum)

PAT – Glucocorticoides 5/8
effets neuropsychiques : troubles du comportement, nervosité, insomnie, changements
d’humeur, psychoses maniaco-dépressives, augmentation du risque suicidaire
Effets métaboliques :
troubles de la balance sodique et hydrique dus à la composante minéralocorticoïde (réactions
croisées), avec rétention d’eau, de sel, et hypokaliémie => prise de poids avec oedèmes, risques
HTA, troubles rénaux contre indication si troubles rénaux ou cardiovasculaires prééxistants.
=> régime désodé ou appauvri en sel et enrichi en calcium
Risque d’hyperglycémie :
Ce risque est peu fréquent mais peut poser problème chez les personnes diabétiques ou à
antécédents diabétiques et chez les obèses. Il n’y a cependant pas de contre-indication chez les
diabétiques malgré cet effet diabétogène. Par contre, il faut adapter le traitement et l’associer à un
régime (↓ des sucres d’absorption rapide). L’insuline pourra être utilisée dans les cas graves.
Atteinte musculaire :
Elle peut conduire à une myopathie. Touche principalement les membres inférieurs (pouvant
empêcher la marche dans certains cas). Il faut alors mettre en place un régime hyperprotidique.
Atteinte de la croissance :
Touche surtout les enfants. Il peut y avoir blocage complet de la croissance ou simplement un retard
de croissance. Cet EI concerne surtout les thérapies supérieures à 6 mois.
Ostéoporose :
Elle est due à un catabolisme accru de l’os par une augmentation de l’activité des ostéoclastes, une
dépression de l’activité des ostéoblastes, une diminution de l’absorption intestinale du calcium et
une augmentation de son élimination urinaire. Tout ceci conduit à l’augmentation du syndrome
ostéoporotique.
Mesures hygiéno-diététiques : apport de calcium et de vitamine D.
Une ostéoporose préexistante peut être une contre-indication à la corticothérapie.
L’ensemble des effets métaboliques des glucocorticoïdes ressemble au Syndrome de Cushing ou
hypercorticisme. Il est caractérisé par une « bosse de bison » (amas de graisse dû à la répartition
centripète des graisses), un faciès lunaire avec acné, hirsutisme, ecchymoses et vergetures.
3. Risque infectieux :
Ce risque existe pour tout type de pathogène. Il s’explique par le fait que les glucocorticoïdes
sont des immunosuppresseurs. Ils favorisent donc la survenue d’infection et masquent leurs signes
cliniques. Il faut donc écarter tout risque d’infection avant de commencer le traitement. S’il y a
infection, elle peut être traitée en même temps.
Dans les cas graves (tuberculose), des radiographies de contrôle sont réalisées pour prévenir la rechute. Il faut
vérifier si le patient a des antécédents de tuberculose. En cas de risque, un traitement prophylactique par la rifampicine est
mis en place en même temps que les glucocorticoïdes.
4. Risque oculaire :
Les glucocorticoïdes augmentent la pression intraoculaire. Ils augmentent donc le risque de glaucome
ou aggravent un glaucome préexistant. Un risque de cataracte est présent.
Conséquence : examen ophtalmique fréquent avec arrêt du traitement si nécessaire.
5. Interactions médicamenteuses
 6
6
 7
7
 8
8
1
/
8
100%