Activité documentaire et expérimentale N°1 (C5) Comprendre la

Activité documentaire et expérimentale N°1 (C5)
Comprendre la formation des molécules à partir des atomes
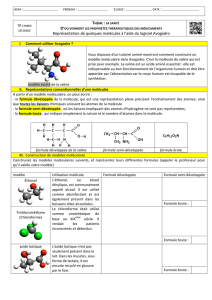
La représentation ci-dessous de molécules composant des médicaments s’appellent la formule semi-développée
d’une espèce chimique, un trait correspondant à une liaison covalente entre deux atomes (sauf pour H) :
OHNHC
O
CH3
H3CN
O N
O
CH3
N
CH3
N
Paracétamol Caféine Acide acétylsalicylique (aspirine)
a) Propose la formule brute (exemple : l’eau H20) de l’acide acétylsalicylique (aspirine) : ………………………………………………
b) Quelle information apporte la formule semi-développée par rapport à la formule brute ? ………………………………………
…………………………………………………………………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………………………………………………………………
c) A partir des zones entourées sur les formules semi-développées ci-dessus, indique le nombre de liaisons
covalentes (représentées par des traits, sauf pour H) qu’établit un type d’atome (C, O, N, H) avec d’autres atomes :
Atome
Carbone C
Oxygène O
Azote N
Hydrogène H
Nombre de liaisons
covalentes
d) Il existe aussi la formule développée. D’après toi, quelle différence y-a-t-il avec la formule semi-développée ?
…………………………………………………………………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………………………………………………………………
e) Pour comprendre le nombre de liaisons covalentes que peut former un atome avec d’autres atomes, complète le
tableau ci-dessous concernant les atomes les plus courants composant les molécules des médicaments :
Atome
Hydrogène
H
Carbone
C
Oxygène
O
Chlore
Cl
Soufre
S
Azote
N
Numéro atomique
Z = 1
Z = 6
Z = 8
Z = 17
Z = 16
Z = 7
Structure électronique
Nombre d’électrons externes
(de valence)
Nombre d’électrons à
acquérir pour respecter la
règle du duet ou la règle de
l’octet (voir C3)
Représentation des atomes
avec leurs électrons externes
(avec un point par électron réparti
sur chaque côté du symbole)
Enchaînement possible
des liaisons covalentes
Pour obtenir le ou les électrons qui lui manquent afin de respecter la règle du duet ou de l’octet qui lui confère
plus de stabilité, un atome va pouvoir établir des liaisons covalentes avec d’autres atomes et former une molécule.
Pour former une liaison covalente, un atome va mettre en commun un électron avec un autre atome :
A · · B, ce qui revient à A B

f) Pour chaque molécule vue au collège, complète le tableau suivant. Construis-les avec le modèle compact puis
éclaté ou avec un logiciel 3D (voir feuille méthode).
RAPPEL : blanc
hydrogène / noir
carbone / rouge
oxygène / bleu
azote / vert
chlore.
Formule brute : H2O
Nom de la molécule : ……………………………………………………………
Composition atomique : ………………………………………………………
……………………………………………………………………………………………………
Représentation en modèle compact et éclaté :
Formule développée :
Formule brute : CO2
Nom de la molécule : ……………………………………………………………
Composition atomique : ………………………………………………………
……………………………………………………………………………………………………
Représentation en modèle compact et éclaté :
Formule développée :
Formule brute : H2
Nom de la molécule : ……………………………………………………………
Composition atomique : ………………………………………………………
……………………………………………………………………………………………………
Représentation en modèle compact et éclaté :
Formule développée :
Formule brute : O2
Nom de la molécule : ……………………………………………………………
Composition atomique : ………………………………………………………
……………………………………………………………………………………………………
Représentation en modèle compact et éclaté :
Formule développée :
Formule brute : N2
Nom de la molécule : ……………………………………………………………
Composition atomique : ………………………………………………………
……………………………………………………………………………………………………
Représentation en modèle compact et éclaté :
Formule développée :
Formule brute : CH4
Nom de la molécule : méthane (gaz de ville)
Composition atomique : ………………………………………………………
……………………………………………………………………………………………………
Représentation en modèle compact et éclaté :
Formule développée :
Quelle information apporte le modèle éclaté par rapport au modèle compact ? …………………………………………………………………
…………………………………………………………………………………………………………………………………………………………………………………………………………………
g) Construis et visualise les molécules du f) avec un logiciel (voir feuille méthode). A partir du fichier « propan-1-
ol.s3d », propose la formule développée, puis semi-développée et brute du propan-1-ol (solvant en pharmacologie).
Formule développée : Formule semi-développée : Formule brute :
h) Le chloral, de formule brute C2OCl3H sert à synthétiser l'hydrate de chloral, utilisé comme sédatif, hypnotique
ou analgésique. Propose la formule développée de la molécule de chloral et vérifie avec le fichier « chloral.s3d ».
1
/
2
100%