Ici

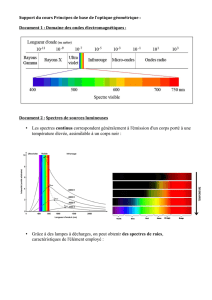
I]
Par analogie entre l’interaction gravitationnelle et l’interaction électrostatique, on décrivait au
début du XXème siècle le mouvement des électrons autour du noyau à l’image du mouvement
des planètes autour du soleil.
2e
n
e/N
2TS
T/S
r
qq
kF
r
MM
GF
eq
eZq
e
n
II] Notion de photon :
Dans le cas de la mécanique quantique on peut décrire la lumière soit comme une onde soit
comme un photon (corpuscule). A une onde électromagnétique monochromatique de
fréquence
correspond à un photon de masse nul, de charge électrique nul et d’énergie
hC
hE
où h est appelé constante de Planck,
s.J10.62,6h 3
.
Exercice :
On considère un photon d’énergie 4eV, calculer la longueur d’onde de l’onde
électromagnétique associée.
J10.41,6eV4E 19
On sait que
C
hE
.
Donc
nm310
10.41,6
10.0,310.62,6
E
hC 19
83
III] Diagramme des niveaux d’énergie d’un atome :
Niveau d’énergie de l’atome
2
E
1
E
0
E
Etat Fondamental
Premier état exité
Emission d’un photon
hEE 02
hEE 01
Chapitre P10 : Quantification de l’énergie d’un atome

Lorsqu’un atome passe d’un état excité d’énergie
1
E
vers un état de plus basse énergie
0
E
, il
émet un photon d’énergie
hC
hEE 01
.
Lorsqu’on excite une population d’atome, les atomes passent de l’état fondamental
0
E
à des
états d’énergies bien définies (quantifiés)
.E,E,E 321
L’état de plus grande énergie est obtenue lorsque l’atome est ionisé, l’appelle état ionisé.
Lorsqu’un atome passe de l’état fondamental d’énergie
0
E
à l’état d’énergie
1
E
, en
absorbant un photon d’énergie
hEE 01
on parle d’absorption d’un photon.
Niveau d’énergie de l’atome
2
E
1
E
0
E
Etat Fondamental
Premier état exité
Absorption d’un photon
hEE 02
hEE 01
1
/
2
100%