Titre du chapitre - Raymond Rodriguez SVTperso

RR - 17/04/17 - 840908859 - 1/8
L’ATP et la vie
cellulaire
I. L'ATP est une plaque tournante de la vie des cellules
A. L'ATP existe chez tous les êtres vivants
B. L'ATP est nécessaire aux synthèses à partir de molécules organiques préexistantes
►TP 1. Contraction musculaire et ATP
C. L'ATP est nécessaire aux mouvements cellulaires comme la contraction musculaire
►TP 2. Respiration, fermentation et production d’ATP
II. Respiration et fermentation sont deux sources d’ATP
A. Dans le hyaloplasme, la glycolyse permet une production limitée d'ATP
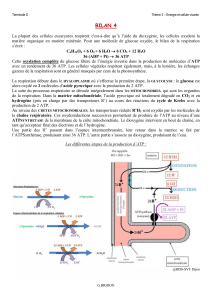
B. Au cours de la respiration l'oxydation complète des métabolites libère de l’ATP
C. Une fermentation correspond à une simple oxydation des composés réduits issus de la glycolyse
OBJECTIF
De l'Adénosine TriPhosphate est produite pendant la phase
photochimique de la photosynthèse puis immédiatement utilisée lors de la
phase non photochimique. C’est pourtant une molécule indispensable à
l’activité de toutes les cellules.
On cherche à préciser le rôle de l'ATP et les mécanismes qui
permettent, aux autotrophes et aux hétérotrophes, d'ajuster en
permanence leur production d'ATP en fonction de leurs besoins.
I. L'ATP est une plaque tournante de la vie des cellules
► FIGURE 1. ATP, ADP et Pi dans Nathan p. 36 fig. 1.
A. L'ATP existe chez tous les êtres vivants
Quel que soit l'organisme, autotrophe ou hétérotrophe, l'énergie chimique est le
plus souvent transmise par l'intermédiaire de l'adénosine triphosphate ou ATP.
On appelle adénosine, l'association d'une adénine (= une base azotée), avec un
ribose (= un ose). Sur cet ensemble peuvent venir se fixer, l'une derrière l'autre,
jusqu'à trois molécules d'acide phosphorique (H3 PO4).
Spécialité
Chapitre
1.3
3 semaines

RR - 17/04/17 - 840908859 - 2/8
À pH cellulaire l'acide phosphorique (H3 PO4) est dissocié en protons (2 H+) et en
phosphate inorganique H PO42- que l'on note Pi. Il en résulte que l'ATP est lui même
dissocié en ATP4-. La présence de ces quatre charges négatives alignées, qui sans cesse
se repoussent (identité de charges) puis se rapprochent (du fait des liaisons covalentes),
entraîne un "stress" électrique qui déstabilise la molécule.
D'autres ribonucléotides comme GTP (guanosine TP) ou UTP (uridine TP) peuvent,
dans certaines réactions, jouer un rôle analogue à celui de l'ATP.
À la différence des ribonucléotides, qui sont stables (dans l'ARN), la présence de
trois groupements phosphates rend la molécule très instable. Elle est alors
facilement hydrolysée en adénosine diphosphate (ADP) et en phosphate
inorganique (Pi) tout en restituant son énergie de liaison. Inversement la
réaction de synthèse, ou phosphorylation, est facile mais consomme de
l'énergie. Ainsi, l'énergie qui a servi à la synthèse d'ATP est très facilement
restituée par hydrolyse, c'est pour cela que l'on dit que l'ATP est une molécule à
haut pouvoir de transfert énergétique.
ATP + H2 O = ADP + Pi - 30,9 kJ (si pH 7 et 37°C)
Le signe "moins" indique la perte d'énergie libre du substrat (
G0(T)) c'est à dire le
caractère exergonique de la réaction. La valeur est donnée pour une température T
donnée en K.
Par habitude, il est fréquent de ne pas indiquer l'eau dans cette réaction. On écrit
alors simplement : ATP = ADP + Pi
Du fait de son instabilité, cette molécule, indispensable en permanence, est
impossible à stocker ou même à transporter d’une cellule à une autre. Pourtant la
quantité d'ATP intracellulaire est constante, quelle que soit sa consommation.
Chaque cellule doit donc en produire en permanence en fonction de ses propres
besoins (turn over).
L'ATP est tellement instable qu'en une seconde, toute l'ATP d'une cellule est hydrolysée.
En fait la vitesse de phosphorylation est égale à la vitesse d'hydrolyse. Ainsi un Homme
adulte produit et hydrolyse chaque jour environ 40 kg d'ATP. Lors d'un effort physique
intense, la vitesse d'utilisation d'ATP peut atteindre 0,5 kg par minute.
B. L'ATP est nécessaire aux synthèses à partir de molécules
organiques préexistantes
On appelle anabolisme l'ensemble des réactions métaboliques permettant la
synthèse de molécules organiques.
Dans tous les types cellulaires (autotrophes ou hétérotrophes) la plupart des
molécules biologiques sont des macromolécules formées de l'association de sous
unités moléculaires (polymères).
- La polymérisation des acides aminés permet de former des protéines (liaison
peptidique).
- Celle des oses permet de produire des glucides (saccharose, amidon...).
- La fixation des acides gras sur le glycérol (ou un autre alcool) permet de
former des lipides.
- La polymérisation des nucléotides permet de produire des acides nucléiques.
R1 O H R2
| || | |
AAR1 + AAR2 NH2― C ― C ― N ― C ― COOH + H2 O
| |
ATP ADP + Pi H H Liaison peptidique

RR - 17/04/17 - 840908859 - 3/8
Toutes ces réactions de biosynthèse sont des réactions de condensation avec
élimination d'eau. Or elles se réalisent dans le milieu intracellulaire aqueux, et ne
peuvent donc se produire spontanément même avec l'intervention d'enzymes. La
cellule doit dépenser de l'énergie pour les réaliser. La seule source d'énergie
utilisable est l'hydrolyse d'ATP qui sert d’intermédiaire du métabolisme
général, intervenant dans de nombreuses réactions et dans tous les types de
cellules (autotrophes ou hétérotrophes).
La formation d'une liaison C=C nécessite par exemple un apport de 350 kJ par mole.
►TP 1. Contraction musculaire et ATP
C. L'ATP est nécessaire aux mouvements cellulaires comme la
contraction musculaire
► FIGURE 2. Du muscle à la myofibrille (dans Bordas p. 218 commentaire
dans TP 1 doc. 2.
► FIGURE 3. Ultrastructure du muscle strié squelettique dans TP 1 doc. 1 et
Bordas p. 219, 220, 221.
Un muscle squelettique est constitué de fibres musculaires qui sont de grandes
cellules plurinucléées formées de myofibrilles allongées, elles mêmes
constituées d'une succession de sarcomères qui sont les unités fonctionnelles du
muscle.
Chaque sarcomère est formé de deux types de filaments protéiques
longitudinaux.
- Les filaments épais (Ø 15 nm) sont des polymères de myosine. C'est une
molécule formée de deux chaînes polypeptidiques qui se terminent chacune par
une tête globulaire. Chaque filament épais est formé de deux "bouquets"
molécules de myosine tête bêche.
- Les filaments fins (Ø 5 nm) sont des polymères d'actine, qui forme deux
chaînes de molécules globulaires enroulées en hélice.
► FIGURE 4. Contraction musculaire à l’échelle moléculaire dans Bordas
1983 p. 254.
Au cours de la contraction le muscle se raccourcit proportionnellement au
raccourcissement de chaque sarcomère. Les filaments d'actine et de myosine ne
changent pas de longueur mais glissent les uns par rapport aux autres (seule la
bande I diminue) selon un mécanisme cyclique et grâce à l'hydrolyse de l'ATP.
► FIGURE 5. Interaction actine-myosine.
ATTENTION : le schéma Nathan p. 35 est confus.
► SCHEMA COURS. Interaction actine-myosine d’après figure 5.
Les têtes de myosine ont une activité enzymatique ATPasique. Cependant
l’ADP reste lié de façon non covalente à la tête de myosine ce qui empêche une
nouvelle hydrolyse (pas de séparation enzyme-produits donc occupation du site
actif). La tropomyosine est une protéine qui, associée à l'actine, empêche tout contact entre
l'actine et la myosine en masquant les sites d'attachement entre les deux molécules. Le
potentiel d'action provoque la sortie de Ca2+ du réticulum endoplasmique. Ca2+ permet
le déplacement de la tropomyosine ce qui démasque les sites d'attachement actine-
myosine.
L'ordre de contraction (potentiel d'action), démasque les sites d'attachement
actine myosine. Il y a fixation actine-myosine.
L'attachement actine myosine provoque une modification de conformation qui
entraîne successivement :

RR - 17/04/17 - 840908859 - 4/8
- la libération de l'ADP par la myosine ;
- le pivotement de la tête de myosine et donc un glissement actine-myosine,
c'est à dire un raccourcissement.
En cas de "panne d'ATP" le mécanisme reste bloqué à ce niveau (rigidité cadavérique).
Une nouvelle molécule d'ATP se fixe sur la tête de myosine ce qui provoque
le détachement entre actine et myosine. Il y a alors retour à l'étape
.
Lors de la contraction musculaire, une déformation moléculaire est à l'origine
d'un raccourcissement à l'échelle cellulaire (en fait le sarcomère) qui, à son tour,
provoque un raccourcissement à l'échelle de l'organe (le muscle squelettique) et
un mouvement à l'échelle de l'organisme. Ce n'est pas le cas des mouvements
intracellulaires d'organites. La cyclose des chloroplastes, ou la migration des
chromosomes lors d'une division cellulaire ne sont visibles qu'à l'échelle
cellulaire et ne provoquent pas de mouvement à l'échelle de l'organisme. Pourtant
ils consomment aussi de l'ATP.
Les mouvements de cyclose sont liés à la présence dans le cytoplasme des cellules
végétales de filaments d’actine et de myosine qui glissent l'un par rapport à l'autre grâce
à de l'ATP.
►TP 2. Respiration, fermentation et production d’ATP
II. Respiration et fermentation sont deux sources d’ATP
A. Dans le hyaloplasme, la glycolyse permet une production limitée
d'ATP
► FIGURE 8a. ATP et glycolyse
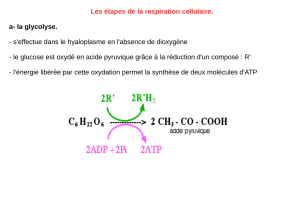
La glycolyse est une première étape commune à la respiration et à la
fermentation. C’est un enchaînement de dix réactions chimiques enzymatiques
qui se produisent dans le hyaloplasme (= cytosol). Globalement elle permet
l'oxydation partielle (par déshydrogénation) d'une molécule de glucose en deux
molécules d’acide pyruvique :
C6 H12 O6
2 CH3 CO COOH + 4 H+ + 4 e- - énergie libre
À pH cellulaire, l'acide pyruvique (CH3 CO COOH) est dissocié en pyruvate
(CH3 CO COO-) en libérant un proton (H+).
La glycolyse a deux conséquences.
Les e- (et les H+) sont pris en charge par des coenzymes oxydées R',
accepteurs d'électrons proches des composés R de la photosynthèse, qui passent à
l'état réduit R'H2.
2 R' + 4 e- + 4 H+
2 R' H2
L'énergie libérée par l'oxydation du glucose en pyruvate permet la synthèse de
2 moles d'ATP par mole de glucose oxydée
2 ADP + 2 Pi
2 ATP + 2 H2 O
La réaction globale de la glycolyse peut donc s'écrire :
C6 H12 O6 + 2 R' 2 C H3 CO COOH + 2 R'H2
2 ADP + 2 Pi 2 ATP

RR - 17/04/17 - 840908859 - 5/8
Dans une cellule, la quantité de coenzyme R' est faible. Pour que la glycolyse
puisse de poursuivre il est nécessaire de les régénérer, c'est à dire de réoxyder les
coenzymes R'H2 en leur fournissant un accepteur final d'e- et d'H+. C'est ce
mécanisme qui différencie fondamentalement respiration et fermentation.
Le glucose est le métabolite le plus fréquemment dégradé. Cependant, en fonction
de l'équipement enzymatique de la cellule, d'autres métabolites, autres sucres, acides
aminés, acides gras ou alcools, peuvent être dégradés.
B. Au cours de la respiration l'oxydation complète des métabolites
libère de l’ATP
La respiration est un phénomène cellulaire à ne pas confondre avec la ventilation
(inspiration et expiration).
► FIGURE 6. Organisation structurale d’une mitochondrie dans Nathan p. 43.
► SCHEMA COURS. Ultrastructure de la mitochondrie d’après figure 6.
Les réactions chimiques spécifiques de la respiration ont lieu dans des organites
cellulaires spécialisés : les mitochondries. Elles sont de petite taille (quelques
micromètres), et sont délimités par une double membrane qui entoure le
matrice. La membrane interne forme des replis appelés crêtes mitochondriales
(recouvertes de sphères pédonculées = ATP synthases).
► FIGURE 7. Mitochondries et production d’ATP dans Nathan p. 42.
► FIGURE 8b. ATP et respiration.
► SCHEMA COURS. Respiration d’après figure 8b (construit progressivement)
1. Dans le matrice mitochondriale le pyruvate est entièrement oxydé
La double membrane mitochondriale est perméable à l'acide pyruvique qui est
alors soumis à l'équipement enzymatique de la matrice, ce qui permet l'oxydation
complète de l'acide pyruvique en dioxyde de carbone (série de
décarboxylations). Cela entraîne la formation de nombreuses nouvelles molécules
de coenzymes réduites (R'H2) et d’ATP.
2 CH3 CO COOH + 6 H2 O 6 CO2 + 20 e- + 20 H+ - énergie libre
10 R' + 20 e- + 20 H+ 10 R'H2
2 ADP + Pi 2 ATP
Soit globalement :
C'est en fait un enchaînement cyclique de neuf réactions chimiques connu sous le nom
de cycle de Krebs ou cycle de l'acide citrique.
Deux familles d'enzymes sont nécessaires à cet ensemble de réactions :
- des décarboxylases qui permettent la libération du CO2 à partir du substrat ;
- des déshydrogénases qui permettent la libération d'H+ du substrat, et donc celle
d'e-.
2 C H3 CO COOH + 10 R' + 6 H2 O 6 CO2 + 10 R' H2
2 ADP + 2 Pi 2ATP
 6
6
 7
7
 8
8
1
/
8
100%