histologie speciale

1
HISTOLOGIE SPECIALE
• TABLE DES MATIÈRES
1. APP. DIGESTIF: CAVITÉ BUCCALE
2. APP. DIGESTIF: OESOPHAGE, ESTOMAC
3. APP. DIGESTIF: INTESTINS
4. FOIE ET PANCREAS
5. APPAREIL URINAIRE, 1ère PARTIE
6. APPAREIL URINAIRE, 2ème PARTIE
7. APPAREIL GENITAL MASCULIN
8. APPAREIL GENITAL FEMININ
9. APPAREIL RESPIRATOIRE
10. SYSTÈME IMMUNITAIRE
11. GLANDES ENDOCRINES
HISTOLOGIE DE L’APPAREIL DIGESTIF (1)
•
•
L
LA
A
C
CA
AV
VI
IT
TE
E
B
BU
UC
CC
CA
AL
LE
E
– INDEX
• 1) Introduction générale
• 2) Introduction, cavité buccale
• 3) Lèvre
• 4) Dent
• 5) Langue
• 6) Glandes salivaires
APP DIGESTIF: INTRODUCTION
• Le rôle essentiel de l’appareil digestif consiste à morceler les substances nutritives de manière à
faciliter leur absorption dans le corps. Ce processus comporte cinq phases caractéristiques des
différentes régions de l’appareil digestif.
• L’ingestion et le morcellement se font dans la cavité buccale. Le bol alimentaire convoyé à
l’œsophage, est facilité par la sécrétion de la salive provenant des glandes salivaires.
• L’œsophage transporte les aliments à l’estomac où le processus de morcellement s’achève et où
commence la digestion. Cette dernière associée à la contraction intense de la paroi gastrique,
réduit le contenu gastrique en un liquide à demi digéré appelé le chyme.
Le chyme est projeté à travers le pylore dans la première partie de l’intestin grêle, le duodénum, où
sont déversés les produit de sécrétion de deux glandes annexes, le pancréas et le foie.
Dans l’intestin grêle se termine la digestion et se fait la majeure partie de l’absorption. Les résidus
liquidiens non absorbés passent dans le gros intestin, ou colon, par la valvule iléo-coecale, où ils se
solidifient. La portion terminale du gros intestin, le rectum est le lieu de rétention des fèces avant la
défécation qui se fait par le canal anal.
CAVITÉ BUCCALE - INTRODUCTION
• La digestion commence dans la cavité buccale où se font l’ingestion, la fragmentation et
l’humidification des aliments. Les principales structures de la cavité buccale, les lèvres, dents,
langue, muqueuse buccale participent à toutes ces fonctions, en association avec les glandes
salivaires.

2
LEVRE
• La coupe sagittale au faible grossissement montre le revêtement de surface labial qui sur le versant
externe, est cutanée avec ses annexes, laissant place à un épithélium malpighien kératinisé au
niveau du vermillon, qui fait la transition avec la muqueuse, également malpighienne, non
kératinisée, buccale. Le tissu conjonctif fibro-vasculaire de support, enveloppe des sections de
fibres musculaires (muscle orbiculaire), et héberge dans le versant muqueux des glandes
salivaires accessoires.
DENT
• Le schéma d’une section sagittale d’une dent en place, et passant par la lèvre, montre les deux
parties qui la constituent :
• -la couronne qui se projette dans la cavité buccale, recouverte et protégée par une couche trés
minéralisée, l’émail.
• -la racine qui s’insère dans l’os alvéolaire du maxillaire.
• La majeure partie de la dent est formée par de l’ivoire ou dentine, tissu minéralisé, centrée par la
cavité pulpaire, contenant un tissu conjonctif, riche en fibres nerveuses sensitives. La racine est
recouverte par une couche fine de cément, tissu dense minéralisé, et reliée à l’os par une fine
couche fibreuse appelée ligament alvéolodentaire.
• Les coupes non décalcifiées (incisive à G, et molaire à D) montrent les structures de la dent. La
dentine qui forme la majeure partie de la dent est composée d’une matrice organique calcifiée
identique à l’os. L’émail, extrêmement dur et transparent, est constitué de prismes parallèles de
matériel très calcifié.
• La microscopie électronique à balayage, objective l’arrangement du matériel calcifié au niveau de
l’émail et de la dentine.
• Dans l’émail, les prismes sont reliés un matériel presque aussi calcifié. Dans la dentine, la
composante inorganique est similaire, et plus abondante que celle de l’os.
LANGUE
• La langue organe musculaire de malaxage, et de perception principalement gustative, présente en
surface un sillon, le V lingual, qui sépare les deux tiers antérieurs du tiers postérieur. La muqueuse
de la partie antérieure est formée de trois types de papilles, filiformes, fongiformes, et caliciformes.
Ces dernières, au nombre de douze à vingt, forment une ligne en avant du V lingual.
• La microscopie électronique à balayage montre les papilles filiformes qui sont les plus nombreuses,
entourant une papille fongiforme.
• Sur une coupe au faible grossissement, apparait le relief irrégulier et rugueux des papilles filiformes,
et une papille caliciforme. La partie profonde de la section est formée de faisceaux entrecroisés de
fibres musculaires striées. Il s’y mêle de nombreuses glandes salivaires accessoires.
• A un plus fort grossissement, le revêtement de surface des papilles est en continuité avec celui de la cavité
buccale. Il est de type épidermoïde, kératinisé au niveau des papilles filiformes, et fin sur les papilles
fongiformes, qui sont soulevées par un tissu conjonctif richement vascularisé.
• Le corps de la langue est formé de faisceaux de fibres musculaires striées, entourant des glandes
salivaires accessoires séreuses, et muqueuses (peu colorées).
• Les papilles caliciformes localisées en avant du V lingual, sont encerclées par un profond vallum.
L’épithélium du versant papillaire contient de nombreux bourgeons du goût. Il s’associe à ces
structures nerveuses sensorielles, des amas de glandes séreuses qui s’abouchent à la base du
vallum. Les produits de sécrétion aqueux de ces glandes, dissout les composants alimentaires et
facilitent la perception du goût.
• Le tiers postérieur de la langue fait partie de l’anneau de tissu lymphoïde qui avec les amygdales
palatines, et les végétations adénoïdes protègent l’entrée des tractus digestif et respiratoire. Les
surélévations formées d’amas lymphoïdes recouverts par l’épithélium pavimenteux constituent les
amygdales linguales. Elles sont pénétrées par des invaginations ou cryptes épithéliales, qui

3
augmentent le contact du tissu lymphoïde avec la cavité buccale.
GLANDES SALIVAIRES
• La salive est produite par 3 paires de glandes salivaires : la parotide, la sous-maxillaire, et la
sublinguale, et par de nombreuses glandes accessoires. La sécrétion est continue dans les glandes
accessoires, tandis que les glandes principales sécrètent sous une stimulation parasympathique.
• La salive est une sécrétion aqueuse contenant des quantités variable de mucus, d’enzymes,
d’anticorps, et d’ions inorganiques. Chaque glande comporte deux types de cellules sécrétoires
(séreuse et muqueuse)
• La glande salivaire est une structure tubulo-acineuse ramifiée. L’acinus est composée de cellules
sécrétoires muqueuses, séreuses ou mixte, coiffées de quelques cellules myoépithéliales. Les acini
sont drainés par des canaux intercalaires également bordées de cellules sécrétoires. Ces derniers
confluent dans des canaux plus larges, les canaux striés.
• Sur une coupe au fort grossissement, les acini muqueux sont délimités par les expansions des
cellules myoépithéliales dont la contraction pousse la sécrétion vers les canaux. Les cellules
sécrétoires sont peu colorées, et leur noyau est aplati, basal.
• Les glandes mixtes séromuqueuses associent des croissants séreux aux acini muqueux.
• Les canaux striés présentent des replis membranaires (d’ou leur aspect strié en microscopie). Leurs
cellules sont riches en mitochondries. Ils modifient la constitution de la sécrétion salivaire
principalement séreuse, isotonique pour la rendre hypotonique.
• La glande salivaire principale présente une architecture lobulée. Les lobules, formés d’unités
sécrétoires, sont entourés par des septa de tissu conjonctif, qui contiennent les grands canaux, les
vaisseaux, et les nerfs
• La glande parotide est presque exclusivement constituée d ’acini de type séreux. La section
apparait fortement colorée.
• La glande sous-maxillaire est formée d’acini mixte séro-muqueux.
• Les acini de type muqueux prédominent dans la glande sublinguale, d’ou la section parait
faiblement colorée à l’hématoxyline-éosine.
HISTOLOGIE DU TUBE DIGESTIF (2)
• INDEX
– 1) Introduction
– 2) Structure générale
– 3) Œsophage
– 4) Jonction oeso-gastrique
– 5) Estomac
– 6) Jonction gastroduodénale
INTRODUCTION: LA DIGESTION
• L’ingestion et le morcellement se faisant dans la cavité buccale. Le bol alimentaire convoyé à
l’œsophage, est facilité dans sa progression par la sécrétion de la salive provenant des glandes
salivaires.
• L’œsophage transporte les aliments à l’estomac où le processus de morcellement s’achève et où
commence la digestion. Cette dernière associée à la contraction intense de la paroi gastrique,
réduit le contenu gastrique en un liquide à demi digéré appelé le chyme.
STRUCTURE GENERALE DU TUBE DIGESTIF

4
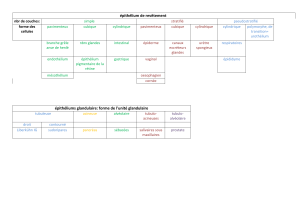
• Le tube digestif présente quatre couches fonctionnelles, dont la muqueuse varie principalement selon les
régions:
• 1) La muqueuse, qui comporte un revêtement épithélial, est soutenue par un tissu conjonctif appelé chorion.
Elle est limitée par une couche musculaire fine, la musculaire muqueuse.
• 2) La sous-muqueuse, formée de tissu conjonctif lâche, contient les vaisseaux, et les nerfs.
• 3) La musculeuse, constituée de 2 couches musculaires lisses, interne circulaire, et externe longitudinale.
• 4) L’adventice, couche externe de tissu conjonctif lâche contenant les gros vaisseaux et les nerfs. Dans les
portions recouvertes par un épithélium pavimenteux simple ou mésothélium, on l’appelle séreuse.
• Quelque soit la région du tube digestif, l’épithélium de la muqueuse, qui varie selon la fonction de
cette région, repose sur un chorion contenant des leucocytes en abondance variable. Ces derniers
constituent le système de défense régional contre les microorganismes.
• La musculaire muqueuse maintient un mouvement doux et constant de la muqueuse de surface et
propulse les sécrétions des cryptes glandulaires.
• La sous-muqueuse relie la muqueuse à la masse de la couche musculaire
• Dans le tube digestif, les fonctions sécrétoires et le péristaltisme (rythme de contraction de la
musculeuse) sont sous l’influence du système nerveux parasympathique. Les neurones effecteurs
constituent des plexus (petits ganglions) répartis de manière irrégulière dans la sous-muqueuse
(plexus de Meissner). De là, les fibres post-ganglionnaires atteignent les glandes.
• Les amas de cellules neuroganglionnaires, s’arrangent de manière plus régulière entre les couches
interne et externe de la musculeuse, et forment les plexus myentériques ou d ’Auerbach. Les
fibres post-ganglionnaires gagnent les muscles lisses environnants.
ŒSOPHAGE
• L’œsophage est un tube musculaire puissant qui s’étend de la cavité buccale (oropharynx), à
l’estomac. La première partie de la déglutition est un acte volontaire, suivi par un réflexe
péristaltique qui déplace le bol alimentaire vers l’estomac. Les aliments ne restent que quelques
secondes dans l’œsophage. Un sphincter physiologique évite le reflux des aliments vers l’œsophage.
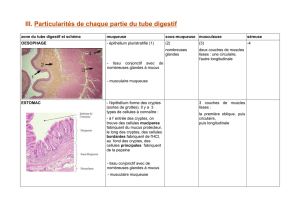
• Cette coupe au faible grossissement du tiers inférieur de l’œsophage, montre la muqueuse qui
présente des replis profonds au repos, permettant une distension importante lors du passage du bol
alimentaire. La sous-muqueuse contient quelques amas lymphoïdes et par place des glandes
muqueuses, qui participent à la lubrification de cette portion de l’œsophage. Les fibres musculaires
striées prédominantes dans le tiers supérieur, laissent place aux deux couches musculaires lisses
dans le tiers inférieur.
• La lumière de l’œsophage est bordée par un épithélium pavimenteux stratifié épais. Il assure une
fonction de protection contre la friction du bol alimentaire avec la paroi œsophagienne.
• L’épithélium pluristratifié est formé de plusieurs couches de cellules polyédriques. A partir de
cellules cubiques basales, elles s’agencent, tant dans l’épaisseur de l’épithélium que sa surface, en
pavés. Au repos, le tissu conjonctif du chorion s’invagine dans l’épaisseur du revêtement.
JONCTION OESO-GASTRIQUE
• A la jonction oeso-gastrique, la muqueuse subit une transition abrupte, d’un épithélium
pavimenteux de protection à une muqueuse glandulaire.
• Le revêtement pavimenteux parait clair et luisant sur cette vue interne de la jonction, et la
muqueuse gastrique montre un aspect rugueux brunâtre.
• Les autres tuniques sont en continuité de manière ininterrompue, notamment la sous-muqueuse qui
dans l’estomac siège immédiatement à la base des glandes gastriques.
• Il n’existe pas de sphincter anatomique au niveau de cette jonction.
• Dans certaines conditions pathologiques, la muqueuse gastrique se retrouve déplacée au niveau de
l’œsophage. N’étant pas adaptée à une fonction de protection, la muqueuse glandulaire présente
des modifications inflammatoires (teinte rougeâtre), et des ulcères (destruction du revêtement).
ESTOMAC
• L’estomac est une partie dilatée du tube digestif. Les aliments ingérés séjournent deux heures ou

5
plus, et y subissent un morcellement mécanique, par la puissante contraction de la musculeuse,
et une dégradation chimique par le suc gastrique. Le relâchement du sphincter pylorique permet au
chyme de passer dans le duodénum.
• Au repos, la muqueuse gastrique présente de nombreux replis longitudinaux. Ces plis permettent
une grande distension après le repas. Anatomiquement, l’estomac se divise en quatre régions: le
cardia, la grande tubérosité ou fundus, le corps, et l’antre pylorique. Le pylore se termine par un
puissant sphincter entourant la jonction gastroduodénale.
• Sur cette coupe du corps gastrique au faible grossissement, les plis de la muqueuse découpent le
relief en surface, où s’abouchent les cryptes glandulaires. Le fond des glandes repose sur la fine
musculaire muqueuse. La sous-muqueuse lâche et extensible, contient les gros vaisseaux. La
musculeuse est épaisse. La séreuse est fine, invisible à ce grossissement.
• La muqueuse du fundus et du corps gastrique est constituée par des glandes tubuleuses droites. Le
produit de sécrétion aqueux, très acide et contenant de la pepsine est libéré par le collet des
glandes au niveau des cryptes. Ces dernières ainsi que l’épithélium de surface sont formées de
cellules mucosécrétantes. L’épaisse couche de mucus neutre sécrété par ces dernières recouvrant la
surface de la muqueuse, la protège de l’autodigestion.
• Les glandes gastriques entassées, mal individualisées sur la coupe histologique, comportent trois
types de cellules: 1) les cellules mucosécrétantes qui recouvrent la surface et les cryptes, 2) les
cellules sécrétant l’acide chlorhydrique appelées cellules bordantes ou pariétales, 3) les cellules
principales qui élaborent la pepsine.
• La cellule bordante présente une membrane plasmique qui forme des canalicules profonds et anastomosés,
avec de nombreuses microvillosités. La sécrétion acide nécessitant un grand besoin énergétique, une richesse
cytoplasmique en mitochondries y est observée.
• Au niveau des glandes gastriques, il existe de nombreuses cellules endocrines mêlées aux autres cellules,
faisant partie du système endocrinien diffus(APUD). Leurs grains sécrétoires apparaissent denses aux
électrons.
• Contrairement aux glandes tubuleuses droites du fundus et du corps gastriques les glandes
pyloriques sont de type tubuleux ramifié. Leurs cryptes sont allongées. Les glandes sont
principalement mucosécrétantes. Le mucus élaboré sert à lubrifier et protéger le passage du chyme
dans le duodénum.
• Au fort grossissement les glandes antrales présentent un aspect comparable aux cryptes. Elles sont
également formées de cellules mucosécrétantes dont la majeure partie du cytoplasme est occupé
par une mucine neutre, non colorée.
• Tout le long de la muqueuse du tube digestif, il existe des cellules APUD ou neuroendocrines. Ces
cellules sécrètent des hormones suite à une stimulation locale, et induisent une action dans le
même secteur du tractus digestif. Elles sont mises en évidence par des techniques
immunohistochimiques, qui objectivent le produit de sécrétion spécifique de la cellule par le dépôt
intracytoplasmique d’un colorant brun.
JONCTION GASTRO-DUODENALE
• La jonction est marquée par le sphincter pylorique, au niveau duquel la muqueuse glandulaire
gastrique fait place au relief villeux qui caractérise la muqueuse duodénale et le reste de l’intestin
grêle. Le sphincter consiste en un épaississement important de la couche circulaire de la
musculeuse.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
1
/
50
100%