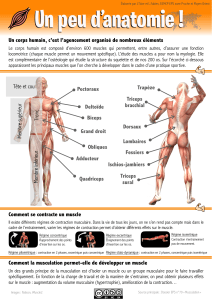
Mécanismes de contraction musculaire (en )

Les mécanismes de la contraction musculaire
A l'échelle de la cellule mais aussi à l'échelle du muscle.
Le calcium est le signal de la contraction et possède 3 fonctions :
Libération du neurotransmetteur (acétylcholine) au niveau de la plaque motrice
Glissement des filaments d'actines et de myosines. Pénétration grâce à des canaux calciques
potentiels dépendants (6 types)
Sur le plan métabolique, favorise la dégradation du glycogène et la synthèse d'ATP
I La contraction du rhabdomyocyte et du muscle squelettique strié : (figure 13
page 9)
Ni la longueur des filaments ni la longueur des filaments de myosine n'est modifiée,
seul les fibres coulissent entre elles (Théorie de la contraction par glissement des filaments)
Ensemble de réaction intervenant dans un ordre précis. Le point de départ est l'apparition
d'un PA au niveau de la membrane de la cellule musculaire squelettique.
Avec Em équivalent à EK car [K]e = 5mM et [K]i = 150mM → EK = - 90mV, même que le
potentiel de la membrane.
Ce PA apparaît par la libération de l'acétylcholine au niveau de la membrane.
L'acétylcholine n'intervient pas dans la contraction musculaire car au repos il y a libération en
permanence de quanta d'acétylcholine (un quantum = 10 000 molécules) qui produit une
modification du potentiel de membrane d'environ 1mV qui est trop faible pour réaliser un
dépolarisation totale (on parle de potentiel miniature). Le potentiel de la plaque motrice est
analogue au potentiel post synaptique excitateur au niveau des synapses neurones/neurones. Entre 2
neurones les variations peuvent être excitatrices ou inhibitrices alors que dans le cas de la synapse
de la plaque motrice n'est que excitatrice.
L'acétylcholine peut alors soit se lier à ses récepteurs canal soit être dégradée par voie
enzymatique (acétylcholine estérase) pour former de la choline qui est alors recapter par la
terminaison pour reformer de l'acétylcholine. Certaines molécules d'acétylcholine fuient dans
l'espace intermembranaire en sortant de la jonction neuromusculaire.
Maladies et drogues peuvent modifier le fonctionnement de la jonction.
La myasthénie (maladie auto immune) est une disparition progressive des récepteurs
cholinergiques.
Le curare bloque la jonction en se fixant sur les récepteurs canal à l'acétylcholine. C'est
un antagoniste inhibiteur.
Les récepteurs nicotiniques à l'acétylcholine sont des canaux ioniques liguant
dépendants dont la fixation du messager entraîne une entrée de Na+ et une sortie de K+
(3Na+/2K+).
La dépolarisation est au départ locale puis s'étend secondairement sur l'ensemble de la
surface de la cellule ouvrant au fur et mesure les canaux ioniques voltages dépendants (Na+VD)
entraînant l'entrée de Na+ qui accentue du coup la dépolarisation. On obtient donc une contraction
complète de la cellule musculaire (loi du tout ou rien).
Le potentiel de membrane (Em) se rapproche de celui de Na+ sans l'atteindre. La
phase de contraction dure entre 50 à 100ms ce qui beaucoup plus long que le phénomène
électrique responsable (1 à 2ms) intervenant avant la contraction. Couplage
excitation/contraction. Le PA est toujours terminé avant la contraction, on remarque un temps de
latence. (figure 14 page 9)

Une entrée de Ca2+ se produit puisque les variations du potentiel de membrane arrive
jusqu'à une triade (tubule transverse (invagination du sarcolemme) et réticulum sarcoplasmique)
permettant d'augmenter la libération du Ca2+ (grâce aux récepteurs à la ryanodine). Ce Ca2+ réagit
avec la sous unité C de la troponine qui change alors de conformation entraînant un écartement
entre l'actine et la myosine, et une modification de la sous unité I qui va alors permettre à la tête de
myosine de se fixer à l'actine et donc raccourcir le sarcomère. Le signal calcique disparaît
rapidement (30ms) grâce à la pompe Ca2+ATPasique qui fait rentrer le Ca2+ dans le réticulum
sarcoplasmique. La calcéquestrine piège alors le Ca2+. La troponine reprend sa forme intiale,
l'activité ATPasique de la tête de myosine est inhibée par I, la cellule musculaire se détend et
retourne à sa forme initiale. On a une période de relâchement (repolarisation de la membrane
sarcoplasmique). Fermeture des canaux Na+ et ouverture des canaux K+, sortie de K+ à cause du
gradient de concentration puis intervention de la Na+/K+ATPase.
La contraction musculaire est consommatrice d'énergie sous forme d'ATP. Elle doit
donc régénérer les ADP+Pi en ATP. Les réserves en ATP sont suffisantes pour réaliser une 10aine de
contractions. La myokinase permet la transformation à partir de 2 ADP d'ATP et AMP.
Il y a également le O2 (dette en dioxygène). Facteur limitant de la contraction. On trouve de
la myoglobine (une seule sous unité de l'hémoglobine) qui permet à la cellule de faire face à ce
déficit. La myoglobine a une plus grande affinité à l'O2 que l'hémoglobine (10 fois supérieure)
(figures 17 et 18 page 10)
La courbe sigmoïde de l'hémoglobine trahie la coopération entre les sous-unités.
Hyperbole pour la myoglobine. On a une meilleure affinité pour une pression partielle faible en
O2 de la myoglobine face à l'hémoglobine.
→ Stock d'O2 donc au niveau de la cellule musculaire près des mitochondries.
La tension et la force du muscle s'exerçant sur le tendon dépendent de plusieurs facteurs :
Le degré d'activation correspondant aux nombres de fibres musculaires sollicitées (force de
contraction plus importante si plus de fibres sollicitées)
Fréquence de stimulation, une stimulation unique entraîne une secousse musculaire, stimulus
maximal lors de la contraction de toutes les fibres. Si 2 PA phénomène de somation qui
s'observe bien lors de l'augmentation de PA jusqu'à atteindre le tétanos.
Niveau de raccourcissement dépendant du type de contraction musculaire qui intervient.
On distingue 3 types de contractions musculaires : (figure 19 page 12)
La concentrique : Cette contraction s'observe par un raccourcissement du muscle
s'accompagnant d'un mouvement de l'articulation. On parle de contraction dynamique. La
force produite provient du glissement des filaments de myosine et d'actine.
La statique s'effectue sans mouvement de l'articulation et sans modification de la
longueur du muscle, elle est dite isométrique (soulever une valise à bras tendus). Force
interne au muscle égale au moins à l'objet que l'on veut porter. Pas de glissement des fibres
d'actine et de myosine. Les unités motrices sont sollicitées et la force interne développée par
le muscle est supérieure à la force de l'objet porté. C'est une force dynamique.
L'excentrique implique un mouvement de l'articulation, c'est une contraction
dynamique car allongement du muscle. La force développée par le muscle dépend du
nombre d'unités motrices mobilisées, du type de muscle concerné, de la taille du muscle
avant contraction, de l'articulation et de la vitesse de contraction du muscle.
Plus d'unités motrices sont sollicitées, plus la force sera grande. Également, plus de il y a
de fibres de types II, plus la contraction est importante. Plus un muscle est volumineux, plus il
développe une importante force de contraction. La longueur du muscle dépend de sa forme et de la
longueur de ses tendons (son attachement aux os)
Au repos un muscle est légèrement étiré, il emmagasine une énergie potentielle de

contraction. La force maximale qu'il peut développer dépend de sa longueur initiale. Ce stock
d'énergie potentielle s'ajoute à la contraction des unités motrices.
Si un muscle est étiré de plus de 20% de sa longueur théorique d'étirement, sa force de
contraction sera plus faible. Les filaments d'actine et myosine seront trop éloignés, il y aura moins
de chevauchements donc cela limitera la puissance de contraction.
Cette force se transmet aux os par l'intermédiaire des tendons, il existe du coup un angle
articulaire maximal pour lequel la force transmisse à l'os (qui modifie l'angle de l'articulation) sera
maximale. Chaque articulations étant différentes, elles auront un angle optimal propre. Cet angle
doit donc être ni trop grand ni trop petit pour une contraction maximale du muscle.
La vitesse de contraction est aussi importante selon que l'on ait un muscle concentrique
(la force musculaire augmente quand la vitesse baisse) ou un muscle excentrique (la relation
entre vitesse et force est alors inversée).
II La contraction du cardiomyocytes et du cœur :
(figure 20 page 12)
Ces cellules sont serrées, étroitement proches, liées par des dispositifs (GAP jonctions, macula
adherens) qui permettent leur contraction simultanée.
Les cardionectrices ont une double spécificité, elles initient l'excitation myogénique
(automatisme cardiaque) et maintiennent la conduction de cette excitation.
Le cœur est composé de 3 types de cellules les contractiles, les cardionectrices et les
cardiomyocytes endocrines (ANF).
Le cœur commence à battre avant qu'il ne soit innervé pendant la vie fœtale. Si l'on
sectionne l'innervation du cœur, celui-ci continue de battre. Enfin si l'on met en culture des
cardionectrices elles se contractent spontanément.
On distingue 2 types de cellules cardionectrices, les nodales et les celles de Purkinje.
Les nodales se trouve au niveau des nœuds sino-auriculaire (Keith Flack) et atrio-ventriculaire
(Aschoff Tawara) en faisceaux (faisceaux de His) et en réseau au niveau du réseau de Purkinje.
Ces cellules assurent la rythmicité du cœur via l'orthosympatique (OS) par les sécrétions
de noadrénaline (NO) qui excitent les cellules et le parasympathique (PS) qui par l'acétylcholine
(Ach) ralentie leur activité.
Cela est le cas chez l'Homme, ce n'est pas vrai pour les autres animaux. Le système nerveux

(SN) a donc un contrôle sur le rythme myogène mais cependant on ne peut pas par notre volonté
contrôler notre rythme cardiaque.
(figure 21 page 13)
Les cardiomyocytes sont liés entre eux par une zone de contact nommée disque
intercalaire présentant des stries scalariforme (en forme d'escalier). On distingue les segments
transversaux perpendiculaires à l'axe de la cellule on l'on a des bosses et des creux. Les bosses
permettant l'encrage des filaments d'actine sur le disque intercalaire via 2 protéines (actinine
et vinculine) et les creux qui sont épais c'est la macula adherens (zone d'adhésion).
La zone dans l'axe de la cellule présente des GAP jonctions ou nexus qui sont des
connexons (composés de 6 connexines) formant des canaux permettant les échanges Na+, Ca+,
K+ et ATP.
Le point de départ du rythme cardiaque sont les cellules nodales qui transmettent leur
activité aux cardiomyocytes via les GAP jonctions. Ce sont des pacemakers. L'excitation
commence aux oreillettes (nœud sino-auriculaire) puis se propage au nœud auriculo-ventriculaire.
On observe ensuite un ralentissement de la transmission du signal dans les faisceaux de His dû au
tissu fibreux (qui joue le rôle d'un isolant électrique) qui va permettre de produire une contraction
des ventricules en décalage de celles des oreillettes. (figure 22 page 13)
On peut parler d'un couplage excitation/contraction par le tracé d'un électrocardiographe
(ECG) qui est une représentation des forces électromotrices générées par l'ensemble de l'activité du
cœur. Ce couplage implique des canaux ioniques qui vont faire varier les PA des cellules. On étudie
leur fonctionnement grâce aux techniques de Patch Clamp.
(figure 23 page 13)
On caractérise les cellules nodales par le fait qu'elles possèdent un potentiel de repos
instable, on parle de potentiel pacemaker. Ce potentiel instable est dû à la perméabilité au K+
de la cellule. Alors que le K+ sort de la cellule on a une ouverture des canaux Na+VD (ce courant
sodique est dit « funny »(étrange) car il se réalise alors que le potentiel de membrane est positif).
On a alors une ouverture transitoire des canaux Ca2+ (T) suivit d'une ouverture des canaux Ca2+
(L). Cette entrée de Ca2+ entraîne une dépolarisation qui ne comporte pas de plateau (pas de tétanos
possible donc). Cette dépolarisation se transmet alors au reste des cellules (cardiomyocytes). Le
retour au repos se fait par l'ouverture des canaux K+.
(figure 24 page 15)
L'activité des oreillettes et ventricules se caractérise par des variations de potentiels. Cette
activité cardiaque comprend 5 étapes
Les ondes P, correspondant à la dépolarisation (donc contraction) des oreillettes
L'intervalle PQ, durée nécessaire à la transmission de l'influx électriques des oreillettes aux
ventricules
L'onde QRS correspond à la dépolarisation des ventricules. (repolarisation des oreillettes)
L'intervalle ST durée de la période réfractaire empêchant un tétanos
L'onde T correspond à la repolarisation des ventricules (relâchement Er = - 90mV)
Le potentiel de repos est dû à l'inégale répartition des ions de part et d'autre des cellules. Le
PA est issu d'une dépolarisation brève et réversible, il n'existe que sous la loi du tout ou rien. Le PA
dépolarise jusqu'à +30mV (près du potentiel de repos de Na+). On utilisant de la tétrodoxine
(TTX) on bloque les canaux Na+ et l'on empêche l'apparition du PA.
Le Na+ en entrant dans la cellule favorise l'ouverture d'autres canaux Na+, il amplifie son
entrée. Cependant ceux ci s'inactivent ce qui l'empêche d'atteindre ENa+. L'entrée d'autres ions
comme le K+ va alors repolariser la cellule. Il existe des pompes qui contre balance l'entrée de Na+,
notamment la NaATPase.

Chez l'homme le coeur bat environ 70 à 75 fois par minute. Le nombre de battement est
inversement proportionnel à la taille de l'animal. Le cœur d'une musaraigne bat entre 500 et 700 fois
par minutes alors que celui d'un éléphant produit 20 à 30 battements/min.
Une telle variabilité provient d'une modification de la période réfractaire (intervalle ST) qui
raccourcie ou augmentée. Chez les souris la priorité est au contrôle de l'OS (excitateur), chez
l'homme c'est le PS (inhibiteur) qui est prioritaire
La régulation porte sur la fréquence cardiaque et le volume d'éjection systolique. Cela
entraîne donc une régulation du débit cardiaque (fréquence x éjection systolique). Cette
régulation dépend de l'innervation OS et PS.
(figure 26 p16)
Le nerf vague (PS) projette sur les nœuds tandis que l'OS projettent sur l'ensemble (à peu près) du
cœur.
La fréquence cardiaque est due à un effet chronotrope inhibiteur du PS par la libération
d'Ach, au niveau sinusal, sur les récepteurs cholinergiques muscariniques couplés à l'adénylase
cyclase qui active des protéines G inhibitrices qui entraînent une diminution de l'AMPc provoquant
l'ouverture des canaux K+ et donc une hyperpolarisation.
L'OS est chronotrope positif , libérant de la NO qui agit sur les récepteurs β1 au niveau des
oreillettes et des ventricules (l'ensemble du myocarde). Les récepteurs β1 sont couplés à l'adénylase
cyclase qui active des protéines G activatrices augmentant la concentration d'AMPc permettant
l'entrée de Ca2+ (effet ionotrope positif) qui augmente le plateau.
Comme l'on a un effet dominant du PS sur l'OS il faut couper en premier l'innervation PS
si l'on veut observer l'effet chronotrope positif.
Au cours d'un effort physique la fréquence cardiaque augmente grâce à une diminution de
l'OS et une augmentation du PS. Les catécholamines surrénales circulent en trop faible
concentration pour avoir un effet sur le rythme cardiaque sauf lors d'un stress.
(figure 27 page 16)
La régulation d'éjection du volume systolique (environ 65 à 70ml chez l'homme, au repos).
Il faut augmenter le volume si l'on veut ralentir l'activité du cœur. Système de précharge, volume de
sang déjà présent dans un ventricule avant sa contraction d'environ 130ml appelé volume
télésystolique. Phénomène de la post charge (variation de pression des artères issues des
ventricules). Plus un ventricule reçoit du sang, plus il se dilate et plus il accumule de l'énergie qui
lui permet d'éjecter du sang. Plus le volume télédiastolique est important plus le volume
d'éjection systolique est important. Pour augmenter ce volume il faut donc augmenter les retour
veineux. On a donc une adaptation interne au débit cardiaque qui suit la loi de Starling. Le
volume d'éjection systolique est le même dans chaque oreillette bien que la pression soit différente.
L'innervation OS concerne tout la cœur et augmente la force de contraction du cœur ce
qui augmente le volume télédiastolique. Plus l'effet OS est important plus le volume télédiastolique
est important. L'OS à un effet plus important que la loi de Starling
(figure 28 page 17)
Contrôle PS sur le volume, car l'effet de PS est antagoniste de celui d'OS ? Non, car pas
de contrôle de PS sur le volume d'éjection vu qu'il ne projette pas sur les ventricules.
La contractilité du cœur est égale au rapport volume d'éjection systolique sur celui
télésystolique et est égal à 0,5.
OS est responsable aussi de la relaxation des ventricules. Le mécanisme de post charge
 6
6
1
/
6
100%