Octobre 2009 BIOTECHNOLOGIES ET PRODUCTIONS

Octobre 2009
BIOTECHNOLOGIES ET PRODUCTIONS
VEGETALES
Les méthodes spécifiques d’amélioration des plantes
Mme Bonnet
Ces techniques englobent toutes les interventions humaines cherchant à modifier le génome
des plantes pour mieux les adaptées au besoin de l’homme
Ce sont des méthodes qui comportent à la fois des modifications dans les cultures artificielles
et de la biologie moléculaire.
I. Mutagenèse et sélection in vitro
= introduction volontaire d’un changement dans la séquence NTidique d’un gène : mutation.
Elles permettent d’agir sur la relation entre la séquence d’un gène et la fonction de la protéine
qu’il code.
A. Mutagenèse aléatoire
Permet de produire des mutations à des emplacements non déterminés du vecteur qui porte le
gène d’étude.
Le gène qu’on veut étudié est inséré dans un vecteur
En admettant qu’il code pour une protéine,
cela va entraîner un phénotype donné et
quand on fait de la mutagenèse, c’est qu’on
va étudier le gène dans lequel on a
introduit une mutation. A priori la protéine
codée sera différente et cela se traduira au
niveau du phénotype.
On cherche a établir une relation entre la
structure du gène et la protéine qu’il code.

3 techniques différentes :
On utilise une enzyme de
restriction qui possède un
site dans le gène. Ici EcoRI
On linéarise le vecteur.
- 1 : on utilise une nucléase qui va permettre d’éliminer l’ADN sous forme simple brin.
On fait agir une ligase qui va permettre de recirculariser le vecteur.
Le gène possède 4 paires de bases en moins : on a introduit une mutation par délétion dans
ce gène.
- 2 : on réalise une addition de NT pour n’avoir que des doubles brins.
On fait de nouveau agir la ligase pour relier les 2 extrémités.
Le gène a été agrandi par addition de NT.
- 3 : on ajoute une molécule d’ADN étranger qu’on coupe avec la même enzyme.
L’ADN étranger est inséré dans le vecteur.
Le gène a été muté.
A partir des gènes mutants, on va regarder s’il y a un effet sur le phénotype.
Le phénotype qu’on va trouver, c’est le résultat d’une modification de plusieurs NT. Ce n’est
pas toujours évident d’associer le phénotype muté à telle ou telle mutation.
Cela reste une première approche pour étudier les relations structure/fonction.
B. Mutagenèse dirigée
Va porter sur un endroit précis du gène.
On va modifier d’une manière prédéterminée la séquence du gène.
- On intègre un gène dans un vecteur.
- On digère le gène par E et H.
- On obtient un vecteur ouvert et la zone
entre E et H éliminée.
- On introduit dans le vecteur un gène
muté au niveau d’un seul NT entre
deux sites E et H
- On recircularise le vecteur avec le gène
muté
On l’appelle la mutagenèse par cassette.
On va faire s’exprimer le gène pour regarder si la mutation a changé le phénotype.

II. Les transferts de gènes ou génie génétique
A. Le transfert du gène dans la plante-hôte
On vise à créer un OGM.
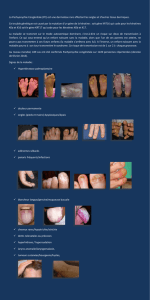
ON exploite un phénomène naturel qui existe entre les plantes et une famille de bactéries : les
agrobactéries (agrobacterium).
Ces plantes sont de la famille des rhizobiacées vivant dans les sols et elles infectent les
végétaux en pénétrant par une blessure de la plante.
Ce phénomène entraîne la formation de tumeur ou de galles au niveau du collet (allongement
entre la tige et les racines) mais aussi au niveau des racines et des tiges.
Cette maladie s’appelle : « croun-gall ».
Le développement de la tumeur ne s’arrête qu’à la mort de la plante.
Les cellules atteintes contiennent des substances spécifiques qu’on appelle opines (AA peu
courants) et sont synthétisées dans la tumeur à partir des gènes bactériens au dépend du
métabolisme de la plante. Ces opines vont servir aux bact pour se fournir en énergie.
Ti : tumefasciens
Ri : rhizogenes
Ce plasmide Ti confère le pathogène à la
bactérie. Au niveau de ce plasmide Ti, on a
une région ADNt qui va être transféré au
génome de la plante receveuse.
Ops : gènes responsables de la synthèse
des opines
Onc : Prolifération tumorale est la
conséquence de la synthèse de cytokinine
et auxine.
Région T : Ops + Onc
C’est cette région qui est transférée dans la
plante grâce à la région Vir.
Opc : responsable du catabolisme des
opines (pour que les bact puissent se
fournir en énergie)
Il y a aussi une région responsable de la
réplication du plasmide
Le génie génétique a exploité ce plasmide
naturel en exploitant cette région T en
enlevant les fonctions oncogènes et en les
remplaçant par le gène introduit dans la
plante receveuse.
On a de l’ADNt désarmé, c’est le gène qui
nous intéresse qui va être transféré dans la
plante grâce à la région Vir qui elle est
toujours présente.

B. Le clonage du gène
1. insertion du gène dans un vecteur
Le vecteur qu’on va utiliser est celui d’E. Coli.
BD/BG : bordure droite/bordure gauche
GUS : code pour
une enzyme la
βglucuronidase
Il est entouré de 2 sites : XbaI et EcoRI
NPTII : code la néomycine
phosphotransférase II, il confère la
résistance à un Ab la kanamycine chez les
euK.
Kan R : confère lui aussi la résitance à la
kanamycine mais chez les proK
p35S : promoteur qui permettra la Tc du
gène d’intérêt qui lui sera intégré en aval.
On remplace ce gène dans le vecteur de Coli à la place de GUS (entre XbaI et EcoRI)
2. insertion du plasmide recombiné dans E. Coli
Plasmide recombiné avec le gène, on réalise la transformation dans E. Coli.
Les bactéries doivent être traitées au CaCl2 ce qui créer des pores au niveau de la paroi de la
bactérie : la bactérie est compétente => elle est prête à recevoir un plasmide.
On réalise un choc thermique (4-42°C)fait en sorte qu’il y a une déstabilisation des couches
lipidiques de la paroi => le plasmide va pouvoir entrer dans la bact, une fois dedans on
rabaisse la température pour restabiliser les couches lipidiques, et le plasmide ne peut plus
sortir.
On met en culture ces bact à 37°C pendant la nuit. On aura indirectement une amplification
du gène.

3. sélection des bactéries recombinantes
Le gène peut ou non s’intégrer au vecteur,
on obtiendra donc deux types de cellules.
On va donc faire un criblage grâce au gène
GUS et grâce à la kanamycine sur boite de
Petri avec de la gélose (Kanamycine + X-
glucoronide (substrat de la β-glucoronidase
codée par le gène GUS))
On obtient des colonies individualisées. Deux types de colonies : blanches opaques et bleues.
Les colonies qui nous intéressent sont les blanches car les bleues sont celles qui ont eu le
vecteur où le gène GUS a pu s’exprimer.
On pique une colonie, on fait une culture liquide à 37°C pendant une nuit sous agitation pour
que la bactérie se multiplie.
4. la conjugaison triparentale
Elle va permettre d’introduire le plasmide recombiné dans Agrobacterium tumephasciens.
Ces trois souches sont mises en présence
dans le même tube.
Le plasmide Helper va stimuler
l’introduction du plasmide recombiné dans
A. tumefasciens qui se retrouve avec deux
plasmides.
Il faut que le gène aille se positionner dans
le plasmide Ti
Il va y avoir recombinaison homologue
grâce à la reconnaissance des bordures
droite et gauche. Ce qui fait qu’il va y
avoir échange entre les ADN des
plasmides Ti et d’E. Coli.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%