Cardiologie 350KB Sep 10 2010 06:40:17 PM

Cardiologie
Anatomie du cœur .................................................................................................................................. 4
Caractères généraux ............................................................................................................................ 4
Conformation externe ......................................................................................................................... 5
Conformation interne .......................................................................................................................... 5
Structure du cœur ............................................................................................................................... 6
Innervation cardiaque ......................................................................................................................... 7
Vascularisation cardiaque ................................................................................................................... 7
Rapports et topographie du cœur ....................................................................................................... 8
Présentation générale de la physiologie du cœur et terminologie ......................................................... 9
Organisation générale de la circulation .............................................................................................. 9
Variables cardiaques ........................................................................................................................... 9
Terminologie spécifique ...................................................................................................................... 9
Physiologie générale des vaisseaux sanguins .................................................................................... 10
Paramètres sanguins ......................................................................................................................... 11
Régulation des processus cardiaques ............................................................................................... 11
Electrophysiologie du myocarde et du tissu nodal ............................................................................... 12
Potentiel membranaire de repos ...................................................................................................... 12
Potentiel d’action .............................................................................................................................. 12
Facteurs de variation ......................................................................................................................... 12
Conduction de l’onde électrique ....................................................................................................... 13
Physiologie du myocarde ...................................................................................................................... 14
Organisation ...................................................................................................................................... 14
Métabolisme ..................................................................................................................................... 14
Mécanismes de la contraction cardiaque ......................................................................................... 14
Physiologie de la pompe cardiaque....................................................................................................... 15
Les différentes phases de la contraction ........................................................................................... 15
Rôles des valves ................................................................................................................................. 16
Signes extérieurs du fonctionnement de la pompe cardiaque ......................................................... 16
Régulation de la pression artérielle ....................................................................................................... 17
Importance de la régulation de la pression artérielle ....................................................................... 17
Autorégulation locale ........................................................................................................................ 17
Régulation nerveuse .......................................................................................................................... 18

Régulation hormonale ....................................................................................................................... 18
Régulation passive ............................................................................................................................. 19
Mise en œuvre de la régulation de la pression artérielle ................................................................. 19
Conclusion ......................................................................................................................................... 19
Les bruits physiologiques du cœur chez le cheval et le chien ............................................................... 20
Définitions préliminaires ................................................................................................................... 20
Les bruits du cœur ............................................................................................................................. 20
Les souffles cardiaques ...................................................................................................................... 22
Auscultation cardiaque : aspects pratiques ...................................................................................... 23
Sémiologie de l’appareil cardiovasculaire ............................................................................................. 25
Anamnèse et commémoratifs ........................................................................................................... 25
Examen clinique général ................................................................................................................... 25
Inspection .......................................................................................................................................... 25
Palpation............................................................................................................................................ 25
Auscultation....................................................................................................................................... 25
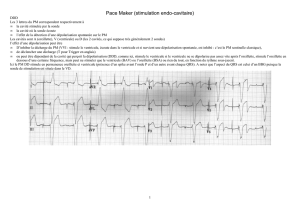
Electrocardiographie chez les animaux domestiques ........................................................................... 28
Définition ........................................................................................................................................... 28
Importance ........................................................................................................................................ 28
Principes de l’analyse vectorielle ...................................................................................................... 28
Présentation d’un tracé électrocardiographique type ...................................................................... 29
Dépolarisation et repolarisation chez les animaux domestiques ..................................................... 29
Les dérivations électrocardiographiques .......................................................................................... 31
L’axe électrique du cœur ................................................................................................................... 34
Vectocardiographie ........................................................................................................................... 35
Electrocardiogrammes des animaux domestiques ........................................................................... 35
Technique d’enregistrement et de lecture d’un tracé ECG............................................................... 36
Sémiologie radiographique de l’appareil cardiovasculaire .............................................................. 40
Techniques et indications .................................................................................................................. 40
Principes d’interprétation ................................................................................................................. 40
Images radiologiques normales ........................................................................................................ 40
Guide pratique ....................................................................................................................................... 57
Auscultation....................................................................................................................................... 57
Physiologie cardiaque ........................................................................................................................ 58
Electrocardiogramme ........................................................................................................................ 58


Anatomie du cœur
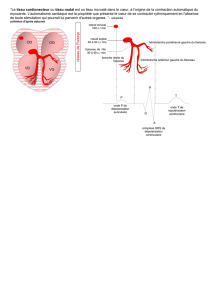
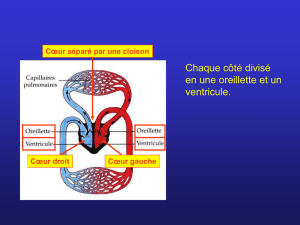
Le cœur est l’organe central de l’appareil circulatoire, c’est le moteur de la circulation sanguine. Il est
entouré d’une séreuse, le péricarde. Chez les mammifères, il est cloisonné en deux chambres : un
demi-cœur gauche et un demi-cœur droit.
Le cœur droit reçoit le sang carbonaté, qui est alors chassé dans les poumons. Il participe à la
circulation pulmonaire, ou « petite circulation ».
Le cœur gauche reçoit le sang hématosé et le propulse vers les tissus. Il participe à la circulation
générale, ou « grande circulation ».
Chaque cœur est divisé par des valves en deux chambres : l’atrium (ou oreillette), où débouchent les
veines, et le ventricule, d’où part un tronc artériel. La division n’est pas totale : les deux chambres
communiquent par les valves.
Le cœur fonctionne de façon cyclique : il se contracte pendant la systole, se relâche et se remplit de
sang pendant la diastole.
Caractères généraux
Le cœur est de couleur rouge. Les sillons présents sur l’organe et les vaisseaux sont recouverts d’une
graisse sous-épicardique, qui est la dernière à disparaître en cas de cachexie. Cette graisse est jaune
et molle chez le cheval, blanche et onctueuse chez le porc, blanche et ferme chez les bovins.
La consistance du cœur est ferme au niveau des ventricules, molle au niveau des oreillettes. Ses
dimensions et sa masse sont très variables. Sa capacité est difficile à estimer ; néanmoins, on évalue
le volume de l’ondée systolique à ¼ de la capacité totale des ventricules.
C’est un cône, aplati dans le même sens que le thorax (dorso-ventralement chez l’Homme, latéro-
latéralement chez les animaux domestiques). Le cœur droit est crânial, le cœur gauche, caudal. La
pointe du cœur est orientée ventro-caudalement. Ce cône est divisé en deux par le silαlon
interventriculaire.
Le cœur est incliné par rapport au sternum, d’un angle α variable selon les espèces : 25° chez le chat,
40° chez le chien, 50° chez le porc, 90° chez les bovins et les chevaux.
3° côte
6° côte
1° côte
Axe
horizontal

Conformation externe
La face auriculaire est constituée d’une partie atriale, comportant les auricules, reliquats
embryologiques, et d’une partie ventriculaire, reconnaissable à son sillon interventriculaire
paraconal.
La face ventriculaire montre les embouchures des grosses veines. Le sillon coronaire y est plus large,
indivisé, et partage à son tour cette face en une partie atriale, portant les atria droit et gauche, et
une partie ventriculaire, caractérisée par le sillon interventriculaire sous-sinusal.
La base du cœur est formée du croissant atrial, et comporte les veines caves caudale et crâniale,
l’aorte et les veines pulmonaires.
La pointe (ou apex) appartient totalement au ventricule gauche. Les fibres musculaires qui le
constituent se terminent en spirale, appelée « vortex ».
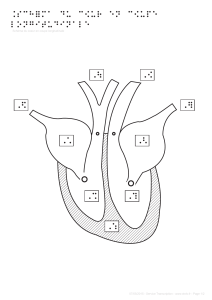
Conformation interne
La complexité de l’organogénèse explique qu’il n’existe pas deux individus avec une conformation
cardiaque identique.
Les septums
Le cœur est traversé par deux cloisons perpendiculaires :
- la première est longitudinale et continue, il s’agit du septum interatrial et interventriculaire.
Le septum interatrial est le résultat de la fusion de plusieurs vestiges embryonnaires. Le
septum interventriculaire est constitué d’une partie membraneuse, fine, et d’une partie
musculeuse, épaisse.
- la seconde est transversale, incomplète, et s’appelle le septum atrio-ventriculaire. Il est
percé de deux orifices, les orifices atrio-ventriculaires droit (valvule tricuspide) et gauche
(valvule mitrale).
Ces septums divisent le cœur en 4 cavités de taille inégale.
Les cavités
A droite
L’atrium droit reçoit le sang carbonaté et le chasse dans le ventricule droit. Dans la partie lisse,
débouchent les veines caves crâniale et caudale, le sinus coronaire et les veines du cœur. La partie
pectinée correspond à l’auricule droite. Ces deux parties sont séparées par une crête terminale qui
correspond en conformation externe au sillon terminal.
Le ventricule droit est séparé en une chambre d’entrée et une chambre de sortie du sang par la crête
supraventriculaire. Il contient l’ostium atrio-ventriculaire droit et l’ostium pulmonaire.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
1
/
58
100%