L`objet de l`étude est le moteur Vulcain assurant la propulsion de l

Examen de Thermodynamique
L. LE MOYNE
Novembre 2002
sans documents – 2h
Les moteurs d'automobile fonctionnent en brûlant un mélange air combustible lorsque le
volume du piston se trouve au minimum, autour du point mort haut. Dans un moteur essence
4 temps le mélange air combustible est aspiré par la descente du piston. Près de la position
basse (point mort bas) du piston, les soupapes d'admission se ferment et le mélange est
emprisonné dans une enceinte fermée, formée par le piston, le cylindre et la culasse, jusqu'à
l'ouverture des soupapes d'échappement. Pendant la phase où l'enceinte est fermée les gaz
subissent une compression puis une combustion.
Les parois du cylindre, du piston et de la culasse sont considérées adiabatiques dans un
premier temps.
Le volume dans le cylindre en fonction du degré vilebrequin
est donné par la formule :
22
v
v
csincos1
21
1
1
V
V
(
c
V
est la cylindrée unitaire,
v
le rapport volumétrique,
le rapport course/bielle, et
le
degré vilebrequin).
On étudie un moteur avec les caractéristiques suivantes :
c
V
=330cm3
v
=9
=3,8
angle de fermeture des soupapes admission:
=214°
On assimile le mélange air combustible à un mélange idéal de gaz parfaits de rapport de
capacités calorifiques constant et égal à 1,4.
1 Calculer le volume Vfa dans le piston à la fermeture des soupapes admission.
2 En considérant que le mélange air combustible qui pénètre dans le piston est dans les
conditions de pression et température ambiantes jusqu'à la fermeture des soupapes
admission, calculer la masse de mélange enfermée au moment de la fermeture des
soupapes.
En raison des pertes de charge et des transferts thermiques dans les conduits d'admission, la
pression et la température du mélange à la fermeture des soupapes n'est que de 390mg.

Les figures 1 à 3 montrent l'évolution de certaines variables thermodynamiques pendant une
partie du cycle moteur en fonction de l'angle vilebrequin
. La compression, qui a lieu de
=214 à
=360 (point mort haut ou PMH), est considérée réversible et les parois du cylindre
isolées thermiquement.
3 A partir de la masse réelle et des courbes de pression et de volume, calculer la pression
et la température réelles du mélange à l'admission, au moment de la fermeture des
soupapes.
A
=360 (PMH), la combustion démarre. On peut modéliser la combustion comme un apport
de chaleur au mélange air combustible proportionnel à la quantité de combustible brûlé. Ainsi,
si pendant un temps dt, on brûle une masse de combustible dmc , la quantité de chaleur reçue
par le mélange est
c
Q
=k.dmc .
4 En écrivant le premier principe, exprimer la variation de température du mélange en
fonction de la chaleur reçue
c
Q
et du travail des forces de pression.
5 Exprimer
c
Q
en fonction uniquement de P, V , , dP et dV.
6 A partir de la figure 3, déduire la masse de combustible dans le mélange. Pour l'essence
k=43.106 J/Kg.
En réalité la masse de combustible est de mc= 24,85mg et le cylindre ne peut pas être
considéré adiabatique pendant la combustion.
7 En considérant que le dégagement de chaleur total reste le même mais qu'il y a en plus
un transfert de chaleur à travers les parois du cylindre, évaluer la chaleur perdue
pendant la combustion à travers les parois.
La compression absorbe une partie de l'énergie dégagée par la combustion.
8 Calculer le travail nécessaire à la compression en la considérant adiabatique.
9 Calculer l'énergie restante pouvant être récupérée.
10 Calculer la température des gaz en fin de combustion en considérant que la réaction est
très rapide (tenir compte du dégagement de chaleur par combustion, des pertes
thermiques aux parois et du fait que le volume varie peu autour du PMH).
Données : Patm=1 bar, Tadm=20°C, r=272 J/Kg.K

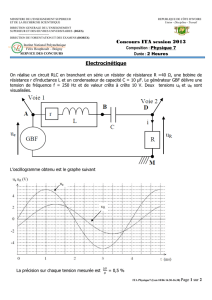
200 250 300 350 400 450 500
0
10
20
30
40
50
60
70
80
(DV)
P (bar)
fig 1-Pression
200 250 300 350 400 450 500
0
50
100
150
200
250
300
350
400
(DV)
V (cm3)
fig 2 - Volume
200 250 300 350 400 450 500
0
200
400
600
800
1000
1200
(DV)
(J)
fig 3 :
360
)PdVVdP(
1
1

1
/
4
100%