Quelques applications de l`électrolyse

TP 8
QUELQUES APPLICATIONS DE L’ELECTROLYSE
TS Spécialité Chimie 2006/2007
Compétences exigibles mises en jeu lors de ce TP :
Objectifs.
Réaliser et analyser la méthode de purification du cuivre par électrolyse.
Utiliser cette technique à la réalisation d'un dépôt électrolytique d’un métal sur un autre.
Réaliser l’électrolyse d’une solution de chlorure de sodium et montrer son intérêt industriel
I. Quelle est la technique de l'affinage du cuivre ?
1. Montage expérimental et protocole.
Vous disposez d'un générateur de tension continue (12 V - 1 A), d'un rhéostat
(33 - 1 A), d'un multimètre.
L'électrolyseur utilisé est constitué :
- d'un becher de 200 mL contenant la solution électrolytique,
- de deux électrodes : une plaque de cuivre à la cathode notée C et un fil de
cuivre à l’anode notée A
Peser les électrodes et noter leurs masses respectives au centigramme près.
Dessiner le schéma du circuit électrique à réaliser pour effectuer une électrolyse en y insérant les appareils
nécessaires pour pouvoir régler et mesurer l’intensité du courant.
Réaliser le montage.
Verser dans le becher 150 mL environ de solution de sulfate de cuivre (II) à la concentration molaire de 1,0
mol.L-1 dans laquelle les électrodes plongent jusqu’à mi hauteur.
Installer sous le becher un agitateur magnétique en évitant que le turbulent heurte les plaques de cuivre lors de
sa rotation.
Mettre le générateur sous tension et régler rapidement l’intensité du courant à 0,50 A. Déclencher le
chronomètre. La durée de l'électrolyse est fixée à 30 minutes.
L'agitation constante de la solution est essentielle pour assurer la stabilité du courant !
Pendant la durée de cette opération, passez aux questions 2 et 3
Au bout de 30 minutes, ouvrir le circuit, extraire les deux plaques et les rincer à l’eau distillée.
Observer et décrire l'état des deux électrodes.
Sécher doucement les deux électrodes. Peser à nouveau chaque électrode et calculer la variation de leur masse
respective.
Quelle constatation peut-on faire compte tenu de la précision de la balance utilisée ?
2. Comment interpréter cette électrolyse ?
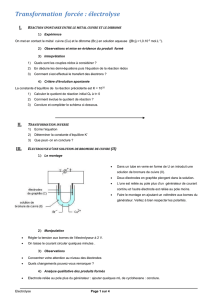
Compléter le schéma ci-contre en indiquant :
- la position de A et de C,
- le sens du courant dans le circuit électrique,
- le sens de déplacement des électrons dans les conducteurs métalliques,
- le sens de déplacement des ions cuivre(II) dans la solution électrolytique.
Cu2+

TP 8
QUELQUES APPLICATIONS DE L’ELECTROLYSE
TS Spécialité Chimie 2006/2007
Identifier l'électrode à laquelle se produit la réaction d'oxydation et l'électrode
à laquelle se produit la réaction de réduction. Ecrire les réactions aux électrodes. (Couple en jeu : Cu2+
/Cu)
En déduire la réaction d'oxydo-réduction correspondant à la transformation chimique provoquée par le
passage du courant dans le circuit. Que vaut le quotient de réaction Qr ? La concentration varie-t-elle au
cours de la réaction ?
Justifier l'expression "électrolyse à anode soluble".
Pourquoi cette technique permet-elle de purifier du cuivre contenant des traces de métaux précieux
inoxydables dans ces conditions ?
3. Peut-on prévoir la masse du dépôt de cuivre ?
Données physico-chimiques :
Charge élémentaire : 1,6.10-19 C Constante d’Avogadro : 6,02.1023 mol-1
Masse molaire du cuivre : MCu = 63,5 g.mol-1
Calculer la quantité d’électricité (Q = I.t) qui a traversé le circuit pendant la durée de l'électrolyse.
Etablir un tableau d’avancement relatif à la réaction anodique
En déduire la masse théorique du dépôt de cuivre. La comparer à la masse mesurée.
II. Une application aux dépôts électrolytiques.
1. Situation-problème.
On vous propose de réaliser un dépôt de cuivre sur un objet métallique par électrolyse.
Dresser la liste du matériel et des produits nécessaires pour y parvenir.
Dessiner le schéma électrique du montage, puis le réaliser. Faire vérifier par le professeur.
Immerger les électrodes de quelques cm dans la solution électrolytique.
Fixer la durée de l'électrolyse à 5 minutes et l'intensité du courant à 0,40 A.
Ecrire les réactions aux électrodes.
2. Vos prévisions sont-elles vérifiées ?
Au bout de 5 minutes, ouvrir le circuit, extraire la cathode de l’électrolyseur avec précaution et la rincer à l’eau
distillée.
Sécher doucement l'électrode
Déterminer la masse du dépôt métallique.
III. Comment et pourquoi réaliser l’électrolyse d’une solution aqueuse de chlorure de sodium ?
1. Montage expérimental et protocole.
Vous disposez d'un générateur de tension continue (6 V).
L'électrolyseur utilisé est constitué :
- d'un tube en U contenant une solution de chlorure de sodium saturée( Na+ +
Cl- )
- de deux électrodes en graphite

TP 8
QUELQUES APPLICATIONS DE L’ELECTROLYSE
TS Spécialité Chimie 2006/2007
Dessiner le schéma du circuit électrique à réaliser pour effectuer une électrolyse
Réaliser le montage.
Ajouter à l’anode quelques gouttes d’indigo et à la cathode quelques gouttes de phénolphtaléine
Mettre en marche le générateur et noter vos observations
2) Questions
1) Faire l’inventaire des espèces chimiques présentes
Ecrire les réactions susceptibles de se produire à l’anode, à la cathode
2) D’après vos observations, quelles sont les réactions effectivement observées ?
3) En déduire l’équation de réaction de l’électrolyse de la solution de chlorure de sodium ?
Refaire la même électrolyse en utilisant un petit bécher à la place du tube en U
Noter vos observations. Quelle odeur prend la solution ?
3) Etude documentaire
Texte publicitaire : « L’eau de la piscine doit avoir une teneur en sel de l’ordre de 3g.L –1 . Elle passe dans une
cellule où elle subit une électrolyse qui produit de l’hypochlorite de sodium ( plus communément appelé eau de
Javel )qui se dilue dans l’eau et constitue un puissant désinfectant. Les piscines ainsi traitées n’ont jamais
l’odeur de chlore »
1) L’ion hypochorite ClO- , est obtenu par la réaction :
Cl2(g) + 2 OH- = ClO-(aq) + Cl- (aq) + H2O (l)
Expliquer pourquoi cette réaction peut se produire
2) Pourquoi les piscines n’ont-elles pas « l’odeur de chlore » ? Pourquoi l’utilisateur ajoute-t-il du sel ?
Mots clés, ou ce que je dois retenir de ce TP :

TP 8
QUELQUES APPLICATIONS DE L’ELECTROLYSE
TS Spécialité Chimie 2006/2007
Au bureau
Produits
Matériel
- solution de sulfate de cuivre à 1 mol.L-1
- solution saturée de chlorure de sodium
- pièces de centimes d’euros décuivrées
- une balance
Binôme élèves
Produits
Matériel
- eau distillée
- indigo
- phénolphtaléine
- générateur de tension continu de 12 V
- un rhéostat de 33Ω
- un multimètre
- un bécher de 200 mL
- un fil de cuivre
- une plaque de cuivre
- agitateur magnétique
- un chronomètre
- un tube en U sur support
- 2 électrodes en graphite
Préparation de la solution de sulfate de cuivre II à 1 mol.L-1
Peser g de cristaux de sulfate de cuivre II. Les introduire dans une fiole jaugée de 1L Ajouter de l’eau
distillée aux 2/3 en agitant pour homogénéiser. Compléter jusqu’au trait de jauge. Boucher et agiter
Préparation de la solution saturée de chlorure de sodium
Peser g de cristaux de chlorure de sodium . Les introduire dans une fiole jaugée de 1 L. Ajouter de l’eau
distillée aux 2/3 en agitant pour homogénéiser. Compléter jusqu’au trait de jauge. Boucher et agiter
1
/
4
100%