B. Étude cinématique

Classe : Tale S DS : Corrigé 10 Avril 08
- 1 -
Corrigé de l’exercice 1 : « L'hydrogène un combustible d'avenir »
Première partie : la fusion nucléaire contrôlée
1- Éléments et noyaux :
1.1 A représente le nombre de masse (nombre de nucléons). Z est le numéro atomique, il
correspond au nombre de proton.
1.2 Les isotopes d'un même élément chimique diffèrent par le nombre de neutrons que contient
leur noyau. (ils possèdent des nombres de nucléons différents ).
1.3 A=2 et Z=1, le noyau de deutérium contient un proton et un neutron.
1.4 Le tritium (A=3, Z=1) formé de un proton et deux neutrons. (Remarque : l’hydrogène est
aussi un isotope du deutérium, il contient 1 proton)
2- Réactions nucléaires :
Lors d’une transformation nucléaire, il y a conservation du nombre de nucléon, et conservation de
la charge électrique. Les deux réactions de fusion sont :
2 2 1 3
1 1 0 2
2 2 1 3
1 1 1 1
H H n He (noyau d'hélium formé)
H H p H (noyau de tritium formé)
3- Conditions :
3.1. D'après la loi de coulomb, des corps portant des charges électriques de même signe se
repoussent.
3.2. Les noyaux de deutérium et de tritium contiennent des protons. Ils sont porteurs de charges
électriques de signe positif.
4- Courbe d’Aston :
4.1. L’énergie de liaison El est l’énergie qu’il faut fournir au noyau pour le dissocier en ses
nucléons isolés et au repos.
4.2. Par définition
E
= m. c², où m représente le défaut de masse du noyau.
E
= [(Z.mP + (A–Z).mn) – mX] .c² où mP = masse d'un proton,
mn = masse d'un neutron,
et mX = masse du noyau
Pour le tritium
3
1H
:
E
= [(mP + 2mn)– m
3
1H
] .c²
méthode 1: On utilise les masses en u, que l'on convertit en kg. On obtient
E
en J, puis on
convertit en MeV.
E
= [(1,007 28 + 2 1,008 66) – 3,015 50] 1,660 54 10–27
(3,00108)²
E
= 9,110–3 1,660 54 10–27 (3,00108)²
E
= 1,3610–12 J
soit en divisant par 1,60 10–13,
E
= 8,50 MeV
méthode 2: On utilise l'énergie de masse de l'unité de masse atomique.
E
= [(1,007 28 + 2 1,008 66) – 3,015 50] 931,5
E
= 8,477 MeV Cette méthode est plus précise et plus rapide.
4.3. Les noyaux les plus stables, possèdent l'énergie de liaison par nucléon (
E
/A ) la plus grande.
Donc ils possèdent les valeurs de –
E
/A les plus basses. Voir zone hachurée sur la courbe ci-
après.

Classe : Tale S DS : Corrigé 10 Avril 08
- 2 -
4.4.1. place du tritium: Voir courbe.
4.4.2. Par lecture graphique approximative:
E
A
(
4
2He
)
– 7 MeV ;
E
A
(
3
1H
)
– 2,8 MeV et
E
A
(
2
1H
)
– 1,1 MeV
L'énergie libérée au cours de la réaction (3)
2
1H
+
3
1H
41
20
He n
, est égale à
Elibérée =
E
A
(
3
1H
)A
E
A
(
2
1H
)A –
E
A
(
4
2He
)A
Elibérée
2,8 3 + 2 1,1 – 4 7
Elibérée
–17,4 MeV
Le système fournit plus d'énergie qu'il n'en reçoit, il perd de l'énergie au cours de la fusion. Le milieu
extérieur reçoit donc cette énergie.
Deuxième partie : l’électrolyse de l’eau
1- Étude de l'électrolyse
1.1. La réaction qui a lieu dans l'électrolyseur nécessite une source d'énergie extérieure pour se produire
: cette réaction n'est pas spontanée.
1.2. La demi-équation électronique correspondant à la formation du dihydrogène fait intervenir le
couple H+(aq)/H2(g) , soit : 2 H+(aq) +2 e– = H2(g) ; O2 (g)+4H+(aq)+4e-=2H2O(l)
1.3. La formation du dihydrogène correspond à une réduction : cette réaction se déroule à la cathode.
1.4. Les électrons arrivent sur cette électrode, elle est donc reliée au pôle négatif du générateur.
2- Intensité du courant dans l'électrolyseur
2.1. D'après la demi-équation électronique : n(H2) = x
2.2. D'après la demi-équation électronique : ne = 2x
énergie reçue par les 2 petits
noyaux pour les séparer en leurs
nucléons isolés au repos
énergie cédée par le noyau d'hélium
lorsque les nucléons séparés s'assemblent
pour le former
E
A
–2,8
3
1H

Classe : Tale S DS : Corrigé 10 Avril 08
- 3 -
2.3. Soit Q la valeur absolue de la charge électrique transportée par ne électrons :
Q = ne .F, soit : Q = 2x.F
2.4. Par définition de l'intensité du courant électrique : I =
Q
t
.
On obtient : I =
2x.F
t
, soit : I =
2
2.n(H ).F
t
2.5. En faisant apparaître dans l'expression précédente le volume V(H2) de dihydrogène dégagé , on
obtient : I =
2
molaire
2.V(H ).F
V . t
Soit : I =
34
3
xx
x
2x5 10 x9,65 10
3,6 10 x25
= 1,1 x 104 A ou 11 kA
Schéma de principe de l'électrolyseur
Troisième partie : La pile à combustible :
1) 1. Les porteurs de charge à l'extérieur de la pile sont des électrons.
2. Le courant circule du pôle de la pile vers le pôle
à l'extérieur de la pile. Les électrons circulent en
sens opposé.
2) 1. couple H+(aq) /H2 (g) : 2 H+(aq) + 2 e- = H2 (g)
couple O2 (g)/H2O(l):O2 (g)+4H+(aq)+4e-=2H2O(l)
2. Equation: 2 H2 (g) + O2 (g) = 2 H2O(l)
3) 1. Une réduction est un gain d'électrons.
Le réactif qui est réduit est l'oxydant O2 , c'est le
"comburant" de la pile.
2. L'électrode où se produit la réduction s'appelle la
cathode.
Elle reçoit les électrons, c'est donc le pôle .
4) 1. n(H2) = m(H2) / M(H2) = 1 500 / 2,0 = 750 mol ; V(H2) = n(H2) . Vm = 750 x 24 = 1,8.104 L =
18 m3
2. Les gaz nécessaires à l'utilisation de cette pile occupent trop de place pour une voiture.
3. Pour occuper moins de place, on peut comprimer ces gaz , augmenter leur pression jusqu'à les
obtenir à l'état liquide. V= n.R.T/ P , en augmentant la pression P , on diminue le volume V.
5) 1. I = 200 A ; Q = I . t = 200 x 24 x 3600 = 1,73.107 C
2. Q = n(e-).F ; n(e-) = Q / F = 1,73.107 / 96 500 = 179 mol
D'après la demi-équation : 2 H+(aq) + 2 e- = H2 (g) , n(H2)cons = n(e-) /2 = 89,5 mol
Nom de l'électrode
Anode
Nature de la réaction :
Oxydation
Équation de la demi-
réaction :
O2 (g)+4H+(aq)+4e-
=2H2O(l)
Nom de l'électrode
Cathode
Nature de la réaction :
Réduction
Équation de la demi-
réaction :
2 H+(aq) +2 e– =
H2(g)
I
e
-
+
–
Solution
ionique

Classe : Tale S DS : Corrigé 10 Avril 08
- 4 -
2005 Réunion Exercice n°2 : Recherche d’un modèle de force de frottement ( points)
A. Exploitation de l’enregistrement
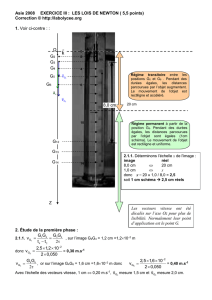
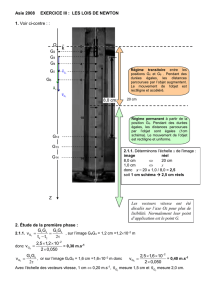
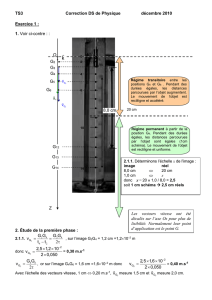
A-1. D’après le document 1, la trajectoire de la bille est une droite. D’après le document 2, la vitesse entre M15
et M21 est constante. Le mouvement de la bille est donc un mouvement rectiligne uniforme.
Ceci illustre la première loi de Newton ou principe d'inertie (vecteur vitesse constant implique que la somme
des forces extérieures est nulle)
A-2. Le caméscope prend des images au rythme de 50 images par seconde, soit une durée entre deux images de
1/50ème s = 0,020 s = 20 ms.
B. Étude cinématique
B-1. v6 =
57
57 tt yy
v6 =
3-
-3
10100)-(140 1041,0)-(69,0
= 0,70 m.s-1
B-2. Les vecteurs vitesses ont tous la même direction et le même sens (mouvement rectiligne), on peut
utiliser directement les normes : a18 =
1719
7191 tt vv
a18 =
3
10)340380(95,095,0
= 0 m.s-2
D’après la deuxième loi de Newton on a
amF
, donc la somme des forces extérieures appliquées à la bille
est nulle ce qui entraîne (première loi de Newton) que le mouvement est rectiligne et uniforme.
Le résultat obtenu est compatible avec la question A-1.
C. Étude dynamique
C-1. Dans un référentiel terrestre, supposé galiléen, la bille est soumise à son poids
P
,
à la poussée d’Archimède
A
P
et aux forces de frottements
f
C-2. m = AV
convertir V en m3 m = 0,5210–6×7850 = 4,1×10-3 kg = 4,1 g
C-3. PA = mH×g = HV×g
PA = 920 0,5210–6×9,8 = 4,7×10–3 N
D. Équation différentielle du mouvement de la bille
D-1. Théorème du centre d’inertie (deuxième loi de Newton) : dans un référentiel galiléen, la somme
vectorielle des forces extérieures appliquées à un solide de masse m, est égale au produit de cette masse par le
vecteur accélération de son centre d’inertie. Soit
GA amfPP
En projetant sur l’axe vertical représenté sur le document n°1 il vient : P – PA – f = m×aG = m×
dt
dv
En divisant par m on a :
dt
dv
+
m
f
=
mPP A
= A car P, PA et m sont des constantes.
D-2. A =
mPP A
=
mPgm A
=
VgVgV
A
HA
= g
A
HA
A = 9,8
7850
9207850
= 8,7 m.s-2
Pour t = 0 s, v = 0 alors f = 0 N donc
dt
dv
= A La constante A est homogène à une accélération.
E. Recherche de modèles pour la force de frottement
E-1. Première hypothèse : f = k1.v
E-1.a) On a :
dt
dv
+
m
f
= A soit
dt
dv
+
m
.vk1
= A
On a bien
dt
dv
+
.vB1
= A avec B1 =
m
k1
E-1.b) Quand la vitesse limite est atteinte, cette valeur est constante, donc
dt
dv
=0
f
A
P
P

Classe : Tale S DS : Corrigé 10 Avril 08
- 5 -
B1.vlim = A donc B1=
lim
vA
Et B1 =
m
k1
soit k1 = m.B1 = m
lim
vA
k1 =
95,0 7,8
101,4 3
= 3,7×10–2 kg.s-1 car A en m.s–2, vlim en m.s–1, m en kg
calcul effectué avec la valeur non arrondie de A
E-2. f = k2.v² et
dt
dv
+ B2 . v² = A
quand v = vlim alors
dt
dv
= 0 B2 . vlim² = A B2 =
2
lim
vA
B2 =
m
k2
(même raisonnement que pour la
question E-1.a) soit
2
lim
vA
=
m
k2
k2 =
2
lim
v
A
m
k2 =
2
395,0 7,8
101,4
= 4,0×10–2 kg.m-1 car A en m.s–2 , vlim² en m².s–2 et m en kg
E-3. Pour 0
v
0,8 m.s–1, il semble que le modèle 1 convienne mieux.
Pour 0,8
v
1 m.s–1, il semble que ce soit le modèle 2 qui convienne.
EXERCICE III : ÉTUDE DE QUELQUES ÉNERGIES RENOUVELABLES 4 points
Partie I : L'énergie éolienne
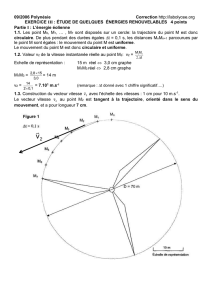
1.1. Les point M0, M1, … , M7 sont disposés sur un cercle: la trajectoire du point M est donc
circulaire. De plus pendant des durées égales t = 0,1 s, les distances MnMn+1 parcourues
par le point M sont égales : le mouvement du point M est uniforme.
Le mouvement du point M est donc circulaire et uniforme.
1.2. Valeur v2 de la vitesse instantanée réelle au point M2: v2 =
13
2
MM
.t
Echelle de représentation : 15 m réel 3,0 cm graphe
M1M3 réel 2,8 cm graphe
M1M3 =
2,8 15
3,0
= 14 m
v2 =
,
14
2 0 1
= 7.101 m.s-1 (remarque : t donné avec 1 chiffre significatif….)
1.3. Construction du vecteur vitesse
2
v
avec l'échelle des vitesses : 1 cm pour 10 m.s-1.
Le vecteur vitesse
2
v
au point M2 est tangent à la trajectoire, orienté dans le sens du
mouvement, et a pour longueur 7 cm.
1.4. La vitesse v du point M est égale à la distance parcourue par le point M pour faire un
tour, soit 2..R = .D, divisée par la durée T d'un tour: v =
.D
T
T =
.D
v
T =
.
1
70
7 10
= = 3,1 s = 3 s (en conservant 1 chiffre significatif…)
2. T est la période de rotation de la pale. La fréquence de rotation est alors : f =
1
T
avec f en
Hz si T en s : f =
1
= 3.10–1 Hz. La fréquence f représente "le nombre de tours" en une
seconde.
Le nombre de tours effectués en une minute (60 s) est : 60 f
soit 60
1
= 1,9.101 tr.min-1 = 2.101 tr.min-1
 6
6
 7
7
 8
8
1
/
8
100%