Nodules et cancers thyroïdiens

Texte du Collège des enseignants d’Endocrinologie-diabétologie-nutrition
Complété par Olivier Chabre et annoté par Sophie Ribotta
1. LES NODULES THYROÏDIENS :
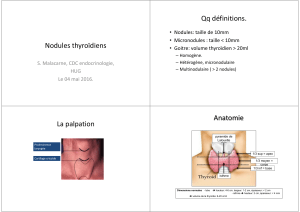
1.1. Définition :
C'est une notion clinique : tuméfaction cervicale inférieure mobile à la déglutition avec le reste
du corps thyroïde.
TYPE DU NODULE
REMARQUE ET EVOLUTION
FREQUENCE, CONTEXTE
Tumeurs vraies bénignes
Adénome (vésiculaire, à cellules
oxyphiles, kystique), kyste
Stable ou lentement évolutif
Adénome parathyroïdien inclus
Très fréquent, c'est la forme habituelle qui sous-
tend le terme de "nodule"
85 % sont peu ou pas fonctionnel (« froid » à la
scintigraphie)
15 % sont fonctionnels (« chaud » à la
scintigraphie) et parfois autonome ou toxique
(extinctif à la scintigraphie)
Très rarement palpables. Responsable
d’hyperparathyroidie Ire (hypercalcémie)
Pseudonodule
inflammatoire
Thyroïdite subaiguë
Réversible
Thyroïdite lymphocytaire chronique
réversible
Thyroïdite aiguë septique
Germes, mycobactéries, réversible
Assez fréquent, viral
Fréquent, auto-immune
Très rare, Malformation sinus piriforme
Tumeurs malignes
thyroïdiennes
CSV (cancer de souche vésiculaire)
- différencié : papillaire (fréquent)
ou vésiculaire évolutif
- , indifférencié anaplasique, (rare)
très évolutif
CMT : cancer médullaire (cellule C),
évolutif
CSV : rare, si le nodule cancéreux est le signe
d'appel (1 à 5 %) ; les microcarcinomes
papillaires (< 10 mm) sont par contre assez
fréquents (3 à 10 %)
CMT : rare, spontané ou familial
Biologie : calcitonine, génétique : mutation du
gène RET
Autres tumeurs
Lymphomes, sarcomes, métastases
Intrathyroïdiennes
Evolutifs
Très rares
Tableau 1
NODULES ET CANCERS THYROIDIENS

1.2. EPIDEMIOLOGIE POSITION DU PROBLEME :
Très grande fréquence : nodules cliniques palpables dans 4 à 5 % de la population
générale, nodules infra cliniques mis en évidence à l'échographie dans plus de 50 % de la
population de 60 ans. La fréquence des nodules augmente avec l'âge, les femmes sont plus
touchées que les hommes.
La découverte d'un nodule thyroïdien pose le problème du dépistage du cancer thyroïdien,
sachant qu'actuellement seuls 5 à 10 % des nodules opérés sont des cancers, la proportion étant
beaucoup plus faible pour les nodules échographiques, mais sachant également tout l'intérêt de
traiter un cancer thyroïdien au stade précoce de nodule isolé sans métastases.
La grande question actuelle est d'améliorer la stratégie diagnostique des nodules
thyroïdiens dans le but de respecter une lésion bénigne et de traiter au plus tôt un cancer.
1.3. Ainsi, la découverte clinique d'un nodule entraîne la recherche d'arguments en faveur de la
malignité
Par l'interrogatoire et l'examen :
Terrain : jeune âge ou à l'opposé patients de plus de 60 ans avec un nodule isolé, sexe
masculin. ATCD personnels d'irradiation du cou, actuellement traitement du Hodgkin, du
cancer du sein, des cancers ORL
ATCD familiaux de cancers thyroïdiens qui font évoquer le carcinome médullaire et le
syndrome de Sipple ou NEM2 (association cancer médullaire de la thyroïde, phéochromocytome,
hyperparathyroïdie) mais il existe aussi des familles de cancer papillaires et de cancers oxyphiles
Signes cliniques locaux : nodule de plus de 3 cm, dur, douloureux, adhérent aux structures
de voisinage, présence d'adénopathies cervicales (cf Figure 1), signes de compression ou
d'irritation locale.
Signes cliniques généraux qui font rechercher un cancer médullaire : diarrhée motrice,
flush.
Par les examens complémentaires
Le dosage de la TSH pour repérer les nodules toxiques ou prétoxiques (TSH basse :
nodule probablement chaud à vérifier en scintigraphie d'emblée, ce caractère fonctionnel avec
extinction du parenchyme adjacent n'étant qu'exceptionnellement associé à un cancer)
Le dosage de la calcitonine marqueur du cancer médullaire à demander en cas de
symptôme et pour certains au moins 1 fois devant tout nodule. La place de cette exploration n’est
pas encore consensuelle : son grand interêt est qu’elle permet le diagnostic de tous les cancers
médullaires, l’inconvénient est le très faible « rentabilité » de l’examen (cancer médullaire très
rare) et la difficulté d’interprétation des taux faibles de calcitonine (diagnostic différentiel
difficile entre microcarcinome médullaire et simple hyperplasie des cellules C)
Echographie : un cancer est plus volontiers mal limité, hypoéchogène siège de petites
calcifications mais aucun critère échographique n'est suffisamment fiable pour permettre un
diagnostic de malignité.

On attendra de l'échographie :
la mesure exacte de la taille du nodule : indication chirurgicale pour les nodules solides de
plus de 3 cm ; permettant une surveillance longitudinale pour les nodules plus petits
le diagnostic entre kyste d'aspect liquidien et nodule plein ou remanié
la recherche de nodules infra cliniques associés faisant poser le diagnostic de goitre
multinodulaire plutôt que de nodule isolé.
Scintigraphie : seuls les nodules froids sont suspects de cancers mais ils représentent 85
% des nodules palpés. Le caractère non fixant n'est donc pas suffisamment sensible pour donner
des arguments en faveur de la malignité. La scintigraphie est donc plutôt un examen réservé aux
nodules avec TSH basse.
L'examen clef est la ponction cytologique à l'aiguille fine. On ponctionne les nodules
cliniques ou suspects en échographie, la limite est en général d'1 cm. La ponction permet
d'analyser des cellules issues du nodule. Parfois elle permettra aussi d'évacuer un kyste.
Sous réserve d'une technique et d'une interprétation fiable et validée, celle-ci donnera 4 types de
résultats : bénin probable permettant de respecter le nodule, malin indiquant formellement la
chirurgie, douteux notamment dans les lésions vésiculaires ou à cellules de Hurtle faisant discuter
la chirurgie (un diagnostic est nécessaire une lésion douteuse ne peut être en général laissée en
place), ininterprétable nécessitant une nouvelle ponction.
Dans les nodules laissés en place, la ponction thyroïdienne sera renouvelée pour
augmenter la fiabilité du diagnostic.
Au total on peut proposer une stratégie diagnostique qui repose essentiellement sur la
cytoponction lorsque la TSH est normale (Figure 1)

1.4. Traitement :
Le traitement médical des nodules par hormones thyroïdiennes à dose frénatrice est peu
efficace. Il peut être discuté à titre de test, son résultat ne constitue pas un argument permettant de
réfuter une étiologie maligne.
Le traitement chirurgical consiste en une loboisthmectomie du côté du nodule avec
examen extemporané ou examen anatomo pathologique ultérieur qui décidera en fonction des
résultats (cancer ou non ) et des facteurs pronostiques de gestes complémentaires: (totalisation,
curage, iode 131).
1.5. Surveillance :
Tout nodule laissé en place requiert une surveillance longitudinale clinique devant s'assurer de la
stabilité des lésions.
Figure 1 : STRATEGIE DIAGNOSTIQUE DEVANT UN NODULE THYROIDIEN
Certains auteurs proposent en plus un dosage de la calcitonine
TSH
Basse
(< 0,01)
Normale
Scintigraphie
Cytoponction
Non
représentative
20 %
Maligne
ou douteuse
20 %
Bénigne
60 %
Pas de
fixation sur le
nodule
Fixation élective sur
un nodule
Chirurgie
ou Traitement
par iode131
Nodule
toxique
Chirurgie
Surveillance
Traitement
médical
Nodule thyroïde > 1 cm
Hyperthyroïdie
+
Nodule « froid »

2. LES CANCERS THYROÏDIENS (ETIOLOGIE DES NODULES DE LA THYROÏDE) :
C'est un cancer rare, son incidence dans le registre des cancers de la thyroïde des département de
la Marne et des Ardennes est de :
5,57/100 000/an chez les femmes et de 1,67/100 000/an chez les hommes :
2.1. Anatomie pathologique (voir annexe) :
2.2. Les cancers différenciés de la thyroïde :
2.2.1. Définition, épidémiologie :
Ils se développent à partir de cellules thyroïdiennes vésiculaires (= thyréocytes). Prédominent
chez l'adulte jeune : âge moyen 45 ans, exceptionnel avant 10 ans. Prédominance féminine 2/1.
Les irradiations cervicales dans l’enfance sont un facteur de risque. On distingue les carcinomes
(>10mm) des microcarcinomes (<10mm) : ceux-ci sont beaucoup plus fréquents que les
carcinomes (5 à 36% des adultes à l’autopsie) et ils ont un potentiel évolutif très faible.
Ils représentent 80 % environ existent sous deux
formes :
- cancer papillaire (voir figure 2) : 70 % des
cancers thyroïdiens. Papilles : axe conjonctivo-
vasculaire bordé d’une couche de cellules. Celles-ci
ont des anomalies nucléaires caractéristiques. Cancer
souvent multifocal. Evolution généralement lente et
loco-régionale : intra-thyroïdienne et lymphatique :
30 à 65% des patients ont des métastases
ganglionnaires cervicales lors du diagnostic. Plus
rarement métastases pulmonaires : en général
miliaire plus rarement tumeurs nodulaires.
Figure 2 : Volumineuse métastase
ganglionnaire d’un cancer thyroïdien
papillaire. Cette adénopathie jugulo-
carotidienne gauche est en rapport avec
un cancer papillaire du lobe gauche de
petite taille (non visible sur la
diapositive). Les adénopathies
métastatiques sont souvent plus petites.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%