Isolement et Etude de quelques Entérobactéries pathogènes dans

RÉPUBLIQUE ALGÉRIENNE DÉMOCRATIQUE ET POPULAIRE
MINISTÈRE DE L’ENSEIGNEMENT SUPÉRIEUR ET DE LA RECHERCHE SCIENTIFIQUE
Université des Frères Mentouri Constantine
Faculté des Sciences de la Nature et de la Vie
Département : Microbiologie :
Mémoire présenté en vue de l’obtention du Diplôme de Master
Domaine : Sciences de la Nature et de la Vie
Filière : Sciences Biologiques
Spécialité : Microbiologie Générale et Biologie Moléculaire des Microorganismes
Intitulé :
Jury d’évaluation :
Présidente du jury : Mme BOUBEKRI K. (MCA - UFM Constantine)
Rapporteur : Mme BOUZERAIB L. (MAA - UFM Constantine)
Examinatrice : Melle MEZIANI M. (MAA - UFM Constantine)
Année universitaire
2015 - 2016
Isolement et Etude de quelques Entérobactéries pathogènes
dans les eaux usées d’Oued Boumerzoug à Constantine
Présenté et soutenu par
:
SAVADOGO Mahamadi
Le
:
2
8
/06/2016
BOUBKEIR Youssouf

Remerciements
Nous remercions tout d’abord Allah Le Tout Puissant pour nous avoir accordé la santé,
l’énergie et l’opiniâtreté nécessaire à la réalisation de ce modeste travail.
Nous remercions très singulièrement notre encadreur Mme BOUZERAIB L. pour avoir
accepté diriger ce travail, pour ses conseils , son aide, ses suggestions sur la rédaction
de ce mémoire ainsi que la confiance qu'elle nous a témoigné tout au long de cette
étude. Tout au long de la réalisation de ce mémoire, nous avons pu apprécier son
enthousiasme, son savoir-faire, sa pédagogie, son sens de communication. Vous avez été
la quand nos milieux de culture faisaient défauts et nous avons pu apprécier ensemble la
bonne odeur de certaines bactéries. Merci pour tous ces bons moments.
Nous adressons également nos remerciements à :
- Mme BOUBEKRI K. Maître de conférences à l’UFM-Constantine pour l’honneur
qu’elle nous fait de présider ce jury.
- Melle MEZIANI M. Maître assistante à l’UFM-Constantine d’avoir accepté
d’apporter son jugement à ce travail.
Nous remercions aussi nos pays, qui ont bien voulu nous accorder cette bourse d’étude. Nos
plus sincères gratitudes vont vers ce beau pays, l’ALGERIE, qui nous a accueillis et suivi
tout au long de notre parcours.
Nous saisissons cette occasion pour exprimer nos profonds respects et notre reconnaissance à
l’ensemble du corps enseignant de la faculté des Sciences de la Nature et de la Vie plus
particulièrement celui de la spécialité Microbiologie, pour avoir participé à notre
formation graduée.
Merci à Mme ZOGHMAR S. responsable du laboratoire de microbiologie N°11 de la Faculté
et son équipe, à Mme BOUZIDI N. et Mr SLOUGHI S. du laboratoire de biologie
moléculaire qui nous ont beaucoup aidés tout au long de notre travail.
Enfin, nous adressons nos plus sincères remerciements à nos parents, nos amis, nos
camarades ainsi que tous ceux qui nous ont toujours soutenus et encouragés au cours de la
réalisation de ce mémoire.

Dédicace
Je ne peux adresser les prémices de cette dédicace qu’à mes parents,
premiers piliers de mon éducation, vous m’avez soutenu depuis mes débuts
jusqu’à maintenant par vos bénédictions.
A ma chère mère
Aucun mot, aussi expressif qu’il soit, ne saurait remercier sa juste valeur .Puisse
Allah vous garder longtemps auprès de nous et vous bénir infiniment.
A la mémoire de mon père, paix à son âme.
A mon oncle, El Hadj Harouna OUEDRAOGO appelé aussi « Papa » pour tous les
efforts qu’il a effectué et qu’il continue d’effectuer pour la bonne marche de mes
études. Merci Papa.
A mes frères et sœurs Abdoul Salam, Idrissa, Balkissa et Mariam pour leur
encouragement, leur sacrifice qui m’ont permis d’aller de l’avant.
A toute la communauté Burkinabè à (Salo H., Tamboura A., Ouédraogo F.,
Ouédraogo I., Bambara I., Zallé R...)
A mes professeurs de la faculté de SNV (Dr. Arabet D…)
A toute la communauté des étudiants étrangers à Constantine (en particulier
Malienne)
A tous mes amis algériens Akram, Yahia, Meriem, Asma, Sara qui ont
fait de mon séjour en Algérie un paradis sur terre. Merci à vous.
Enfin à tous ceux ou celles que j’ai eu l’immense plaisir de côtoyer.
Merci à vous tous
Mahamadi SAVADOGO

Dédicace
Je dédie ce travail :
A mes très chers parents, que Dieu me les gardent et protègent.
A mes frères et sœurs.
A toute ma famille.
A tous mes amis sans citer les noms.
Youssouf BOUBKEIR

Résumé
Les eaux usées sont susceptibles de renfermer et de véhiculer une grande variété d’agents
pathogènes pour l’homme. Les organismes pathogènes présents dans les eaux usées d’une
collectivité, en reflètent l’état sanitaire.
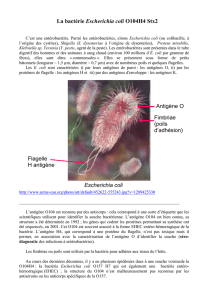
Les entérobactéries représentent une des principales familles de bacilles à Gram négatif
se retrouvant partout y compris les eaux usées. Ce sont les plus impliquées en pathologie
infectieuse humaine surtout en milieu hospitalier.
Notre travail s’inscrit dans le cadre de la recherche et l’étude de quelques entérobactéries
pathogènes dans les eaux usées d’oued Boumerzoug. Ainsi une évaluation préalable de la
FTAM a été effectuée sur nos échantillons avant de procéder à des isolements sur milieux
spécifiques ainsi qu’une identification par des méthodes microbiologiques standardisées puis
une réalisation de profils électrophorétiques de l’ADN total des souches identifiées.
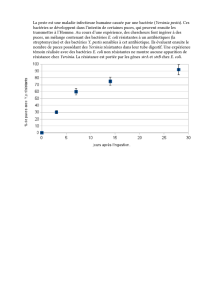
Sur trois échantillons étudiés, les résultats de la FTAM varient entre 1.14 106 et 13.8 106
UFC/ml qui témoignent d’une charge microbienne importante des eaux usées. Quant à
l’isolement, sur un total de quatre germes recherchés, nous avons pu isoler et identifier 3
souches d’E. coli et une absence de Salmonella spp. , Shigella spp. et Yersinia enterocolitica a
été observée. Par contre d’autres germes ont été isolés comme Proteus mirabilis, Proteus
morganii, Enterobacter agglomerans et Pseudomonas sp. . Les profils électrophorétiques de
l’ADN total des souches identifiées ont été aussi obtenus.
La presente étude nous a permis de récolter des données locales relatives à la présence de
pathogènes et des indicateurs de contamination fécale tels qu’E. coli. et une contribution à
l’extraction de l’ADN total des souches isolées.
Mots clés : Entérobactéries, eaux usées, Oued Boumerzoug, FTAM, isolement
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
 80
80
 81
81
 82
82
 83
83
 84
84
 85
85
 86
86
 87
87
 88
88
 89
89
 90
90
 91
91
 92
92
1
/
92
100%