Article en pdf - Université de Liège

Reflexions, le site de vulgarisation de l'Université de Liège
© Université de Liège - http://reflexions.ulg.ac.be/ - 20 April 2017
- 1 -
Antibiotiques contre bactéries
11/03/08
Suite à la publication d'un rapport d'experts, l'Union européenne, jusque là très engagée dans le financement
de la recherche de nouvelles molécules d'antibiotique, a fait quelque peu marche arrière. Ce rapport estime
qu'il vaut mieux empêcher les souches résistantes de se répandre plutôt que d'investir de l'argent public dans
la recherche de nouveaux antibiotiques. Jean-Marie Frère et d'autres scientifiques européens répliquent dans
un article (1) publié par The Lancet : il faut certes tout faire pour empêcher les souches résistantes de se
répandre, mais il faut aussi garder une réplique d'avance sur le monde des bactéries. L'occasion de faire le
point sur une lutte sans merci : bactéries contre antibiotiques.
Lorsque l'Union européenne a lancé son 6ème programme-cadre de recherche, elle a fait la part belle
à un important projet d'étude des mécanismes de défense des bactéries face aux antibiotiques. Ce
programme, appelé EUR-INTAFAR, a démarré en février 2005 et se poursuit encore aujourd'hui. Il rassemble
16 laboratoires de recherche disséminés à travers toute l'Europe et est coordonné par l'Université de Liège,
plus particulièrement par Jean-Marie Frère, le directeur du Centre d'Ingénierie des Protéines de l'ULg.

Reflexions, le site de vulgarisation de l'Université de Liège
© Université de Liège - http://reflexions.ulg.ac.be/ - 20 April 2017
- 2 -
Depuis le démarrage de ce projet, un groupe d'experts a remis un rapport au parlement européen : Scientific
Technology Options Assessment (STOA) report on antibiotic resistance (2). Ils y prônent l'abandon du
financement public de la recherche en la matière au profit du développement de la lutte contre la prolifération
des souches bactériennes résistantes. A la suite de ce rapport, l'Union a affectivement diminué ses aides à la
recherche dans le secteur. Pour Jean-Marie Frère et ses collègues engagés dans cette lutte, c'est une erreur.
Certes, il faut tout faire pour empêcher la prolifération des souches résistantes mais il faut aussi poursuivre la
recherche pour garder une longueur d'avance sur les bactéries qui ne cessent de s'adapter et de développer
de nouvelles défenses : l'expansion spectaculaire des maladies nosocomiales en est une preuve.
Or, estime Jean-Marie Frère, ce sont les pouvoirs publics qui doivent financer ce type de recherche, et non
l'industrie pharmaceutique. «Le marché global des antibiotiques est passé de 22,6 milliards de dollars en 1996
à 26,9 en 2005 et il devrait être de 28,9 milliards de dollars en 2008, constate Jean-Marie Frère. C'est donc un
marché en croissance. Pourtant, l'industrie est en train d'en sortir depuis 1989. Pour s'en convaincre, il suffit
de regarder le nombre de nouvelles molécules approuvées par la FDA (ndlr : Food and Drug Administration,
organisme américain qui délivre les autorisations de mise sur le marché des nouveaux médicaments) par
période de 5 ans. Cela traduit le fait que beaucoup de grandes firmes sont sorties du domaine. S'il faut investir
des sommes importantes dans la recherche -environ 800 millions d'euros pour un nouvel antibiotique-, elles
préfèrent le faire dans des maladies chroniques puisque le malade sera obligé de prendre le médicament tous
les jours le restant de sa vie. C'est une rente. Or, les règles, les procédures d'agréation de la FDA sont les

Reflexions, le site de vulgarisation de l'Université de Liège
© Université de Liège - http://reflexions.ulg.ac.be/ - 20 April 2017
- 3 -
mêmes dans un cas comme dans l'autre. Un mouvement de contestation existe d'ailleurs aujourd'hui car on
estime qu'il est ridicule d'exiger le même degré de sécurité pour un médicament pris tous les jours pendant
des années et un antibiotique que, d'habitude, on ne prend que pendant quelques jours.»
(1) Chopra I, Schofield C, Everett M, O'Neil A, Miller K, Wilcox M, Frère J-M, Dawson M, Czaplewski L,
Urleb U, Courvalin P. Treatment of health-care-associated infections caused by Gram-negative bacteria : a
consensus statement. The Lancet infectious deseases, Vol 8, February 2008.
(2) Baquero F, Coast J, Frimodt-Moller N, Ropars A-L, Moller Aarestrup F. Antibiotic resistance. Brussels:
Scientific and Technological Options Assessment, 2006. http://www.europarl.europa.eu/stoa/
publications/studies/stoa173_en.pdf (accessed Dec.3, 2007)
175.000 morts chaque année en Europe
Mais pourquoi continuer la lutte ? Même si les efforts réalisés chez nous dans les hôpitaux commencent à
porter des fruits, la situation reste préoccupante et, surtout, elle n'est pas la même partout. Selon l'article
du Lancet, chaque année, en Europe, environ 2 millions de patients hospitalisés attrapent une infection
nosocomiale, fatale pour environ 175.000 d'entre eux. «Sans oublier, précise Jean-Marie Frère, un surcoût
important pour les systèmes de sécurité sociale : un malade infecté doit rester environ une à deux semaines
de plus à l'hôpital». Et si le Nord de l'Europe est plus épargné que le Sud, c'est encore pire ailleurs, en Afrique
et en Chine particulièrement.
Comment expliquer cette résistance? La différence d'un pays à l'autre fournit déjà un élément d'explication :
elle dépend essentiellement de l'utilisation des antibiotiques. Si celle-ci est raisonnable et rationnelle, elle
reste dans des limites correctes. Dans le cas contraire, des taux de résistance importants sont atteints. Il
est admis aujourd'hui que plus on prescrit des antibiotiques, plus on accroît la résistance des bactéries. Un
phénomène dont médecins et patients se partagent la responsabilité. Les uns prescrivent, mais les autres
exercent souvent une très forte pression pour qu'il en soit ainsi et ne suivent pas les prescriptions en arrêtant
le traitement trop tôt.

Reflexions, le site de vulgarisation de l'Université de Liège
© Université de Liège - http://reflexions.ulg.ac.be/ - 20 April 2017
- 4 -
Il existe un autre facteur explicatif : la disponibilité des différents types d'antibiotiques. Si on ne se base que
sur un seul antibiotique ou une seule classe, la résistance à ceux-ci augmente vite. Dans certains pays par
contre, comme aux Pays-Bas, il existe un système de «cyclage» dans les hôpitaux. En routine, un ou deux
antibiotiques sont utilisés ; quand la résistance augmente, d'autres prennent leur place. Ce n'est évidemment
pas possible dans tous les pays, particulièrement dans les pays les plus pauvres.
Enfin, un dernier facteur explique la résistance des bactéries, mais il est en voie de disparition en Europe :
l'utilisation des antibiotiques dans l'alimentation du bétail. Il existe certes un risque, mineur, de contamination
de l'homme par des traces d'antibiotique qui subsisteraient par exemple dans le lait ou la viande. Mais le vrai
danger est la sélection de souches résistantes chez l'animal, lesquelles peuvent être transférées à l'homme.
Ou du moins, elles peuvent transférer leurs caractéristiques de résistance à des bactéries pathogènes
humaines.
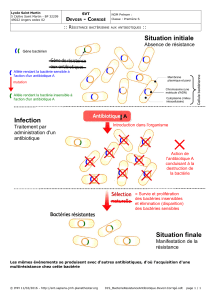
La sélection des plus aptes
Exercer une pression environnementale quelconque -et l'administration d'antibiotiques en est une-, se traduit
par la sélection des plus aptes. Chez les bactéries, cela se fait très rapidement à cause de leur vitesse
ahurissante de reproduction. Si un événement a une chance sur un milliard de se produire, il va se passer
puisque, en quelques heures, une seule bactérie va en donner un milliard d'autres si les conditions de culture
sont bonnes. Pour rare qu'elle puisse être, la mutation d'une bactérie non résistante en bactérie résistante
se produit donc fréquemment.

Reflexions, le site de vulgarisation de l'Université de Liège
© Université de Liège - http://reflexions.ulg.ac.be/ - 20 April 2017
- 5 -
Les modes d'acquisition de la résistance sont, pour l'essentiel de deux types. Le premier est la sélection de
souches qui possèdent des caractères de résistance originaux. On voit aujourd'hui apparaître des souches
qui fabriquent des enzymes de résistance qu'on n'avait jamais vus auparavant, ni eux ni de proches parents.
Des enzymes, appelés Béta-lactamases, qui détruisent les pénicillines sont ainsi apparus. Bien entendu,
ces enzymes s'adaptent eux-mêmes aux familles d'antibiotiques : au cours de ces dernières années, à
l'introduction des céphalosporines (une famille de pénicillines), a répondu l'apparition de mutants d'enzymes
connus. Mais on a aussi vu sélectionner des enzymes tout à fait différents, avec seulement 25 à 30%
d'acides aminés communs avec ceux qu'on connaissait. Ils ne peuvent donc pas descendre de l'hôte par
des mutations récentes. «La divergence génétique s'est faite il y a sans doute plusieurs milliers d'années,
explique Jean-Marie Frère. Ces enzymes ont été trouvés dans des bactéries non pathogènes présentes dans
l'environnement. Personne ne s'explique pourquoi certains microorganismes possèdent naturellement ces
gènes de résistance car la concentration naturelle d'antibiotiques dans la nature est faible. Tellement faible
d'ailleurs, que Fleming lui-même disait que fabriquer la pénicilline est si difficile et si long que les résultats ne
justifiaient pas les efforts nécessaires pour l'obtenir …»
L'autre mécanisme de mutation est le transfert horizontal entre espèces. C'est un problème nouveau et qui
peut se révéler important pour l'homme. Lorsqu'un malade avale une dose d'antibiotique, une bonne partie
se retrouve dans l'intestin. La prise d'antibiotiques y favorise donc la sélection de bactéries non pathogènes
résistantes puisque les autres ont été éliminées. Mais il arrive que l'une ou l'autre bactérie pathogène -elles ne
sont jamais toutes tuées par l'antibiotique- hérite des caractères de résistance. Ceux-ci vont alors se répandre
dans les bactéries pathogènes qui vont devenir insensibles à l'action des antibiotiques. C'est ce qui se passe
dans les hôpitaux où des champions de la résistance finissent par être sélectionnés.
Une panoplie complète
Comprendre comment les bactéries les plus aptes passent leurs caractéristiques aux autres est une chose.
Mais comment sont-elles devenues aptes à se défendre contre les antibiotiques ? Elles ont recours à quatre
grands mécanismes selon l'antibiotique utilisé : elles détruisent l'antibiotique, elles se déguisent pour qu'il ne
les reconnaisse pas, elles l'empêchent d'entrer ou s'il entre, elles le rejettent dehors !
 6
6
 7
7
1
/
7
100%