L`élément cuivre dans tous ses états

Thème Univers : CH 3 : Activité expérimentale :
L'ELEMENT CUIVRE DANS TOUS SES ETATS...
Notion contenu
Compétences
- Éléments chimiques.
- Pratiquer une démarche expérimentale pour vérifier la
conservation des éléments au cours d’une réaction chimique.
- Savoir suivre un protocole, faire le schéma. Interpréter
les résultats.
- Respecter les consignes.
Objectif de l’activité: Voir comment l’élément cuivre se conserve au cours d’une série de réactions chimiques.
Compétences notées: Vous ferez les schémas et observations des réactions chimiques que vous réaliserez au
cours de l’activité en respectant le protocole. Et vous donnerez la conclusion au § VII.
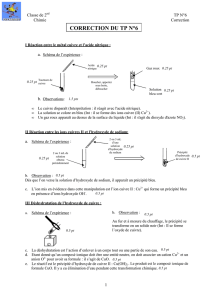
I. Réaction entre la solution d'acide nitrique et un copeau de cuivre.
1. Etat physique et formule des réactifs.
a) le cuivre.
L'observation d'un copeau de cuivre montre qu'il s'agit d'un métal de couleur rouge.
Si l'on admet que le métal est constitué par un empilement régulier d'atomes identiques, la formule du cuivre est Cu.
b) l'acide nitrique.
Pur, l'acide nitrique est un liquide incolore de formule HNO3.
Sa dissolution dans l'eau s'accompagne d'une dissociation faisant apparaître deux ions :
- l'anion nitrate de formule NO3- .
- le cation Hydrogène de formule H+.
L'ion responsable des propriétés acides de la solution est l'ion H+.
2. Expérience et observations.
Protocole : Mettre un copeau de cuivre dans un tube à essai et verser 2 à 3 mL d’acide nitrique.
Schéma :
Observation :
- Il se forme un gaz roux.
- La solution se colore en bleu.
- Le copeau de cuivre disparait.
3. Interprétation.
Information: l'acide nitrique agit ici à la fois par ses ions H+ et NO3-. Le gaz formé initialement n'est pas du dioxyde
d'azote roux, mais du monoxyde d'azote incolore. Dès sa formation, ce dernier est oxydé par le dioxygène de l'air en
dioxyde d'azote.
Ecrire l'équation bilan de la réaction qui conduit à la formation du monoxyde d'azote, sans chercher à l'équilibrer (les
coefficients vous seront donnés).
8 H+ + 2 NO3- + 3 Cu 3 Cu2+ + 2 NO + 4 H2O
Ecrire l'équation bilan de l'oxydation du monoxyde d'azote en dioxyde d'azote.
NO + ½ O2 NO2
4. Pour continuer... Récupérer la solution obtenue précédemment dans un autre tube à essai.
Copeau de
cuivre
Acide
nitrique
Gaz roux

II. Réaction entre la solution de soude et l'ion cuivre II.
1. Rappels sur l'hydroxyde de sodium.
L'hydroxyde de sodium est un solide ionique de formule NaOH.
Sa dissolution dans l'eau conduit à la dispersion de deux ions :
- l'anion hydroxyde de formule OH-.
- le cation sodium de formule Na+
Cette solution est incolore (couleur).
2. Expérience et observations.
Protocole : Verser de l’hydroxyde de sodium NaOH dans le tube à essai contenant la solution précédente.
Schéma :
Observation :
- Il se forme un précipité bleu.
3. Interprétation.
Ecrire l'équation bilan de la réaction observée. Nommer le produit
obtenu : hydroxyde de sodium.
Cu2+ + 2 OH- Cu(OH)2
4. Pour continuer...
Quelle méthode vous permettrait de recueillir le précipité
précédent ? La filtration.
Représenter à l'aide d'un schéma les opérations à réaliser.
Réalisez cette opération. Et placer du précipité à l’aide de
l’agitateur en verre, au fond d’un tube.
III. Déshydratation de l'hydroxyde de cuivre II.
1. Expérience et observations.
Protocole : A l'aide du chauffage électrique, chauffer avec précaution le tube à essai contenant l'hydroxyde de cuivre II
jusqu'à disparition de la couleur bleue.
Schéma :
Observation :
- Le précipité noircit.
Solution
précédente
contenant des
ions Cu2+
Solution
d’Hydroxy
de sodium
Précicpité
bleu
Filtrat
Précipité
Précipité
Four

2. Interprétation.
La déshydratation correspond à l'élimination d’ eau sous forme de vapeur.
Comment aurait-on pu la mettre en évidence ? sulfate de cuivre anhydre.
Information : le produit noir obtenu est un solide ionique formé des ions Cu2+ et O2-.
Ce solide se nomme oxyde de cuivre II et il a pour formule CuO.
Ecrire l'équation bilan de la réaction de déshydratation de l'hydroxyde de cuivre II.
Cu (OH)2 CuO + H2O
IV. Réaction entre l'oxyde de cuivre II et la solution d'acide chlorhydrique.
1. Rappels sur l'acide chlorhydrique.
La solution d'acide chlorhydrique est obtenue par dissolution d'un gaz dans l'eau.
Ce gaz se nomme Chlorure d’hydrogène et il a pour formule HCl.
La solution d'acide chlorhydrique est constituée de deux ions :
- l'anion chlorure de formule Cl-.
- le cation hydrogène de formule H+.
Cette solution est incolore (couleur).
2. Expérience et observations.
Protocole : Au tube que nous avons chauffé précédemment, ajouter au ¾ du tube de l’acide chlorhydrique,
mettre un bouchon et agiter le tube.
Schéma :
Observation :
- La solution se colore en bleu.
3. Interprétation.
Information: l'acide chlorhydrique agit par l'ion H+ (l'ion Cl- est spectateur ou indifférent).
Ecrire l'équation bilan de la réaction observée.
CuO + 2 H+ Cu2+ + H2O
V. Réaction entre les ions cuivre II et une lame de zinc.
1. Expérience et observations.
Protocole : Verser le contenu du tube précédent dans un bécher et placer un clou de fer.
Schéma :
Observation :
- On observe un dépôt de cuivre sur le clou.
chauffage
Oxyde de cuivre
Acide
chlorhydrique
Clou en fer
Dépôt de
cuivre
Solution
contenant des
ions cuivre

2. Interprétation.
Information: il y a réaction entre les ions Cu2+ et Fe avec formation d'ions Fe2+.
Ecrire l'équation bilan de la réaction observée.
Cu2+ + Fe Cu + Fe2+
VI. Récapitulatif.
Parti du corps chimique Cu, nous avons retrouvé ce corps au terme de diverses réactions chimiques.
Compléter le cycle suivant, en indiquant sous quelle forme (atome, ion, corps composé ...) se trouve l'élément cuivre
après chaque réaction, et en donnant la formule du corps.
Conclusion : L’élément cuivre Cu , commun à tous ces composés, s’est conservé lors des réaction chimique.
VII. Réaction entre l’oxyde de cuivre et le carbone
Protocole : On chauffe dans un four à haute température un mélange de carbone et d’oxyde de cuivre II.
Schéma :
Observation :
- On observe un dépôt de cuivre sur les parois du
tube.
Au cours de la réaction il se forme un gaz : le dioxyde de carbone. Comment met-on en évidence la formation de ce gaz?
Avec de l’eau de chaux, il se trouble en présence de dioxyde de carbone.
Ecrire l'équation bilan de la réaction. C + CuO Cu + CO2
Ajouter une flèche dans le schéma récapitulatif § VI.
avec H+
avec OH-
avec Zn
avec HNO3
par chauffage
Cu
Cu2+
Cu(OH)
2
CuO
Cu2+
Mélange CuO + C
1
/
4
100%