Ecosystèmes tumoraux: implications thérapeutiques

1
Onco-Hemato
ON0431F
Ecosystèmes tumoraux:
implications thérapeutiques
Marc Mareel et Indira Madani
UER Radiothérapie et Recherche expérimentale sur le Cancer, UZ Gent, UG
radiothérapie et la chimiothérapie ciblaient unique-
ment ces cellules cancéreuses. Aujourd’hui, les recom-
mandations biologiques pour ces traitements reposent
toujours en grande partie sur des expériences menées
avec des cellules clonées («cloné» signie «provenant
d’une seule cellule»). Pourtant, cela fait maintenant déjà
plus de 100 ans que Stephen Paget (1855-1926),
chirurgien britannique et ls du célèbre pathologiste
James Paget, s’est posé la question «What is it that de-
cides what organ shall suffer in a case of disseminated
cancer?» (Qu’est-ce qui détermine les organes qui se-
ront touchés en cas de cancer métastatique?) et a
abouti à la réponse suivante: «The microenvironment of
each organ (the soil) inuences the survival and growth of
tumor cells (the seed)» [Le micro-environnement de
chaque organe (le sol) inuence la survie et la crois-
sance des cellules tumorales (la graine)] (1). L’impor-
tance de cette théorie de «la graine et du sol», qui
s’applique tant aux métastases qu’aux tumeurs primi-
tives, ne doit pas être sous-estimée. Elle est à la base du
concept actuel d’écosystème, qui façonne en grande
partie notre vision de la biologie moléculaire des cel-
lules cancéreuses et détermine de plus en plus nos
stratégies thérapeutiques.
Le concept d’écosystème
Les tumeurs malignes, primitives ou métastatiques, se
composent de cellules cancéreuses et de cellules hôtes
qui communiquent en permanence et forment ainsi
des écosystèmes. Les différents écosystèmes, comme
les tumeurs primitives et les métastases, communiquent
également entre eux. Ceci implique non seulement des
réseaux intracellulaires et extracellulaires complexes au
sein des tumeurs proprement dites et des organes
impliqués, comme la moelle osseuse, mais aussi une
interaction entre les différents écosystèmes [pour des
publications récentes, voir les références (2-4)]. La dor-
mance (état de sommeil) avec dissémination tardive et
la spécicité des organes touchés par les métastases
sont des phénomènes cliniques connus qui peuvent
research
Les tumeurs malignes se composent de cellules cancéreuses
et de cellules hôtes associées aux tumeurs, et forment ainsi un
écosystème. Les tumeurs métastatiques forment, quant à elles,
plusieurs écosystèmes qui communiquent en permanence.
Les cellules hôtes associées aux tumeurs, qui jouent un rôle
dans les caractéristiques malignes, comme l’invasion et le
processus métastatique, englobent les cellules endothéliales
et les péricytes, les macrophages et les leucocytes, les bro-
blastes et les myobroblastes, les adipocytes, les neurones,
ainsi que les ostéoblastes et les ostéoclastes. Une partie de
ces populations cellulaires provient de précurseurs recrutés
dans la moelle osseuse. Sur le plan moléculaire, la communi-
cation entre toutes ces cellules se caractérise par une multi-
tude de molécules et de réseaux souvent imbriqués. La tu-
meur primitive communique en permanence avec les métas-
tases, un processus dans lequel interviennent également la
moelle osseuse, le foie et les organes endocriniens. Un nou-
veau concept est celui de niche métastatique: des ligands
provenant de la tumeur primitive et des cellules hôtes issues
de la moelle osseuse préparent les sites métastatiques à l’ar-
rivée des cellules cancéreuses. La circulation, dans laquelle on
retrouve des cellules cancéreuses potentiellement métasta-
tiques, des précurseurs de cellules hôtes associées aux tu-
meurs, des ligands et des récepteurs solubles impliqués dans
le processus métastatique, joue un rôle essentiel dans cette
communication. Les cellules hôtes sont la cible de médica-
ments tels que les bisphosphonates, les inhibiteurs de l’angio-
genèse, les anti-inammatoires et les immunomodulateurs.
Les cellules hôtes associées aux tumeurs et leur matrice ex-
tracellulaire ont une inuence sur l’effet des médicaments
utilisés en chimiothérapie. Le concept d’écosystème implique
que le traitement d’un certain élément, par exemple la tu-
meur primitive, peut avoir une inuence négative sur l’en-
semble du système: des effets secondaires pro-invasifs et
pro-métastatiques ont été décrits pour la radiothérapie, la
chimiothérapie et la chirurgie. Les auteurs plaident pour le
développement d’un traitement du cancer ciblant les écosys-
tèmes tumoraux.
Introduction
Les tumeurs malignes ont longtemps été considérées comme des ac-
cumulations de cellules cancéreuses, à savoir des cellules au génome
modié issues d’une ou de plusieurs cellules initiatrices de tumeurs.
Dès lors, jusqu’il y a quelques décennies, des traitements comme la
Peer-reviewed article

2
Onco-Hemato
faire apparaître le rôle déterminant joué par l’hôte. La ten-
dance de certaines tumeurs à envahir l’un ou l’autre organe
spécique à distance n’est pas seulement déterminée par la
circulation sanguine, qui, par exemple, transporte les cellules du
cancer du côlon vers le foie par le biais de la veine porte. Une
analyse de plusieurs modèles de métastases suggère que divers
types de tumeurs trouvent le terrain le plus fertile pour leurs
métastases dans des organes différents, tels que les poumons
pour le sarcome, le foie pour le mélanome, la moelle osseuse
pour le cancer de la prostate et le cerveau pour les cancers du
poumon et du sein. Des métastases peuvent apparaître plus de
10 ans après l’exérèse de la tumeur primitive, un phénomène
qui s’explique par la dormance tumorale. Certaines tumeurs,
telles que le cancer du sein et le mélanome oculaire, ont mau-
vaise réputation à cet égard, si bien que pour ces types de
cancer, le terme «guérison» doit être employé avec toute la
circonspection nécessaire. Il ne fait guère de doute que les cel-
lules cancéreuses à l’origine des métastases proviennent de la
tumeur primitive, d’où elles s’échappent probablement avant
que l’invasion ne devienne évidente, comme dans le cas de
carcinome au stade in situ. Mais où se cachent-elles pendant
tout ce temps? Des métastases hépatiques tardives peuvent se
former à partir de cellules cancéreuses qui se sont implantées
dans l’écosystème du foie depuis la tumeur primitive, ou à par-
tir de cellules qui dormaient dans la moelle osseuse et qui se
sont ensuite dirigées vers le foie pour s’y réveiller, se dévelop-
per et évoluer en métastases cliniquement patentes. Comment
l’organisme contrôle-t-il ces micrométastases? Pourquoi se ré-
veillent-elles? Autant de questions auxquelles des analyses bio-
cellulaires et biomoléculaires approfondies d’écosystèmes tu-
moraux apporteront peut-être une réponse.
Cellules tumorales:
cellules cancéreuses et cellules hôtes
associées aux tumeurs
L’analyse histopathologique des cancers montre clairement la
présence massive de cellules hôtes, qui se mélangent avec les
cellules cancéreuses (Figure 1). Ces cellules hôtes accom-
pagnent les cellules cancéreuses sur le lieu de la tumeur avant
le début de l’invasion et du processus métastatique. Il est frap-
pant de constater à quel point le rapport de l’anatomopatho-
logiste accorde généralement peu d’attention à ces cellules
hôtes. Pourtant, des observations expérimentales et cliniques
montrent bien qu’elles sont impliquées dans la croissance, l’in-
vasion et la dissémination métastatique, des caractéristiques
qui déterminent la malignité des tumeurs. Lorsque les cellules
cancéreuses du cancer du rectum illustré dans la gure 1,
sont isolées et disséminées in vitro sur une matrice extracellu-
laire, il est impossible de mettre en évidence leur caractère in-
vasif. Toutefois, l’ajout de myobroblastes issus de la même tu-
meur déclenche une invasion manifeste (5). En répétant cette
expérience avec des macrophages à la place de myobro-
blastes, les chercheurs ont démontré que cette activité pro-
invasive ne se limitait pas aux myobroblastes.
Les cellules hôtes associées aux tumeurs sont variées (Figure
2) et se rencontrent dans la plupart des tumeurs épithéliales,
ainsi que dans des hémopathies malignes. Les cellules endothé-
liales forment de nouveaux vaisseaux sanguins et lymphatiques
(angiogenèse); elles favorisent le métabolisme de la tumeur,
sont indispensables à sa croissance, transportent les cellules
hôtes circulantes et permettent aux cellules métastatiques
d’accéder à la circulation. L’angiogenèse est régulée par des
équilibres entre promoteurs tels que le VEGF (Vascular Endo-
thelial Growth Factor) et suppresseurs comme l’angiostatine (6).
Dans la majorité des tumeurs, l’angiogenèse est associée à un
pronostic moins favorable. L’angiogenèse ne se limite pas aux
cellules endothéliales. Les péricytes, qui stabilisent les vaisseaux
sanguins, y participent également. Dans le cadre du cancer du
sein, un faible nombre de péricytes (associés aux vaisseaux san-
guins) est associé à une survie réduite. Dans un modèle murin,
Cooke et al. (7) ont constaté qu’une réduction des péricytes
Figure 1: Coupe histologique d’un adénocarci-
nome du rectum, colorée avec un anticorps
dirigé contre l’aSMA (a-Smooth Muscle Actin –
alpha-actine musculaire lisse), un marqueur des
myobroblastes (marron). La èche indique les
cellules cancéreuses, et la pointe de la èche les
lymphocytes (petit noyau sombre).
Figure mise à disposition par le Dr Laurine Verset, Service
d’Anatomie pathologique, Hôpital Erasme, ULB, Bruxelles.

3
Onco-Hemato
conduit à davantage de métastases. Ces auteurs concluent que,
dans l’écosystème de la tumeur primitive, les péricytes jouent
le rôle de «gatekeepers» (gardiens) contre la dissémination
métastatique.
Les macrophages et les leucocytes sont des expressions d’une
inammation et d’une immunité. Ils représentent la partie la plus
importante et la mieux différenciée des cellules hôtes. Le mys-
tère du «Dr Jekyll et Mr Hyde» s’applique bien à la diversité des
leucocytes [Tumor Inltrating Leukocytes (TIL)] et des macro-
phages [Tumor Associated Macrophages (TAM)], les uns dévelop-
pant une activité protumorale et les autres une activité anti-
tumorale au sein de la même tumeur. Les effets opposés sur
l’invasion et la dissémination métastatique découlent de la
différenciation des monocytes en macrophages suppresseurs
M1 ou promoteurs M2 (8). La plupart des TAM sont considérés
comme des macrophages favorisant l’invasion, dans la mesure où
ils produisent des enzymes lytiques qui dégradent la matrice
extracellulaire et ouvrent ainsi la voie aux cellules cancéreuses
invasives (9). Les TAM interagissent également avec d’autres cellules
hôtes; ils sécrètent notamment le VEGF et stimulent ainsi l’angio-
genèse. Le contexte immunologique, tel que visualisé sur la base
des TIL, des TAM et de leurs précurseurs, constitue un facteur
pronostique majeur qui varie d’un type de tumeur à l’autre (10).
Les broblastes et les myobroblastes sont des éléments es-
sentiels de la desmoplasie observée (de manière réversible)
dans le processus de cicatrisation des plaies et (de manière ir-
réversible) en cas de chéloïdes, de brose hépatique, pulmo-
naire et rénale, et de tumeurs épithéliales. Dans les tumeurs,
ces cellules sont également appelées Cancer-Associated Fibro-
blasts (CAF) (11). Cette population cellulaire se compose pro-
bablement de différents sous-types, comme ceux qui ont été
décrits pour les macrophages. Les cancers du sein avec un pro-
nostic plus défavorable se reconnaissent à leur signature géné-
tique broblastique. Nous avons écrit plus haut que les myo-
broblastes ont attiré notre attention sur le potentiel pro-invasif
des cellules hôtes associées aux tumeurs (5). L’activation des
broblastes constitue également un élément important dans la
formation de la niche pré-métastatique que nous décrirons
ENDOCRINE
GLANDS
LIVER BONE
MARROW
PRIMARY
TUMOR
LYMPH NODE
ORGANS
AT
DISTANCE
Glucocorticoids
Oestrogen
Progesteron
Testosteron
Insulin-like growth factor
Parathyroid
hormone
Vascular endothelial growth factors
Tumor necrosis factor
Lysyl oxidase
Glucocorticoids
Tumor antigens
MCC
MCC
MCC
MCC
LC
MSC
HPC
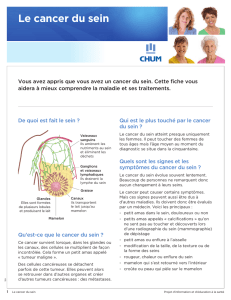
HPC: cellules précurseurs hématopoïétiques; LC: leucocytes; MSC: cellules souches mésenchymateuses;
MCC: cellules cancéreuses métastatiques. La gure ne se veut pas exhaustive. Modiée d’après
M. Mareel et S. Constantino (3).
Figure 2: Représentation schématique des écosystèmes communicants dans une tumeur métastatique.
Les «Organs at distance» (organes à distance) sont les sites des métastases et englobent également la
moelle osseuse (métastases osseuses), le foie et les organes endocriniens, qui sont également présentés
de manière individuelle comme sources d’hormones et facteurs de croissance.

4
Onco-Hemato
plus loin (12). Dans le cancer du sein, l’effet pro-invasif des CAF
est combattu par les cellules myoépithéliales; en cas d’évolution
du carcinome in situ en carcinome invasif, la couche basale or-
ganisée de cellules myoépithéliales disparaît.
Il existe des liens entre l’obésité et le cancer. Il n’est donc pas
étonnant que les cellules graisseuses (adipocytes) gurent sur la
liste des cellules hôtes associées aux tumeurs. Les cellules cancé-
reuses stimulent la production, par les cellules graisseuses, de
protéases qui contribuent à la survie des cellules cancéreuses
invasives dans le tissu adipeux péritumoral. Dans la moelle os-
seuse, les cellules graisseuses favorisent le développement de
plasmocytomes; elles inhibent l’apoptose et stimulent la crois-
sance, ainsi que l’adhérence et la migration cellulaires (13).
L’invasion des neurones et de leur périphérie (invasion intra-
neurale et périneurale) entraîne une dispersion locale dans
différents types de tumeurs tels que les cancers de la prostate,
du sein et du pancréas. La tumeur envoie aux neurones des
signaux afférents qui non seulement causent des douleurs, mais
de plus entraînent une néo-neurogenèse. Les neurones asso-
ciés à la tumeur produisent également des signaux efférents,
tels que l’endothéline, l’histamine et des prostaglandines, qui
stimulent l’inammation, l’angiogenèse et l’invasion (14).
Les ostéoblastes et les ostéoclastes sont des éléments impor-
tants dans l’écosystème de la moelle osseuse et de la métastase
osseuse. Il s’agit des cellules hôtes associées aux métastases les
plus étudiées et qui constituent des cibles majeures pour le trai-
tement (15). La niche ostéoblastique constitue un endroit idéal
pour la nidication des cellules cancéreuses métastatiques.
Le biotope des cellules cancéreuses et de toutes ces cellules
hôtes associées aux tumeurs est la matrice extracellulaire
(MEC). Cette dernière est un assemblage de macromolécules
riches en sucres qui servent à la fois de substrat pour l’adhé-
rence et la migration, et de ligand xé pour la signalisation. La
MEC est également un réservoir de ligands solubles (par
exemple, les facteurs de croissance et les cytokines), qui sont
mobilisés par des protéases (16).
L’origine des cellules hôtes associées
aux tumeurs: le rôle de la moelle
osseuse
On estime qu’un quart des cellules hôtes associées aux tu-
meurs sont recrutées en tant que précurseurs [cellules souches
mésenchymateuses (CSM) et précurseurs hématopoïétiques
(CPH)] au niveau de la moelle osseuse.
Des précurseurs CD34+ se développent dans la moelle os-
seuse, sont affectés (prédestinés) et acheminés vers la circula-
tion, se transforment en monocytes, sont recrutés dans la tu-
meur et se différencient en macrophages (TAM). La moelle
osseuse forme donc un écosystème crucial, non seulement en
tant que site métastatique, mais aussi en tant que source de
cellules hôtes associées aux tumeurs et aux métastases (17).
Communication intratumorale:
aspects moléculaires
Multiplicité et redondance sont deux aspects caractérisant la
communication intercellulaire et intracellulaire. En effet, des
centaines de réseaux et un nombre toujours croissant de mo-
lécules sont impliqués dans ce processus. Ainsi, le nombre de
ligands impliqués dans la communication entre les cellules can-
céreuses et les myobroblastes est passé de trois (18) à
quelques dizaines (2, 5), une tendance qui s’applique également
à d’autres cellules hôtes (19). Aux personnes s’intéressant aux
mécanismes de base qui régissent ce type de réseaux com-
plexes, nous recommandons le livre d’Uri Alon (20).
La communication intracellulaire détermine la réaction de la
cellule aux stimuli externes. Les cellules cancéreuses et les cel-
lules hôtes, de même que les cellules hôtes entre elles,
échangent des signaux par l’intermédiaire de molécules sécré-
tées appelées ligands. La communication au sein de la cellule
s’effectue souvent comme suit: le signal extracellulaire (ligand)
qui, par exemple, stimule l’invasion, se lie à un récepteur spéci-
que situé sur la face externe de la membrane plasmique. Ce
récepteur traverse la membrane plasmique; sa partie intracel-
lulaire comporte un domaine kinase (une kinase est une en-
zyme qui catalyse la phosphorylation) qui induit l’autophos-
phorylation du récepteur. Cette activation marque le début
d’une cascade de kinases qui, au nal, va activer un facteur de
transcription de l’ADN. Ce dernier se lie à un promoteur spé-
cique, qui active le gène codant une protéine qui module des
activités cellulaires impliquées dans l’invasion, telles que la mi-
gration, la prolifération, l’adhérence cellule/cellule et cellule/
matrice et la protéolyse. La dynamique de tels réseaux repose
sur des équilibres entre phosphorylation (kinase) et déphos-
phorylation (phosphatase).
La communication intercellulaire repose, quant à elle, sur l’inter-
action de ligands avec des récepteurs spéciques. Nous citons
ici quelques exemples de scénarios de communication inter-
cellulaire dans les écosystèmes tumoraux. Notez que ces
réseaux ne représentent qu’une partie de systèmes bien plus
complexes, dans lesquels sont impliqués plusieurs molécules
et types de cellules.

5
Onco-Hemato
En cas d’hypoxie, la concentration d’HIF-1a (Hypoxia-Inducible
Factor) dans le cytoplasme de la cellule cancéreuse augmente.
On assiste également à ce phénomène en cas de perte de la
protéine VHL (Von Hippel-Lindau), par exemple en raison
d’une mutation génétique dans le cancer du rein; VHL induit la
dégradation du facteur HIF-1a. Des concentrations accrues
d’HIF-1a entraînent la production et la sécrétion de VEGF, qui
se lie au VEGFR (récepteur du VEGF) sur les cellules endothé-
liales avec, comme conséquence, l’activation du récepteur par
phosphorylation, la transduction des signaux et la stimulation
de la survie, de la migration et de la prolifération (6).
L’extravasation des cellules cancéreuses est assistée par les
macrophages. La cytokine IL-1 (interleukine-1) stimule l’ex-
pression, par les cellules endothéliales, de la VCAM-1 (Vascular
Cell Adhesion Molecule-1) et de la sélectine E. Ces molécules
d’adhérence cellule/cellule hétérotypiques captent les cellules
cancéreuses métastatiques circulantes et leur offrent la possibi-
lité de quitter la circulation et d’aller se nicher dans un nouvel
écosystème potentiellement fertile. Les macrophages pro-
duisent l’EGF (Epidermal Growth Factor), qui, après s’être lié à
l’EGFR (récepteur de l’EGF) sur les cellules cancéreuses, agit
comme facteur de motilité. Les cellules cancéreuses produisent
le CSF-1 (Colony Stimulating Factor-1), qui stimule l’expression
de l’EGF par les macrophages. D’autre part, l’EGF stimule l’ex-
pression du CSF-1 par les cellules cancéreuses (21). Initiale-
ment, cette boucle de rétroaction positive a été découverte
par le biais de l’analyse de l’EGF et du CSF-1. A l’heure actuelle,
elle implique une vingtaine de ligands.
Les cellules cancéreuses produisent le TGF-β (Transforming
Growth Factor-β), qui favorise la transformation des broblastes
en myobroblastes. Ces derniers produisent le SF/HGF (Scatter
Factor/Hepatocyte Growth Factor) et la tenascine C, qui se lient
à des récepteurs sur les cellules cancéreuses et, conformément
aux réseaux intracellulaires décrits plus haut, stimulent des acti-
vités cellulaires associées à l’invasion (5).
Les cellules graisseuses produisent un certain nombre de cyto-
kines appelées adipokines. L’une d’elles, la leptine, stimule la
sécrétion, par les macrophages, de cytokines pro-inamma-
toires telles que l’IL-1 et le TNF-a (Tumor Necrosis Factor-a);
cette activité est combattue par une autre adipokine appelée
adiponectine. (22)
Communication entre écosystèmes:
tumeur primitive, niche métasta-
tique, moelle osseuse et circulation
(Figure 2)
La tumeur primitive est la source des cellules métastatiques.
Elle contient des cellules cancéreuses ainsi que des cellules
hôtes. Sa survie est assurée par des cellules souches cancé-
reuses. Les ganglions lymphatiques constituent un site métasta-
tique fréquent en cas de tumeur épithéliale. Ils contiennent
d’importantes cellules hôtes associées aux tumeurs, à savoir
des macrophages, ainsi que des lymphocytes B et T. Le premier
contact de la tumeur primitive avec le système immunitaire de
l’hôte a lieu dans les ganglions lymphatiques sentinelles. Des
antigènes tumoraux solubles atteignent les ganglions lympha-
tiques avant que les cellules cancéreuses métastatiques n’y par-
viennent. La nidication des cellules cancéreuses dans les gan-
glions lymphatiques implique des récepteurs (par exemple,
CXCR4) sur la cellule cancéreuse et leurs ligands (comme la
chimiokine CXLCL12) dans les ganglions lymphatiques.
Comme Paget (1) l’a décrit, les tumeurs ont tendance à métas-
taser vers des organes bien spéciques. Pour certains de ces
sites de prédilection, une explication d’ordre moléculaire a été
trouvée. Ainsi, les cellules du cancer de la prostate se nichent
dans la moelle osseuse, là où se trouvent normalement les
cellules souches hématopoiétiques (22). De manière similaire,
des cellules du cancer du sein exprimant divers récepteurs de
chimiokines (appelés CXCR ou CCR selon leur motif d’acides
aminés) se logent dans le foie (CXCR4), le cerveau (CXCR1),
la plèvre (CCR6) ou la peau (CCR7). La niche pré-métasta-
tique est un nouveau concept important. Celui-ci veut qu’avant
l’arrivée des cellules cancéreuses sur le site de la métastase, le
terrain est fertilisé par des cellules recrutées dans la moelle
osseuse, en réponse à des signaux (tels que le VEGF-A et le
TNF-a) envoyés par la tumeur primitive (19, 20). Par la suite,
les cellules cancéreuses forment les cellules stromales pour
qu’elles entretiennent les cellules souches cancéreuses qui sont
nécessaires au développement de métastases (25).
La moelle osseuse joue un rôle majeur dans la communication
entre les écosystèmes tumoraux. Elle produit des précurseurs
pour les cellules hôtes observées dans la tumeur primitives et
les métastases, est elle-même un lieu où se développent sou-
vent des métastases et constitue un lieu d’habitat pour les
CTD (cellules tumorales disséminées), lesquelles sont prédic-
tives d’une maladie métastatique au niveau des os ou d’autres
localisations.
Il est évident que la circulation assure la communication entre
les divers écosystèmes. Nous la considérons comme un éco-
système à part entière comprenant des éléments de cancers
métastatiques, à savoir: des cellules cancéreuses métastatiques
et non métastatiques, des précurseurs de cellules hôtes asso-
ciées aux tumeurs (y compris des cellules de niche prémétas-
 6
6
 7
7
1
/
7
100%