1
Objectifs :
❖ Préparer une solution de chlorure de sodium titrée (c.à.d. : de concentration connue) ;
❖ Préparer une solution moins concentrée à partir d’une solution mère plus concentrée.
I. Définitions :
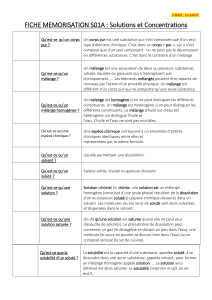
1- La solution :
➢ Par dissolution d’un …………………………. (qui peut être solide, liquide ou gaz) dans un ……………………………
on obtient un mélange homogène appelé ………………………………
➢ Si le solvant est l’eau la solution est dite ………………………………..
Exemples :
Solution aqueuse de chlorure de sodium : le solvant est ………… ; le soluté est :………………………..…………
Solution aqueuse de sulfate de cuivre : le solvant est …………… ; le soluté est :………………………..…..………
➢ On peut préparer une solution en mélangeant deux liquides ………………………………… ; le liquide qui a le
volume le plus petit est le ………………………… et celui qui a le plus grand volume est le …………………………
Exemples :
Solution aqueuse d’alcool : le solvant est ………… ; le soluté est :………………………..…………
Solution aqueuse de vinaigre : le solvant est …………… ; le soluté est :………………………..…..………
2-
La concentration massique notée d’un soluté
dans une solution est égale au rapport de la
masse du soluté dissous au volume de la
solution.
; en )
en gramme en litre (L) ;
;
La concentration molaire d’un soluté dans une
solution est égale au rapport de la quantité du
soluté dissous au volume de la solution.
; en )
en mole en litre (L) ;
;
Relation entre et : ) ou bien,
(en )
II. Matériels : balance électronique ; spatule ; fiole jaugée de ; bécher ; entonnoir ; chlorure de
sodium ; pissette d’eau distillée ; pipette jaugée de ; propipette.
III. Manipulation :
1) Préparation d’une solution titrée :
On désire préparer un volume ………………. d’une solution de chlorure de sodium
de concentration ;
a. Calculer la masse de chlorure de sodium à peser ; on donne ;
…………………………………………………………………………………………………………………………………………………………………..
…………………………………………………………………………………………………………………………………………………………………..

2
b. Pour obtenir la solution , suivre avec délicatesse les étapes suivantes :
2) Préparation d’une solution moins concentrée à partir de la solution ou préparation de
par dilution de
On désire, maintenant, préparer un volume ………………. d’une solution de chlorure
de sodium appelée solution fille, de concentration à partir de la solution
précédente, appelée solution mère, de concentration .
a. Quel volume doit-on prélever de
…………………………………………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………………………………………….
c. Pour obtenir la solution de chlorure de sodium , suivre avec délicatesse les étapes
suivantes :
Remarque :
du
de
100mL
100mL
100mL

3
On prélève le volume à l’aide d’une …………………………………………………………
On prépare une solution titrée dans une …………………………………… jaugée.
Application :
Exercice n°1 : Le résultat d’une analyse de sang d’un patient porte les indications suivantes :
Cholestérol :
Valeurs limites :
1) Calculer la masse molaire du cholestérol de formule brute
………………………………………………………………………………………………………………………………………………………………………
……………………………………………………………………………………………………………………………………………………………………..
2) Calculer la concentration molaire du cholestérol dans le sang du patient.
……………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………..
3) Ce patient a-t-il un taux de cholestérol correct ? Justifier.
……………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………..
On donne ;
1
/
3
100%