Chimie
Le diiode I2 réagit avec le métal zinc (s) (en éxcés). La transformation qui se produit est modélisé par l’équation chimique
I2(aq) + Zn(s) Zn2+(aq) + 2 I–(aq) (1)
On plonge une lame de zinc en excés dans un volume V0=20mL de la solution de diiode à la concentration molaire en soluté
apporté C0=2,00.10-2mol/L.
A l’intervalles de temps réguliers, on prélève V=1,00mL de milieu réactionnel, que l’on dose par solution de thiosulfate de
sodium ( 2 Na+(aq) + S2 O32(aq) - )à la concentration C1=1,00.10-3mol.L-1
1-Ecrire les demi-équations électroniques de la réaction (1) .On donnera en justifiant le nom de chacune de ces réaction (0.5)
2-Dresser le tableau d’avancement et calculer la quantité de matière initial n0 de diode (0.5)
3- calculer l’avancement maximal (0.25)
Le volume necessaire à l’obtention de l’ equivalence est noté VE.
4-4-1 Ecrire l’équation de titrage .On donne les couples mis en jeu I2(aq) /I-(aq) et S4O62-(aq)/S2O32-(aq) (0.5)
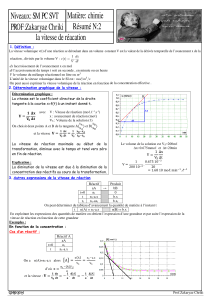
4-3- Les résultas des diffèrent dosages permettent de tracer la courbe de la figure 1.
Donner l’expression de l’avancement x de la reaction (1) dans le mélange en fonction de n0 (I2) , C1 et VE (0.75)
4-4- Trouver la valeur de la quantité de matiére n(I2) presente dans le prélevement à t=900s (0.5)
4-5- donner la définition du temps de demi-réaction et montrer
que sa valeur égale environ à 180 secondes (1)
4-6- trouver l’expression de la vitesse volumique
en fonction de vE (1)
4-7-calculer sa valeur à t=200s ( 0.25)
4-8- comment évolue la vitesse volumique au cours
Du temps ? Quel est le facteur cinétique responsable?( 0.5)
5-on reprend l’expérience en travaillant à la même
Température mais en utilisant une solution de diode
de Concentration C0’=4.10-2mol/L et avec
V0=20mL
Justifier qualitativement si les grandeurs sont modifies
ou non par rapport à l’expérience initiale
-l’avancement maximal
- le temps de demi-réaction (0.75)
- La vitesse volumique initiale de la réaction
6- On considère maintenant l’expérience initiale réalisée dans un bain- marie à une température supérieure à la température de l’expérience
Recopier la courbe et représenter l’allure de la courbe obtenue ( 0.5
t(s)
VE(mL)
Figure 1
40
5
0
500

1
/
2
100%