See discussions, stats, and author profiles for this publication at: https://www.researchgate.net/publication/320237535
Biophysique
Book · October 2017
CITATIONS
0
READS
8,017
1 author:
Some of the authors of this publication are also working on these related projects:
Socioeconomic and Age-incidence of Breast Cancer: Modeling Using Artificial Intelligence Technique View project
radiofrequencies effects on rats View project
Bouharati Saddek
Ferhat Abbas University of Setif
140 PUBLICATIONS198 CITATIONS
SEE PROFILE
All content following this page was uploaded by Bouharati Saddek on 05 October 2017.
The user has requested enhancement of the downloaded file.

Université Ferhat Abbas, Sétif 1
14
BIOPHYSIQUE
Par :
Saddek Bouharati
Faculté des Sciences de la Nature et de la Vie
Département des Etudes de Base

2
Sommaire
Alphabet Grecque…………………………………………………………………………..
Constantes Universelles………………………………………………………………...
Les unités de mesure du système métrique…………………………………………...
Principales unités de mesure anglo-saxonnes……………………………………
Définitions générales…………………………………………………………………….
Les états physico-chimiques des constituants de la matière…………………….....
Discontinuité de la matière.…………………………………………………….
Les forces intermoléculaires………..……………………………………
Agitation moléculaire………………………………………….…………..
Chapitre 1. Solution électrolytique – Phénomène électrocinétique
Conductivité électrolytique………………………………….…………………
Potentiel métal-solution……………………………………….…………………….
Chapitre 2. Phénomène de Diffusion
Diffusion (lois de Fick)……………………………………….……………….………………
Diffusion du point de vue de la théorie cinétique…….…………………….……………….
Analyse d’Overbeek…………………………………………………….…………………….
Osmose et Pression Osmotique….………………………………………….……………….
Mesure de la pression osmotique (osmomètre de Dutrochet)……………………………
Loi quantitative de Pfeffer………………………………………………….…………………
Loi de Vant’Hoff………….…………………………………………………….………………
Loi de Raoult…….……...…………………………………………………….………………
Osmomètrie et Cryoscopie..………………………………………………….………………
Travail osmotique………..…………………………………………………….………………
Interfaces biologiques
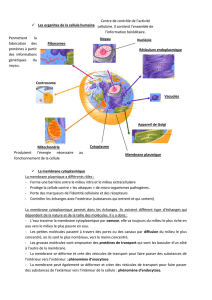
Structure de la membrane biologique………..…………………………..….………………
Rôle des membranes biologiques………..………………………………….……………
Perméabilité des membranes biologiques à l’eau………..………………..………………
Perméabilité des membranes biologiques aux molécules chargées…....………………
Chapitre 3. Phénomènes de surface
Interface liquide-Gaz…………………………..………………………..….…………………
Pression capillaire et relation de Laplace……………………………………………………
Interface liquide-liquide ……...………………..…………………………..….………………
Tension superficielle des solutions…………..…………………………..….………………
Les films mono moléculaires…………………..………..………………..….………………
Propriétés superficielles des protéines et des phospholipides……………………………
Applications biologiques……………………………………………………………………
4
4
5
7
8
10
10
10
12
13
16
17
18
19
20
20
20
21
21
23
23
24
25
25
28
31
32
33
33
34
35
35

3
Chapitre 4. Interface solide-liquide
Contact d’un solide à un liquide.……………..…………………………..….…………….……...36.
Angle de raccordement d’un liquide à un solide………………………………………….……..36
Agents mouillants…………………….………..……………………..….………………….………37
Flottation………………………………………..…………………………..….…………………….37
Relation de Young……………………………..…………………………..….……………………38
Adsorption………..…………………………..….……………………………………………….….38
Phénomènes capillaires et loin de Jurin……..…………………………..….……………………38
Théorie de la double couche électrochimique………………………….………………….….…40
Chapitre 5. Hydrodynamique
Viscosité
Ecoulement laminaire…………..………………………..….…………………….........................42
Ecoulement turbulent…………..…………………………..….……………………….….……..…54
Ecoulement du sang le système cardio-vasculaire………………………………….….…….…46
Force de résistance visqueuse et mesures de la viscosité…………………………..…….…..46
Viscosité des solutions macromoléculaires……………………………………………………….47
Sédimentation…………………………………………………………………………..….………48
Chapitre 6. Biophysique des radiations
Classification des rayonnements……………………………………………………………….….50
Les rayons X…………………………………………………………………………………………51
La radioactivité……………………………………………………………………………….………52
Effet biologique des radiations…………………………………………………………………..…53
Radiodiagnostic ………………………………………………………………………………….…54

4
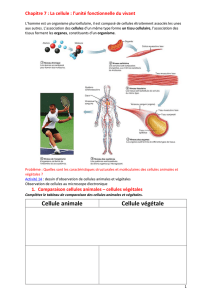
Introduction
Dans cette modeste contribution, nous avons essayé de présenter et d’une façon
très brève l’essentiel du contenu des cours et travaux dirigés du module de biophysique
destiné aux étudiants de la deuxième année des sciences de la nature et de la vie. Nous
l’avons présenté dans l’ordre tel qu’il est fixé officiellement. Cependant, quelques
réaménagements ont été apportés et qui sont jugés nécessaires par l’auteur notamment
l’ordre des sujets. Un maximum d’attention lui a été consacré dans le but de porter aide aux
étudiants de la dite filière.
Nous nous excusons pour toutes erreurs d’inattention ou de frappe qui auraient été introduite
involontairement.
Dr. Bouharati Saddek
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
1
/
56
100%