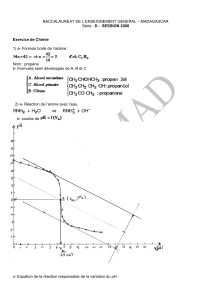
Corrigé – type de l’épreuve de sciences - physiques bac II 2021 série C
Exercice1
1.a) Nom systématique : propane-1,2,3-triol.
b) * Equation bilan
+ 3
3 +
* Les caractéristiques : Lente, limitée athermique.
2. * Equation bilan
+ 3()
+ 3( )
* Nom usuel : saponification
* Caractéristiques : Lente et totale
* Rôle de l’éthanol : solvant
3.a) Intérêt : bloquer la réaction de saponification
b) Démonstration
=
Or
=
-
=
(
c) *Tableau : =
(60-X)
t(min)
0
4
9
15
24
37
53
83
X(m)
0
52,9
46,3
40,4
33,5
27,5
22,2
16,3
0
2,37
4,57
6,53
8,83
10,83
12,6
14,57
* Courbe
d) Vitesse de formation : =
= coefficient
directeur de la tangente à la courbe.
* à = 9 min, = 3,74. mol/min
* à = 37min, = 1,28. mol/min
e) Justification
Les vitesses diminuent. Ceci se justifie par la
diminution de la concentration des réactifs.
Exercice 2
1. Protocole :
= =
= 5m
Prélever 5 m de à l’aide d’une pipette graduée et
l’introduire dans une fiole jaugée de 100m. Puis
compléter de l’eau distillée jusqu’au trait de jauge et
homogénéiser en agitant.
2.a) Equation bilan
+ +
b) * Expression de
= - = -
* Rapport :
=
=
.
) Démonstration
=
=
=
d) Tableau : = (mo/)
(m)
4
6
8
11
16
pH
3,6
3,8
4
4,3
4,8
1/()
0,25
0,17
0,125
0,091
0,0625
(mo/)
25,1
15,8
10
5,01
1,58
e) *Equation numérique
= a (
+ b avec a=
=1,26.
= 0,63.- (1,26. 0,1) = - 6,3.
= 1,26. (
- 6,3.
* Déduction du pKa
=
= 6,3.
pKa = -log Ka = 4,2
Volume : =
= 20 m
) Formule et nom de l’acide carboxylique.
= or =
d’où
= 122g/mol
M = 13 + 44
= 6
: Acide benzoïque
. a) Démonstration
׀
׀
׀
׀
׀
׀
׀
׀
׀
׀
׀
׀
׀
׀
׀
׀

= 10g/ 3g/ d’où est nécessairement
saturée.
) Calcul de
c) Calculer de
Exercice 3
1. Accélération de la fusée au décollage
TCI :
Sur (Oz) ma = F- P
a = 8,95 m/s².
2. * Expression de V en fonction de K, r et M
TCI :
Sur
:
d’où
* Expression de T en fonction de K, r et M
* Déduction
3. Déduction de la masse M
avec
(coef dir) ①
D’après la courbe
S.I
①
M = 5,92.1024 kg
4. a) Expression de Ep, Ec et Et
;
b1) Expression de Ve
b2) Expressions de , et
En P : r = R
;
5. a) Demonstration
sont constants donc varie avec
b) est minimale lorsque
donc les
bases de lancement se situent à l’équateur.
6. Calcul de V1
1ère méthode
avec
,
;
r = R + h ;
= 7,9 km/s
Exercice 4
1. Identification : L1 est biconvexe car
2. Position, nature et grandissement
* Position :
* Nature :
est une image réelle
* Grandissement :
= -2
3. a) Démonstration
Objet à l’infini
car l’image
A’B’ est virtuelle or
Or
et
< 0 alors
or
d’où
4. a) * Position de par rapport à L1.
* Déduction de la position de A’B’ par rapport à L2.
étant à l’infini, A’B’ se trouve dans le plan focal
image de L2 A’B’ se trouve à
avant L2
b) Distance O1O2 : O1O2 = d - O1A + O2A’ = 25 cm
c) Détermination des positions de F et F’
* Foyer image F’
:
= -0,025 m,
avec
F’ est virtuel
* Foyer objet F
:
- 0,6 m
avec
0,05 m F est réel
1
/
2
100%