Xanthomes
H. Adamski, D. Bligny, J. Chevrant-Breton
Les xanthomes sont des tumeurs bénignes brun jaunâtre dysmétaboliques liées essentiellement à
l’infiltration cutanée par des histiocytes macrophages spumeux, remplis de gouttelettes lipidiques
composées surtout de cholestérol estérifié et parfois triglycérides. D’aspect clinique très varié allant du
xanthélasma à des xanthomes tubéreux, tendineux localisés, à des formes en nappe, en stries,
notamment des plis, leur diagnostic est histologique. Deux types de xanthomatose primitive sont
individualisés après avoir éliminé des xanthomisations épiphénomènes secondaires à des processus
variés tels que les dermatoses inflammatoires, lymphomes, histiocytoses, tumeurs, etc. : les
xanthomatoses dyslipidémiques, témoin d’une hyperlipoprotéinémie primitive familiale ou secondaire, ou
beaucoup plus rarement d’une autre dyslipidémie (xanthomatose cérébrotendineuse, sitostérolémie,
maladie de Tangier) ; les xanthomatoses normolipidémiques très rares, qui nécessitent la recherche de
localisations extracutanées, de pathologies associées : dysglobulinémies, myélome et syndromes
hématologiques, notamment lymphoprolifératifs, vascularites, hypocomplémentémiques notamment au
cours du xanthogranulome nécrobiotique, de la xanthomatose plane diffuse, plus rarement du
xanthogranulome juvénile et de la xanthomatose disséminée de Montgomery. Le traitement de ces
xanthomes est d’abord étiologique dans les formes dyslipidémiques, mais souvent aussi symptomatique
médicochirurgical, dans les formes normolipidémiques.
© 2009 Elsevier Masson SAS. Tous droits réservés.
Mots clés : Xanthome ; Xanthomatose disséminée de Montgomery ; Xanthomes plans diffus ;
Xanthogranulome nécrobiotique ; Xanthogranulome juvénile ; Xanthome papuleux ;
Xanthome verruciforme ; Dyslipidémies
Plan
¶Introduction 1
¶Aspects cliniques 1
Xanthélasma ou xanthomes palpébraux 1
Xanthochromie striée palmaire 2
Xanthomes plans diffus 2
Xanthomes éruptifs 2
Xanthomes tubéreux 2
Xanthomes tendineux 2
¶Aspect anatomopathologique 2
¶Rappel du métabolisme des lipoprotéines 3
¶Diagnostic d’une dyslipoprotéinémie 3
Dosage du cholestérol total 3
Dosage du HDL-C et calcul du LDL-C 3
Dosage des triglycérides 3
Dosage des apolipoprotéines 4
¶Étiologies 4
Xanthomatoses dyslipoprotéinémiques 4
Xanthomes normolipidémiques 6
¶Traitement 9
Traitement local des xanthomes 9
Prise en charge d’une dyslipidémie 9
■Introduction
[1, 2]
Les xanthomes sont des néoformations cutanées jaunâtres
constituées essentiellement de cellules macrophagiques riches
en granulations lipidiques faites de cholestérol et de
triglycérides.
Cette définition permet d’éliminer :
• les surcharges lipidiques exogènes (paraffinome, etc.) ;
• les lipomes constitués d’adipocytes ;
• les lipidoses extracutanées dans le cadre des maladies lysoso-
miales (maladie de Gaucher, maladie de Niemann-Pick,
maladie de Farber...).
■Aspects cliniques
Les manifestations cliniques des xanthomes varient en
fonction de leur topographie. La coloration jaune de ces lésions
peut parfois manquer, mais la vitropression la met presque
toujours en valeur. Les xanthomes peuvent constituer le
symptôme d’une maladie générale du métabolisme lipidique,
d’une altération cellulaire locale ou d’une histiocytose
généralisée.
Xanthélasma ou xanthomes palpébraux
C’est la forme la plus fréquente des xanthomes cutanés. Il
débute sur l’angle des paupières supérieures et inférieures par
¶98-725-A-10
1Dermatologie

des papules mollasses, pouvant confluer en nappes jaunâtres. Il
est souvent bilatéral et symétrique (Fig. 1). Les lésions précoces
peuvent être confondues avec un grain de milium ou un
syringome. Seulement la moitié des patients porteurs d’un
xanthélasma sont atteints d’une hyperlipidémie, le plus souvent
liée à une hypercholestérolémie.
Xanthochromie striée palmaire
Il s’agit d’une infiltration linéaire jaune des plis de flexions
des paumes et des doigts. Elle est caractéristique d’une hyperli-
pidémie mixte de type III, et est à distinguer des xanthomes
plans palmaires décrits dans les dysglobulinémies et les
cholestases.
Des xanthomes interdigitaux ou des plis axillaires et fessiers
ont été décrits, confondus parfois avec un pseudoxanthome
élastique.
Xanthomes plans diffus
Ils correspondent à une extension en nappes de lésions
maculopapuleuses touchant souvent le tronc et la racine des
membres de façon symétrique. Le plus souvent, ils sont associés
à des hémopathies (myélome, gammapathie monoclonale
bénigne...).
Xanthomes éruptifs
Ils sont constitués de papules discrètes jaune brun entourées
d’un halo rouge d’apparition brutale et situées le plus souvent
sur les fesses et les faces d’extension des coudes et des genoux.
Ces lésions sont parfois douloureuses ou prurigineuses puis
disparaissent en laissant une hyperpigmentation transitoire. Ils
témoignent presque toujours d’une dyslipoprotéinémie avec
hypertriglycéridémie le plus souvent.
Xanthomes tubéreux
Ces éléments nodulaires (mesurant jusqu’à quelques centimè-
tres) sont indolores, lisses à bords réguliers. Ils siègent habituel-
lement aux zones de pression (coude, genoux, fesses) et peuvent
être formés par la coalescence de lésions plus petites (Fig. 2). Ils
s’observent chez les patients atteints d’hyperlipidémie.
Xanthomes tendineux
Ce sont des lésions cutanées profondes qui sont localisées
principalement dans la région du tendon d’Achille (Fig. 3)et
des extenseurs des doigts. La peau en regard est de couleur
normale ou bistre. Ils sont mobiles sous la peau et indolores. Ils
constituent le plus souvent le symptôme d’hypercholestérolémie
familiale. L’échographie peut permettre de les dépister et suivre
leur évolution
[3]
.
■Aspect anatomopathologique
À l’examen histologique, on observe dans le derme et l’hypo-
derme la présence de fibroblastes, d’histiocytes souvent qualifiés
de spumeux et parfois de cellules géantes dites de Touton
caractérisées par une multinucléation en couronne avec pré-
sence de gouttelettes lipidiques intracytoplasmiques (Fig. 4).
Une réaction inflammatoire est souvent observée de nature
polymorphe (lymphocytes, polynucléaires). Les lipides sont
habituellement dissous par les fixations et les colorations
standards (hématéine-éosine). Ils peuvent être visibles sous la
forme de cristaux biréfringents en lumière polarisée. Certaines
colorations (noir Soudan, oil red O) peuvent être utilisées afin
de confirmer la nature lipidique des dépôts intracellulaires.
Figure 1. Xanthélasma des paupières.
Figure 2. Xanthomes tubéreux.
Figure 3. Xanthomes tendineux.
Figure 4. Infiltrats xanthomateux de cellules spumeuses avec cellules
géantes de Touton.
98-725-A-10
¶
Xanthomes
2Dermatologie

Enfin, les études biochimiques permettent de connaître la
nature de surcharge lipidique. L’aspect peut être différent selon
le type clinique de xanthomes. Les lésions récentes sont plus
riches en triglycérides, puis en cholestérol. Au début, les
xanthomes s’accompagnent d’une réaction inflammatoire,
secondairement les cellules xanthomateuses sont prépondéran-
tes puis les lésions vieillies sont fibreuses.
■Rappel du métabolisme
des lipoprotéines
[4, 5]
Les lipides sanguins sont composés de cholestérol (libre et
estérifié), de triglycérides et de phospholipides, molécules
hydrophobes circulant dans le sang sous forme de particules
hydrosolubles : les lipoprotéines. Celles-ci sont des particules
hétérogènes isolables selon leur densité par ultracentrifugation
(very low density lipoproteins [VLDL], low density lipoproteins [LDL],
intermediate density lipoproteins [IDL], high density lipoproteins
[HDL] et chylomicrons) ou par électrophorèse (alpha, pre-beta,
broad-beta et beta-lipoproteins). Il existe ainsi cinq grandes classes
de lipoprotéines : les volumineux chylomicrons qui ne migrent
pas en électrophorèse, les très légères VLDL ou pre-
betalipoproteins, les légères LDL ou beta lipoproteins, les IDL ou
broad-betalipoproteins, les lourdes HDL ou alphalipoproteins. Une
autre lipoprotéine apparaît en bande étroite à l’électrophorèse
nommée la Lp(a). Les apolipoprotéines (apo) permettent le
chargement des lipides et dirigent leur devenir. Les apo sont
classées et dénommées par une lettre de l’alphabet dont les
principales sont les apo-A, les apo-B (B-48 et B-100), les apo-C
(C-II), les apo-E et les apo-D. La composition en apo est
différente selon la classe des lipoprotéines conférant à chacune
un rôle propre.
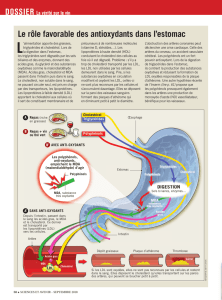
Le métabolisme des lipoprotéines (Fig. 5) commence par la
synthèse des chylomicrons formés dans la lumière intestinale à
partir des triglycérides alimentaires exogènes. Ils sont ensuite
déversés par le canal thoracique dans la circulation sanguine.
Puis ils sont hydrolysés par la lipoprotéine lipase (LPL) avec
l’aide d’un cofacteur (la lipoprotéine apo-CII) qui libère les
triglycérides donnant les acides gras libres. Les « remnants » ou
particules résiduelles sont captées par le foie et transformées en
VLDL. Ces particules, synthétisées en dehors des repas, trans-
portent des triglycérides endogènes et du cholestérol estérifié et
les délivrent aux tissus. Les VLDL sont ensuite dégradés par la
lipoprotéine lipase en remnants de VLDL et en IDL qui sont
captés par le foie grâce à un récepteur hépatocytaire. Les VLDL
et IDL non internalisés au sein des hépatocytes s’enrichissent en
cholestérol pour donner les LDL sous l’action de la lipase
hépatique. Le cholestérol fixé aux LDL est transporté aux
cellules et tissus de l’organisme. Ce cholestérol fixé aux LDL
(LDL-C) provient d’un transfert d’apo et de cholestérol estérifié
des HDL facilité par la cholesteryl ester transfer protein (CETP).
Cette protéine échange les esters de cholestérol du HDL
(HDL-C) contre les triglycérides des VLDL et chylomicrons. Ces
LDL deviennent néfastes car elles dévient leur métabolisme vers
les voies de l’athérogenèse. Ainsi, le LDL-C est appelé « mauvais
cholestérol ». Le rôle essentiel des HDL est l’épuration du
cholestérol en excès des cellules, puis son transfert au foie afin
d’être éliminé dans la bile. Les HDL évitent ainsi le dépôt des
molécules de cholestérol notamment sur les parois vasculaires.
Donc le HDL-C est surnommé le « bon cholestérol ».
■Diagnostic
d’une dyslipoprotéinémie
[4, 6]
Nous indiquons ici les principaux examens à pratiquer dans
le cadre du dépistage, du diagnostic et du traitement des
dyslipidémies et de son suivi. Ces recommandations sont
complémentaires et ne se substituent pas à celles de l’Afssaps
(Agence française de sécurité sanitaire des produits de santé ;
http : //agmed.sante.gouv.fr/pdf/5/rbp/dysreco.pdf). Le bilan
comporte les dosages du cholestérol total, des triglycérides et du
HDL-cholestérol (HDL-C) et le calcul du LDL-cholestérol (LDL-
C). L’aspect du sérum à jeun est spécifié. Selon les données
cliniques, une ultracentrifugation et une électrophorèse des
lipoprotéines peuvent compléter le bilan.
Dosage du cholestérol total
Il doit être dosé après un jeûne strict de 12 heures, à distance
d’une affection ou d’un traitement susceptible de modifier les
taux, par une méthode enzymatique.
Dosage du HDL-C et calcul du LDL-C
La technique par précipitation est la plus fiable. Les taux
normaux de HDL-C sont supérieurs à 0,4 g/l (1 mmol/l). Des
taux supérieurs à 0,60 g/l (1,5 mmol/l) sont anciennement
dénommés « syndrome de longévité », il permet de soustraire
un facteur de risque cardiovasculaire. Le LDL-C est calculé par
la formule de Friedewald
[7]
:
LDL-C (g/l) = cholestérol total (g/l) - HDL-C (g/l) - triglycéri-
des (g/l)/5 si les triglycérides sont inférieurs 4 g/l.
Si les triglycérides sont supérieurs à 4 g/l, le LDL-C ne peut
être calculé par cette formule, il peut être alors mesuré par une
méthode directe. Le taux normal du LDL-C est inférieur à
1,6 g/l (4,1 mmol/l) chez un patient sans facteur de risque
cardiovasculaire.
Dosage des triglycérides
Il doit être effectué après un jeûne strict de 12 heures par une
méthode enzymatique. Le taux doit être inférieur à 1,5 g/l
(1,70 mmol/l) chez l’adulte.
Cellule
Foie
IDL
IDL
Remnants
Chylomicrons
LPL
LPL
LPL
LPL
Intestin
Cholestérol
LCAT
LCAT
HDL
HDL
CETP
CETP
Triglycérides
VLDL
VLDL
Lp(a)
Lp(a)
LDL
LDL
Figure 5. Métabolismes des lipoprotéines. LCAT : lécithine-cholestérol-
acyl-transférase ; CETP : cholesterol ester transfer protein ; VLDL : very low
density lipoproteins ;LDL:low density lipoproteins ;IDL:intermediate density
lipoproteins ; HDL : high density lipoproteins ; Lp(a) : lipoprotéine (a) ; LPL :
lipoprotéine lipase.
Xanthomes
¶
98-725-A-10
3Dermatologie

Dosage des apolipoprotéines
L’apo-B explore le LDL-C et l’apo-A1 explore le HDL-C. Ces
dosages n’ont pas d’intérêt quand le dosage du HDL-C est
correctement réalisé. Dans le but de documenter un risque
vasculaire, la Lp(a) peut être dosée.
Les valeurs de références sont :
• 1, 20 g/l < apo-A1 < 2, 20 g/l ;
• 0, 55 g/l < apo-B < 1, 25 g/l ;
• Lp (a) < 300 mg/l.
■Étiologies
On distingue habituellement les xanthomatoses dyslipopro-
téinémiques et les xanthomatoses normolipidémiques. Certaines
manifestations cliniques des xanthomes sont assez évocatrices
d’une étiologie (Tableau 1).
Xanthomatoses dyslipoprotéinémiques
Elles sont séparées en deux grands groupes :
• formes associées à une dyslipoprotéinémie primitive d’origine
familiale ;
• formes associées à une dyslipoprotéinémie secondaire.
Forme avec dyslipoprotéinémie familiale
[4]
La dyslipoprotéinémie primitive est liée à une anomalie de
structure d’une enzyme intervenant dans le métabolisme
lipidique, d’une apolipoprotéine ou d’un récepteur des lipopro-
téines. Une classification a été proposée par Frederickson
(Tableau 2) qui reconnaît cinq types et deux sous-types d’hyper-
lipidémie d’origine héréditaire (I, IIa, IIb, III, IV, V). Il faut
rajouter les dyslipoprotéinémies familiales liées à une accumu-
lation des stérols inhabituels s’accompagnant de façon incons-
tante d’hyperlipidémie.
Hyperchylomicronémie (Type I ou exogène)
Cette maladie exceptionnelle (1/1 million), transmise en
récessivité est due à un déficit soit en lipoprotéine lipase ou soit
en son cofacteur en apoprotéine CII.
Les chylomicrons ne sont plus hydrolysés dans la lumière
vasculaire et s’accumulent dans le sang. Le sérum est lactescent.
Les triglycérides sont élevés (> 30 g/l) et le cholestérol normal.
Les LDL et HDL sont souvent diminués. Les manifestations
débutent dans l’enfance avec des douleurs abdominales secon-
daires à une pancréatite. La présentation cutanée correspond
aux xanthomes éruptifs. Il n’y a pas de dépôt vasculaire en
cholestérol. Le régime restrictif en graisses est la seule possibilité
thérapeutique.
Hypercholestérolémie (Type IIa)
Cette affection à transmission autosomique dominante est
responsable d’une surcharge en LDL. Elle existe sous deux
formes : hétérozygote (1/500 naissances) et homozygote (excep-
tionnelle). Elle est liée à un déficit partiel ou total des récepteurs
aux LDL (mutation du gène du récepteur apo B/E ou apo B100)
empêchant donc un LDL-C de pénétrer dans les cellules :
cholestérol total entre 3 et 5 g/l. Il peut s’exprimer sous deux
formes. Dans sa forme hétérozygote les signes se manifestent
vers l’âge de 20 ans par une athérosclérose et des lésions
cutanées à type de xanthomes tendineux, tubéreux et palpé-
braux. Leur importance est fonction du taux du cholestérol.
L’homozygotie, exceptionnelle et grave (mortalité < 30 ans), se
caractérise par la précocité des signes cutanés et vasculaires
apparaissant dans l’enfance. Un signe est très évocateur et
précoce : les xanthomes cutanés plans interdigitaux. Dans le
type IIa, le cholestérol est très élevé ainsi que les LDL et
l’apoprotéine B ; l’hypercholestérolémie essentielle est de loin la
plus fréquente des causes d’hypercholestérolémie, mais les
dépôts extravasculaires sont rares et les complications survien-
nent vers 60 ans.
Hyperlipidémies mixtes (Type IIb et III)
Hyperlipidémie combinée (Type IIb). De transmission
autosomique dominante, elle associe la forme IIa et IV et
correspond donc à une accumulation en LDL et VLDL. Il
concerne une naissance sur 200, mais ne s’exprime que chez
l’adulte. Les dépôts cutanés sont rares et les complications
vasculaires fréquentes (70 %).
Dysbêtalipoprotéinémie (Type III). Cette affection résulte de
la dégradation incomplète de VLDL avec accumulation de
lipoprotéine intermédiaire (IDL). Elle est due à un déficit en
apo-E (protéine porteuse des VLDL). L’isofocalisation des
différentes formes moléculaires d’apo-E des sujets atteints
retrouve le plus souvent un phénotype apo E2/E2. Les triglycé-
rides et le cholestérol sont augmentés. L’électrophorèse
confirme l’augmentation des IDL par la présence de broad-beta-
lipoproteins. Les premières manifestations apparaissent à 20 ans.
Tableau 1.
Type de xanthome et affection(s) associée(s).
Xanthélasma Hypercholestérolémie primitive
ou secondaire (cholestase,
hypothyroïdie)
États normolipémiques
Xanthochromie striée palmaire Hyperlipidémie de type III
Xanthomes plans diffus Dysglobulinémie
Cholestase
Xanthomes éruptifs Hypertriglycéridémie primitive
ou secondaire (diabète, alcoolisme,
estrogènes, syndrome
néphrotique...)
Hyperchylomicronémie (type I)
Xanthomes tubéreux Hyperlipidémie mixte de type III
Hypercholestérolémie primitive
ou secondaire
Xanthomes tendineux Hypercholestérolémie primitive
ou secondaire
Xanthomatose cérébrotendineuse,
sitostérolémie
Xanthomes verruciformes États normolipémiques
Xanthomes interdigitaux Hypercholestérolémie familiale
de type IIa homozygote
Tableau 2.
Caractères des hyperlipidémies primitives selon la classification de
Frederickson.
Type Aspect du sérum
et anomalies
lipoprotéinémiques
Modification du cholestérol
et des triglycérides
I Sérum lactescent
Hyperchylomicronémie
LDL et HDL normaux
ou diminués
Triglycérides augmentés
IIa Sérum clair
LDL augmentés
Apo-B augmenté
Cholestérol augmenté
IIb Sérum clair
LDL et VLDL augmentés
Apo-B augmenté
Cholestérol et triglycérides
augmentés
III Sérum lactescent
Présence IDL
HDL diminué
Cholestérol augmenté
Triglycérides très augmentés
IV Sérum lactescent
VLDL augmentés
Cholestérol augmenté
Triglycérides très augmentés
V Sérum lactescent
Hyperchylomicronémie
VLDL augmentés
Cholestérol augmenté
Triglycérides très augmentés
LDL : low density lipoproteins ; HDL : high density lipoproteins ; VLDL : very low
density lipoproteins ;IDL:intermediate density lipoproteins.
98-725-A-10
¶
Xanthomes
4Dermatologie

Un xanthélasma et des xanthomes tubéroéruptifs sont présents
associés à des xanthomes des plis palmaires et plantaires
caractéristiques. L’obésité est fréquente. Le pronostic est réservé
en raison d’une artériosclérose.
Hypertriglycéridémie de type IV
Type IV majeur. Sa fréquence est de 0,3 % dans la popula-
tion générale, souvent difficile à distinguer des hypertriglycéri-
démies associées à l’obésité, le diabète, l’alcool. Il est transmis
sous le mode autosomique dominant (dans 1/10
e
des cas) mais
est le plus souvent polygénique. Il est caractérisé par une
augmentation des VLDL. Le sérum est lactescent. L’hypertrigly-
céridémie entre 2 et 6 g/l et s’accompagne souvent d’une
élévation du cholestérol. Il est découvert soit de façon fortuite,
ou soit devant un syndrome douloureux abdominal. L’examen
clinique met en évidence une obésité et une hépatosplénomé-
galie associées, un diabète et une hypertension artérielle.
L’apparition de xanthomes de type éruptif est souvent secon-
daire à une aggravation de cette affection (déséquilibre de
diabète, écart alimentaire). La complication majeure est la
survenue de pancréatite aiguë
[8]
.
Type IV mineur. Il est fréquent et représente habituellement
25 % des dyslipidémies. L’hypertriglycéridémie est entre 1,5 et
10 g/l. Il n’entraîne pas habituellement de xanthomes.
Hypertriglycéridémie combinée de type V
Cette forme est associée à une élévation des chylomicrons et
des VLDL. Elle combine les types I et IV. Cette condition est
rare, atteignant un sur 1 000 adultes. Le sérum est trouble avec
une élévation des triglycérides (> 10 g/l) et modérée du choles-
térol. Les xanthomes sur le mode éruptif surviennent chez les
patients souvent obèses. Sur le plan général, une artériosclérose
est inconstamment présente, associée à des poussées de
pancréatite.
Dyslipoprotéinémie primitive avec accumulation de stérols
inhabituels
Ces affections exceptionnelles d’origine héréditaire se trans-
mettent sur le mode autosomique récessif.
Xanthomatose cérébrotendineuse
[9, 10]
. Elle est due à un
déficit en stérol 27-hydroxylase mitochondriale (CYP 27)
responsable de la synthèse d’acides biliaires. Cette enzyme est
codée par un gène situé sur le bras long du chromosome 2 qui
est muté dans cette affection. La xanthomatose cérébrotendi-
neuse débute dans l’enfance par un retard mental, une cataracte
et une diarrhée chronique. Les xanthomes tendineux incons-
tants qui apparaissent vers l’âge de 10 ans au niveau des
tendons d’Achille sont caractéristiques. Des xanthomes palpé-
braux et tubéreux peuvent être présents. Le diagnostic est fait
sur l’élévation du cholestanol sanguin et des alcools biliaires
urinaires. Le pronostic est sombre par la survenue des compli-
cations neurologiques (ataxie cérébelleuse) et cardiovasculaires.
Un traitement combinant un inhibiteur de HMG-CoA, l’acide
chénodésoxycholique avec une aphérèse des LDL peut permet-
tre de ralentir la progression de la maladie
[11]
.
Sitostérolémie
[12, 13]
. Cette affection est liée à une accumu-
lation de stérols végétaux, due à une incapacité des entérocytes
à estérifier ces phytostérols. L’anomalie génétique est située au
niveau du chromosome 2p21 affectant deux gènes adjacents
codant pour les transporteurs adénosine triphosphate ATP-
binding (ABCG5 et ABCG8) responsable d’hypersitostérolé-
mie
[14]
. Les xanthomes sont de type tendineux et tubéreux. Des
accidents coronariens et des arthropathies sont associés. Le
diagnostic est posé par l’élévation de sitostérol sanguin évaluée
en chromatographie, associée ou non à une hypercholestérolé-
mie. Un cas a été traité avec succès par ézétimibe
[15]
.
Maladie de Tangier
[16]
. Elle est due à une anomalie du
récepteur membranaire cellulaire ABCA1 permettant un passage
du cholestérol intratissulaire vers le milieu sanguin pour être
capté par les HDL. Les lésions débutent chez l’enfant par des
xanthomes cutanés et profonds (amygdales jaune-orangé et
atteinte hépatosplénique) dus à une accumulation de cholestéryl
esters. Au niveau sanguin on retrouve un taux bas de cholesté-
rol et des HDL associés à une hypertriglycéridémie. Des compli-
cations à type d’anémie, neuropathies périphériques et atteinte
cornéenne sont signalées.
Forme avec dyslipoprotéinémie secondaire
Les hyperlipoprotéinémies secondaires doivent être connues
car elles sont susceptibles de régresser avec le traitement du
facteur causal. La survenue de xanthomes au cours de ces
hyperlipoprotéinémies reste rare.
Au cours d’endocrinopathies
[17]
Diabète. Le défaut d’épuration des VLDL au cours du diabète
insulinodépendant est responsable d’hypertriglycéridémie. Le
déficit insulinique diminue l’activité de la lipoprotéine lipase.
Dans le diabète non insulinodépendant, l’hyperinsulinisme
entraîne une superproduction des VLDL. L’association diabète et
hyperlipidémie est fréquente. Le déséquilibre diabétique aggrave
l’hypertriglycéridémie et il est corrélé à l’intensité de la rétino-
pathie. Les xanthomes sont habituellement de type éruptif.
Hypothyroïdie. Le déficit en sécrétion d’hormone thyroï-
dienne est responsable d’une hypercholestérolémie par inhibi-
tion de son catabolisme. Il peut être retrouvé une
hypertriglycéridémie par inactivité de la lipoprotéine lipase. Les
xanthomes sont rares et ont une présentation sous forme
éruptive ou tubéreuse.
Au cours des cholestases
L’obstruction biliaire extra- ou intrahépatique acquise (cir-
rhose biliaire primitive
[18]
, cholangite sclérosante primitive
[19]
)
mais aussi congénitale par atrophie des canaux excréteurs
(syndrome d’Alagille
[20]
) entraîne une accumulation du choles-
térol sérique. Les xanthomes sont fréquents, d’aspect varié et
notamment de type plan palmaire et sont liés à l’hypercholes-
térolémie. Ils peuvent régresser après traitement médical ou
chirurgical telle la greffe hépatique au cours du syndrome
d’Alagille
[21, 22]
.
Au cours du syndrome néphrotique
La sévérité de l’hyperlipoprotéinémie habituellement mixte
est en rapport avec l’hypoalbuminémie et la protéinurie. Dans
le syndrome néphrotique, la survenue de xanthomes reste
exceptionnelle et se manifeste de façon éruptive
[23]
.
Au cours de l’intoxication alcoolique
L’abus de boissons alcoolisées inhibe l’oxydation des acides
gras hépatiques qui sont transformés en triglycérides dont une
part est reprise sous forme VLDL et l’autre part reste dans le foie
entraînant une hépatomégalie. Des xanthomes éruptifs sont
observés dans la majorité des cas
[24]
.
D’origine médicamenteuse
[17]
Certains médicaments peuvent révéler ou aggraver une
dyslipoprotéinémie préexistante (hyperlipidémie familiale,
diabète, alcoolisme). Mais la survenue de xanthomes d’origine
médicamenteuse proprement dite reste exceptionnelle.
Estrogènes (contraception orale, hormonothérapie substi-
tutive). Il s’agit le plus souvent d’une hypertriglycéridémie par
une synthèse accrue des VLDL au niveau hépatique. L’hyper-
chylomicronémie induite par l’excès de VLDL est responsable de
pancréatite. Des complications thromboemboliques peuvent se
voir. La présentation cutanée des xanthomes est de type éruptif.
Corticostéroïdes. Au cours d’une corticothérapie prolongée,
une hyperlipidémie, surtout des triglycérides, survient par
l’intermédiaire d’un hyperinsulinisme.
Rétinoïdes per os. L’élévation des triglycérides et du choles-
térol se rencontre à des fortes posologies d’isotrétinoïne dans
20 % des cas environ. Des xanthomes éruptifs peuvent
survenir
[25]
.
Citons encore. Les bêtabloquants, les diurétiques thiazidi-
ques, la cimétidine, les cyclines et la ciclosporine qui peuvent
être responsables d’une exacerbation d’une dyslipidémie latente.
Xanthomes
¶
98-725-A-10
5Dermatologie
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%