Lire l'article complet

La Lettre du Sénologue • n°40 - avril-mai-juin 2008 |13
DOSSIER THÉMATIQUE
Images en pathologie
Images in pathology
M.C. Mathieu*
* Institut Gustave-Roussy, Villejuif.
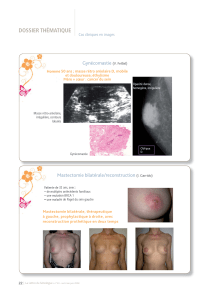
Figure 1. Les lésions de métaplasie cylindrique,
constituées par des tubes bordés de cellules cylin-
driques hautes, peuvent être associées à des micro-
calcifications classées ACR 4 ou 5. Dans la lumière
des tubes, les calcifications sont assez volumineuses.
Cette lésion est souvent associée à une hyperplasie
atypique nécessitant de réaliser une exérèse du foyer
de microcalcifications.
Figure 3. Une forme de carcinome in situ avec nécrose révélée par des microcalcifica-
tions classées ACR 5 est bien individualisée grâce à l’étude immunohistochimique de
la E-cadhérine. Il s’agit du carcinome lobulaire in situ à cellules pléiomorphes. Ces
formes étaient auparavant le plus souvent classées en carcinome intracanalaire. Lors-
qu’elles sont diagnostiquées sur pièce opératoire, le taux de composantes infiltrantes
associées est plus élevé que dans la forme classique et une exérèse complète avec des
marges saines est nécessaire, comme pour le carcinome intracanalaire.
Lésions mises en évidence
par des microcalcifications
Le développement des macrobiopsies sous stéréo-
taxie a augmenté la fréquence de diagnostic de
certaines entités histologiques. La conduite à tenir
devant certaines lésions a été redéfinie.
Figure 2. Les lésions mucocele-like peuvent être révélées par des calcifications volu-
mineuses. Ces lésions correspondent à des canaux remplis d’un matériel de sécrétion,
mucine, dont la paroi se rompt et la mucine diffuse dans le tissu mammaire. Ces lésions,
en raison de leur association fréquente avec des lésions de carcinome in situ ou de
carcinome mucineux impliquent de réaliser une vérification histologique.

14 | La Lettre du Sénologue • n° 40 - avril-mai-juin 2008
DOSSIER THÉMATIQUE Techniques en images
Figure 4. En l’absence de microcalcifications vues
histologiquement, le pathologiste doit rechercher
en polarisation les cristaux d’oxalate de calcium,
appelés cristaux de Wedellite non colorés et mal
visibles en coloration standard. Ces cristaux, situés
dans des kystes, sont tout à fait bénins.
Figure 5. Le carcinome lobulaire à cellules pléio-
morphes se distingue du carcinome lobulaire infil-
trant de forme classique par des cellules de plus
grande taille avec une anisonucléose marquée et
une activité mitotique élevée. Il est généralement
de grade histopronostique III. Le phénotype de ces
carcinomes est aussi différent de celui de la forme
classique : RE-, RP-, HER2 +, p53 + (C : canal).
Figure 6. Le carcinome de type basal, défini par les études de génomique, a un phénotype
particulier : peu différencié, RE-, RP-, HER2-, cytokératines de type basal (CK5/6, CK14),
activité mitotique élevée (T : tumeur, S : stroma).
Figure 7. Le carcinome de type luminal, défini par les études de génomique, a une
expression génique proche de celle des cellules épithéliales luminales bordant les
canaux et exprime les RE, les cytokératines CK8/18 et/ou CK19. Ces carcinomes sont
de meilleur pronostic que les formes de type basal.
Les nouvelles classifications
des carcinomes infiltrants
Figure 8. Le phénotype des tumeurs associées à BRCA1 et BRCA2 est particulier. Les
tumeurs associées à BRCA1 sont plus souvent de type basal, avec un stroma riche en
lymphocytes (proche des carcinomes médullaires) [T : tumeur, S : stroma]. Les tumeurs
associées à BRCA2 sont le plus souvent de type lobulaire.

La Lettre du Sénologue • n°40 - avril-mai-juin 2008 |15
DOSSIER THÉMATIQUE
Figure 9. Métastase de plus de 2 mm associée
à un risque d’envahissement du reste du curage
axillaire de 50 %.
Le ganglion sentinelle
Cette technique est une alternative au curage axil-
laire proposée pour des tumeurs de petite taille. Une
nouvelle classification pTNM des métastases a été
publiée en 2003. Elle nécessite de mesurer de façon
Figure 10. Micrométastase de taille située entre
0,2 et 2 mm classée pN1mi. Le risque d’envahisse-
ment du reste du curage est de l’ordre de 25%.
Figure 11. Présence d’emboles vasculaires sous-
capsulaires visibles en coloration standard mais
mieux détectés par immunohistochimie. Ces
métastases sont appelées “cellules isolées” ou
“submicrométastases” et classées pN0 (i+). Le
risque d’envahissement du reste du curage est de
l’ordre de 10 à 15%. L’intérêt de compléter le curage
axillaire est remis en question.
précise la taille des métastases. Le taux d’envahisse-
ment des ganglions non sentinelles augmente avec la
taille de la métastase dans le ganglion sentinelle. Une
étude immunohistochimique avec un anticorps anti-
cytokératines est nécessaire pour mettre en évidence
des métastases de petite taille.
Figure 12. Présence de cellules isolées non visibles
en coloration standard mais détectées par immu-
nohistochimie, classées pN0(i+) dans un carcinome
lobulaire infiltrant. Cet aspect est plus fréquent
dans les carcinomes de type lobulaire que dans
ceux de type canalaire.
0,5 mm

16 | La Lettre du Sénologue • n° 40 - avril-mai-juin 2008
DOSSIER THÉMATIQUE Techniques en images
Les biomarqueurs
Actuellement, ce sont les marqueurs prédictifs de
réponse ou traitement ou cibles thérapeutiques tels
que les récepteurs hormonaux et HER2 qui sont
détectés en routine par immunohistochimie dans les
carcinomes infiltrants. HER2, cible du trastuzumab et
du lapatinib, peut être détecté par différentes tech-
niques. La qualité et la fiabilité de cette détection
est essentielle pour une bonne indication du traite-
ment. Des recommandations émises par l’American
Society of Clinical Oncology ont modifié les critères
d’évaluation de HER2 en 2007. Une adhésion du
laboratoire de pathologie à une structure de contrôle
de qualité tels que l’AFAQAP (France) ou UK-NEQAS
(Royaume-Uni) est nécessaire. O
Figure 13. L’évaluation de RE et de RP est impor-
tante car il a été montré par l’étude ATTAC que
les tumeurs du sein RE+/RP- répondaient mieux
à l’anastrozole qu’au tamoxifène.
Figure 15. Carcinome avec une amplification de
HER2 par hybridation in situ fluorescente (FISH).
Plus de 20 copies du gène HER2 sont mises en
évidence grâce à une sonde fluorescente rouge et
2 à 4 copies du centromère du chromosome 17 sur
lequel est situé le gène HER2 sont marquées en vert.
Une tumeur est amplifiée si le ratio du nombre de
copies de HER2/nombre de copies du chromosome
17 est > 2,2. Cette recherche de l’amplification du
gène HER2 est faite pour les tumeurs de score 2+ en
immunohistochimie.
Figure 16. Carcinome avec amplification du gène
HER2 par hybridation in situ chromogène (CISH).
Le nombre de copies (ici en marron) est de l’ordre de
20. L’avantage de cette technique est une meilleure
préservation du tissu et une bonne conservation
des lames. Le centromère du chromosome 17 peut
maintenant être recherché par CISH.
Figure 14. Une surexpression de HER2 de score 3+
est définie par un marquage immunohistochimique
membranaire continu d’intensité forte de plus de
30% des cellules carcinomateuses. Des recomman-
dations émises par l’American Society of Clinical
Oncology ont modifié les critères d’évaluation de
HER2 en 2007.
1
/
4
100%