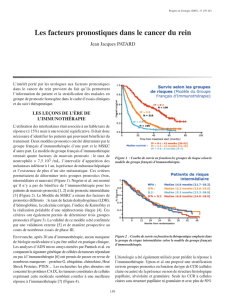
Facteurs pronostiques dans les cancers du rein localisés et métastatiques d

La Lettre du Cancérologue - Vol. XV - n° 5 - octobre 2006
236
Dossier thématique
Dossier thématique
DE L’UTILITÉ DE DÉFINIR DES SYSTÈMES
PRONOSTIQUES FIABLES DANS LE CANCER
DU REIN
Pourquoi est-il utile de disposer de systèmes pronostiques
fi ables, tant dans le cadre du cancer localisé que du cancer du
rein métastatique ?
Facteurs pronostiques dans les cancers du rein localisés
et métastatiques
Prognostic factors in localized and in metastatic renal cell carcinomas
IP J.J. Patard*
* Service d’urologie, CHU de Rennes.
Tout d’abord dans un but d’information. À l’ère de la consulta-
tion d’annonce, il existe une exigence grandissante de donner
au patient des informations précises et complètes et de pouvoir
décliner celles-ci en termes de risque individuel.
Deuxièmement, le risque de récidive, de progression ou de
décès par cancer est important à apprécier pour pouvoir
déterminer des protocoles de surveillance adaptés, tant pour
le rythme que sur le plan des outils biologiques ou d’ima-
gerie nécessaires à mettre en œuvre. Ce n’est un objectif
intéressant, mais qui n’est pas encore atteint en l’état actuel
des connaissances.
RÉSUMÉ
Il est utile de disposer de facteurs et de systèmes pronostiques
fi ables pour prendre en charge les cancers du rein dans le triple
but d’informer les patients, de leur proposer des algorithmes
de suivi rationnels et enfi n de leur off rir des traitements ou de
les intégrer à des essais cliniques adaptés à leur risque.
On distingue des facteurs pronostiques : anatomiques (inté-
grés dans la classifi cation TNM), histologiques (comme le
grade de Fuhrman ou le type histologique), cliniques (comme
les symptômes ou le performance status) et enfi n biologiques
ou moléculaires.
Afi n d’améliorer la performance pronostique des systèmes
usuels comme le système TNM, des systèmes pronostiques
plus complexes combinant plusieurs variables indépendantes
ont été mis au point. Dans le cancer du rein localisé, les deux
systèmes les plus effi caces sont l’UCLA Integrated Staging System
(UISS) et le “Stage” “Tumor Size” “Fuhrman Grade” “Tumors
Necrosis” (SSIGN). Dans les cancers du rein métastatiques, les
deux systèmes pronostiques prédictifs de la réponse à l’immu-
nothérapie qui ont été largement utilisés sont le modèle du
Groupe français d’immunothérapie et le modèle de Motzer.
On évolue maintenant vers des systèmes qui combineront
des variables cliniques, pathologiques et moléculaires.
Mots-clés : Carcinome - Cancer du rein - Pronostic - Survie.
SUMMARY
It is useful to have reliable prognostic factors in Renal Cell
Carcinoma (RCC) for 3 major goals: providing patient
information, designing rationale follow-up algorithms
and selecting patients for adapted treatment schedules
as well as new clinical trials.
Prognostic factors in RCC include: anatomical (TNM clas-
si cation), histological (Fuhrman grade and histological
subtype), clinical (symptoms and performance status) and
molecular factors.
For improving predictive accuracy of prognostic systems
such as the TNM classi cation, new prognostic algorithms
or nomograms have been designed combining indepen-
dent prognostic variables. UISS and SSIGN are the two
most eff ective prognostic systems within localized RCC. In
metastatic disease, the two main systems that have been
used for predicting response to immunotherapy are the
model of the French Group of Immunotherapy and the
Motzer model.
Finally, there is an increasing interest in combining mole-
cular variables with previously established models. These
new systems will require further validation as part of large
prospective clinical trials.
Keywords: Carcinoma - Renal cell - Prognostic - Survival.

La Lettre du Cancérologue - Vol. XV - n° 5 - octobre 2006
Dossier thématique
Dossier thématique
237
Enfi n, l’aspect le plus important et qui se développe particuliè-
rement à l’heure actuelle est celui de l’utilisation des systèmes
pronostiques pour sélectionner les patients en fonction de leur
risque soit pour des essais cliniques, soit pour des traitements
qui ont fait la preuve de leur effi cacité dans certains groupes.
LES CRITÈRES PRONOSTIQUES USUELS
On distingue, parmi les facteurs pronostiques classiques, les
facteurs anatomiques, histologiques, cliniques et moléculaires.
Les facteurs anatomiques
Ils comprennent la taille de la tumeur, l’invasion veineuse (veine
rénale, veine cave inférieure), le dépassement de la capsule rénale,
l’envahissement des ganglions locorégionaux et l’existence de
métastases à distance. Tous ces facteurs sont pris en compte
par la classifi cation TNM. La version actuelle de la classifi cation
TNM date de 2002. Il existe cependant encore de nombreux
sujets de controverse quant à la validité de certaines variables
de cette version. La sous-stratifi cation des tumeurs T1, qui
est la principale modifi cation de la version 2002, a été validée
par de nombreuses études (1-3). Il est clair maintenant que le
groupe de tumeurs où des améliorations demeurent néces-
saires est le groupe des tumeurs pT3. Tout d’abord, il semble
que l’invasion de la graisse du sinus rénal soit eff ectivement un
facteur de mauvais pronostic (pT3a depuis 2002), mais il n’est
pas évident que la survie de ces patients soit la même que celle
des patients qui ont une tumeur pT3a par envahissement de
la graisse périrénale (4, 5). Deuxièmement, beaucoup d’études
suggèrent que l’invasion de la surrénale est de très mauvais
pronostic et devrait être reclassée pT4 ou stade IV plutôt que
pT3a (6, 7). Finalement, il n’est pas évident que la stratifi ca-
tion des patients qui ont un thrombus cave en pT3b, pT3c soit
valide, et des études supplémentaires sont nécessaires pour
questionner la valeur pronostique intrinsèque de la présence
d’un thrombus cave (8). Enfi n, plus récemment, la validité de la
sous-classifi cation N1-N2 pour l’envahissement ganglionnaire a
été remise en cause (9). La question essentielle pour établir les
stades N et M est de savoir quels moyens ont été utilisés pour
cette stadifi cation. La classifi cation TNM 2002 donne une limite
de 8 ganglions prélevés pour un staging adéquat en deçà duquel
le patient devrait être classé Nx. En pratique, cette limite n’est
presque jamais atteinte, en particulier en cas de néphrectomie
partielle ou de néphrectomie laparoscopique. Pour l’établis-
sement du stade M, même si aucune recommandation n’est
donnée, il semble évident que le scanner thoraco-abdominal
est l’examen de référence.
Les facteurs histologiques
Ils incluent le grade de Fuhrman, le sous-type histologique,
la présence de contingents sarcomatoïdes, l’invasion micro-
vasculaire, la nécrose tumorale et l’invasion du système collec-
teur. Le grade nucléaire de Fuhrman est le critère pronostique
histologique le plus largement accepté (10). Bien que ses princi-
pales limites tiennent à des variations intra- et inter observateur
qui existent pour tous les grades histologiques, diff érentes études
ont confi rmé que le grade de Fuhrman gardait sa valeur pronos-
tique indépendante quel que soit l’investigateur, et même si
l’on envisageait des regroupements de grades de manière à le
simplifi er et à le rendre plus reproductible (11).
Selon la classifi cation OMS (12) [www.uicc.org/tnm], il existe
trois sous-types histologiques principaux de cancer à cellules
rénales : les types à cellules claires, tubulo-papillaires et chro-
mophobes, qui représentent respectivement 80 à 90 %, 10 à
15 % et 4 à 5 % des cas. De nombreuses études ont montré
que le sous-type histologique avait une valeur pronostique en
analyse univariée, le carcinome à cellules claires étant la forme
la plus agressive, suivi par les carcinomes papillaires puis par
le carcinome chromophobe (13, 14). Cependant, cette valeur
pronostique disparaît en analyse multivariée, suggérant que le
stade et le grade ont un rôle plus déterminant pour le devenir
que le sous-type histologique (14).
Parmi les carcinomes papillaires, on distingue deux sous-groupes
de profi ls pronostiques radicalement diff érents (15). Les carci-
nomes papillaires de type I sont habituellement de bas grade et
ont un pronostic très favorable. Les carcinomes papillaires de
type II sont essentiellement de haut grade et ont un très haut
potentiel métastatique.
Les facteurs cliniques
Ils incluent le performance status (ECOG, index de Karnofsky),
les symptômes locaux, la cachexie, l’anémie (16).
Les facteurs moléculaires
Il existe de nombreux marqueurs moléculaires qui ont été
explorés et qui sont candidats à être des facteurs pronostiques
dans le cancer du rein. Parmi ceux-ci, on retiendra : CaIX,
VEGF, hypoxia-inducible factor (HIF), Ki67, p53, PTEN,
E-cadhérine, CD44 (17). La limite actuelle à l’usage de ces
marqueurs est que, dans la plupart des études, ils ont été testés
dans des cohortes de taille modeste, et surtout que leurs perfor-
mances pronostiques n’ont pas été comparées de manière fi able,
ni entre elles, ni à celles des systèmes pronostiques usuels.
On espère, par ailleurs, que l’étude des profi ls d’expression de
gènes dans des groupes défi nis permettra à l’avenir de défi nir
de nouveaux marqueurs moléculaires.
LES SYSTÈMES PRONOSTIQUES DANS LE CANCER
DU REIN LOCALISÉ
La classifi cation TNM et le grade de Fuhrman on un rôle prédo-
minant en tant que systèmes pronostiques dans le cancer du rein
localisé. Cependant, ces systèmes sont souvent pris en défaut du
fait de l’évolution parfois imprévisible du cancer du rein. Ainsi, il
peut y avoir une grande variabilité biologique et de devenir entre
une tumeur T1G1 de 4 cm et une tumeur T1G4 de 6 cm, même

La Lettre du Cancérologue - Vol. XV - n° 5 - octobre 2006
Dossier thématique
Dossier thématique
238
0,50
0,25
0,00
0 24 48 72 96 120 144
0,75
1,00 Bas risque
Risque intermédiaire
Haut risque
Pourcentage de survie
Figure 2.
Strati cation des patients ayant un cancer localisé
par l’UISS en trois groupes de survies signi cativement di é-
rentes dans une cohorte multicentrique de 3 119 patients.
Figure 1.
Le système UISS permettant de dé nir trois groupes
de risque dans le cancer du rein localisé repose sur le stade
TNM, le grade de Fuhrman et l’ECOG (performance status).
Stade T 1 2
Intermédiaire
3 4
Grade
nucléaire 1-2 3-4 1 > 1
ECOG PS
Risque
0
Bas Haut
≥ 1 0 ≥ 1 0 ≥ 1 0 ≥ 1
si, sur le plan du “stade” TNM, ce sont les mêmes tumeurs. En
eff et, quand on compare la précision pronostique des systèmes
usuels sur la base de l’index c de Harrel, on s’aperçoit que celui-ci
est à 0,65 pour le grade de Fuhrman, à 0,66 pour l’ECOG et à 0,77
pour le TNM, 0,5 étant la prédiction due au hasard et 1 étant
la prédiction parfaite (18). Certains auteurs ont donc, afi n de
mieux traduire la complexité biologique des tumeurs, combiné
dans des algorithmes diff érentes variables pronostiques indépen-
dantes afi n d’augmenter la précision pronostique des modèles.
Le premier à avoir eu une telle approche a été M.W. Kattan (19).
Son système, qui est un nomogramme, combine les symptômes
au diagnostic, le sous-type histologique (cellule claire, papillaire,
chromophobe), la taille de la tumeur et le stade TNM 1997. Ce
système n’a été validé qu’une fois en externe par notre groupe
à l’occasion d’une comparaison entre modèles pronostiques, et
sa précision prédictive n’était que de 0,77, c’est-à-dire pas très
diff érente du stade TNM (20). Le modèle de Kattan n’est pas
utilisé en pratique mais est intéressant dans son concept.
Le deuxième système pronostique majeur est l’UISS (fi gure 1). Il
combine stade TNM, grade de Fuhrman et ECOG et comprend
une variante pour la maladie localisée et une autre pour la
maladie métastatique (21). Sa grande force est d’avoir été validé
à plusieurs reprises par des groupes externes, dont le nôtre, à
l’occasion d’une étude coopérative multicentrique internationale
(22). Cette étude comprenait plus de 4 000 patients provenant
de 8 centres internationaux. Dans le cancer du rein localisé, le
système prédictif fonctionnait dans tous les centres quels que
soient le profi l d’agressivité des tumeurs et le type de recrutement
ou de pratique des centres (fi gure 2). En moyenne, la valeur
prédictive était de 0,8, c’est-à-dire substantiellement meilleure
que celle du TNM. Le système montrait donc, au moins dans
la maladie localisée, une bonne précision pronostique et une
bonne reproductibilité, ce qui est important pour un usage
potentiellement large. Ce système va être utilisé de manière
prospective au cours de deux essais adjuvants pour stratifi er
les patients ayant des formes de cancer du rein à risque dans
le cadre de traitements antiangiogéniques (essais ECOG 2805
et START).
Le troisième système pronostique important est le SSIGN.
Ce système n’a été mis au point que pour les variétés histo-
logiques à cellules claires. Il s’agit, comme pour les modèles
précédemment décrits, d’un modèle postopératoire qui inclut
des variables anatomiques et histologiques. Il n’inclut pas de
variables cliniques, à la différence du modèle de Kattan et de
l’UISS. Ce modèle n’a été validé de manière externe qu’une
seule fois dans le cadre d’une petite série monocentrique
(23). Cependant, la précision pronostique retrouvée était
de 0,88, ce qui en fait potentiellement un des modèles les
plus pertinents. La contrainte en est toutefois la nécessité de
disposer systématiquement, de la part de l’uropathologiste,
d’une évaluation de la nécrose tumorale. Cette variable est
très intéressante, car elle est sans doute une mesure indirecte
des phénomènes d’hypoxie et est probablement reliée à HIF
et VEGF, ce qui reste néanmoins à vérifier. Il est aussi à noter
que ce modèle sera utilisé pour stratifier les patients de risque
intermédiaire et élevé dans le cadre d’un essai adjuvant (essai
SORCE).
LES SYSTÈMES PRONOSTIQUES DANS LE CANCER
DU REIN MÉTASTATIQUE
Si le système TNM joue un rôle majeur dans la prédiction
pronostique des tumeurs localisées ou localement avancées,
soit seul, soit intégré à des modèles prédictifs, il n’en est pas de
même en situation métastatique. En eff et, toutes les tumeurs
métastatiques par défi nition sont de stade IV et le plus souvent
de haut grade. Il faut donc identifi er d’autres paramètres perti-
nents. L’identifi cation de paramètres biologiques ou moléculaires
trouve ici tout son intérêt tant les paramètres anatomiques ou
cliniques sont uniformes et fi xés.
Les différents modèles pronostiques qui ont été élaborés
jusqu’alors sont principalement des modèles prédictifs de
la réponse à l’immunothérapie. Là encore, il a été compris

La Lettre du Cancérologue - Vol. XV - n° 5 - octobre 2006
Dossier thématique
Dossier thématique
239
que combiner plusieurs variables était plus pertinent que
d’utiliser une variable seule, même si celle-ci est un puissant
facteur pronostique. Un des principaux modèles pronosti-
ques qui ont prouvé leur utilité est le modèle du Groupe
français d’immunothérapie. Il repose schématiquement sur
le nombre de polynucléaires neutrophiles, sur l’intervalle
entre le diagnostic initial et la survenue de métastases, sur la
présence de métastases hépatiques et sur le nombre de sites
métastatiques. Sur cette base, trois groupes ont été définis,
selon que le pronostic est bon, intermédiaire ou mauvais
(médiane de survie : 42, 15 et 6 mois respectivement) [24].
Par la suite, la principale utilité de ce modèle a été de stra-
tifier les patients pour des essais cliniques, et il a pu être
clairement démontré que les patients de mauvais pronostic
et à risque intermédiaire ne bénéficiaient pas du traitement
à base d’IFN et d’IL-2. Ainsi, un modèle pronostique a pu
contribuer à une avancée majeure dans la prise en charge
des patients métastatiques.
Le deuxième modèle le plus largement utilisé est celui de
Motzer. Il a lui aussi subi quelques modifi cations depuis sa
conception, mais repose schématiquement sur les taux de LDH,
d’hémoglobine, de calcium corrigé, sur l’index de Karnofsky et
sur la réalisation préalable d’une néphrectomie. Il en résulte
le calcul d’un score et la défi nition de trois groupes pronosti-
ques. Les survies médianes pour ces trois groupes sont de 20,
10 et 4 mois (25). Ce modèle a été validé de manière externe
(26) et a été utilisé de manière prospective comme système
de stratifi cation pour de nombreux essais, incluant les essais
récents qui ont abouti à l’autorisation de mise sur le marché
des nouvelles drogues antiangiogéniques (27).
Malgré plus de 20 ans d’utilisation de l’immunothérapie comme
traitement standard du cancer du rein métastatique, on n’a pu
défi nir de facteur biologique prédictif fi able. On a beaucoup
insisté sur la valeur pronostique du sous-type histologique
et des variables pathologiques. Il a d’ailleurs été établi un
modèle prédictif de la réponse à l’IL-2 uniquement fondé sur
des variables pathologiques : proportion de cellules claires, de
contingents papillaires, alvéolaires et granulaires (28). Finale-
ment, la seule variable moléculaire qui semble émerger comme
facteur prédictif intéressant à la fois pour l’immunothérapie
et potentiellement pour les antiangiogéniques est le CaIX
(29). Cette anhydrase carbonique, qui joue un rôle dans le ph
extracellulaire, est sous le contrôle de HIF et, comme VEGF,
s’accumule quand VHL est inactivé. Cependant, comme on l’a
indiqué précédemment, il est peu vraisemblable qu’une variable
seule émerge comme un facteur pronostique universel répon-
dant à toutes les situations cliniques et à toutes les variétés
histologiques. Il faudra tester son intégration à des systèmes
pronostiques déjà constitués et évaluer si l’ajout de telle ou
telle variable augmente la prédiction pronostique du système
(18). De ce point de vue, il est aussi probable que l’étude des
profi ls d’expression géniques comparant diff érents groupes
pronostiques nous conduira à l’identifi cation de nouveaux
marqueurs (30).
CONCLUSION ET PERSPECTIVES :
L’AVENIR DES SYSTÈMES PRONOSTIQUES
La classifi cation TNM et les critères histologiques comme
le grade restent l’ossature des systèmes pronostiques dans le
cancer du rein localisé. Cependant, nous avons vu que nous
évoluons de plus en plus vers des systèmes intégrés qui combi-
nent plusieurs variables pronostiques indépendantes. Ces
systèmes sont particulièrement utiles en situation de cancer
localisé pour décider d’un protocole adapté de surveillance
ou d’un traitement adjuvant. En situation métastatique, les
systèmes sont encore plus déterminants, tant TNM et grade
sont pris en défaut. L’évaluation du risque dans cette situation
se décline plus particulièrement en termes de prédiction de la
réponse à un traitement. C’est pourquoi l’introduction dans les
systèmes pronostiques de variables biologiques et moléculaires,
qui sont des éléments clés de la progression métastatique et
du mode d’action des thérapeutiques ciblées, est un espoir
tout à fait concret. En l’état actuel de notre connaissance,
des nomogrammes prédictifs sont maintenant en mesure de
répondre à la question de savoir si l’ajout de telle ou telle
variable va améliorer la précision pronostique du modèle. En
eff et, il faudra apporter la preuve que ces variables moléculaires
font mieux en termes de prédiction que les variables cliniques
ou biologiques actuellement utilisées. ■
RéféRences bibliogRaphiques
1. Frank I, Blute ML, Leibovich BC et al. Independent validation of the 2002
American Joint Committee on cancer primary tumor classifi cation for renal cell
carcinoma using a large, single institution cohort. J Urol 2005;173:1889-92.
2. Salama ME, Guru K, Stricker H et al. pT1 substaging in renal cell carcinoma:
validation of the 2002 TNM staging modifi cation of malignant renal epithelial
tumors. J Urol 2005;173:1492-5.
3. Ficarra V, Schips L, Guille F et al. Multi-institutional European validation of
the 2002 TNM staging system in conventional and papillary localized renal cell
carcinoma. Cancer 2005;104:968-74.
4. Bonsib SM. e renal sinus is the principal invasive pathway: a prospective
study of 100 renal cell carcinomas. Am J Surg Pathol 2004; 28:1594-600.
5. ompson RH, Leibovich BC, Cheville JC et al. Is renal sinus fat invasion
the same as perinephric fat invasion for pT3a renal cell carcinoma? J Urol
2005;174:1218-21.
6. Han KR, Bui MH, Pantuck AJ et al. TNM T3a renal cell carcinoma: adrenal
gland involvement is not the same as renal fat invasion. J Urol 2003;169:899-
903; discussion 903-4.
7. ompson RH, Leibovich BC, Cheville JC et al. Should direct ipsilate-
ral adrenal invasion from renal cell carcinoma be classifi ed as pT3a? J Urol
2005;173:918-21.
8. ompson RH, Cheville JC, Lohse CM et al. Reclassifi cation of patients with
pT3 and pT4 renal cell carcinoma improves prognostic accuracy. Cancer 2005;
104:53-60.
9. Terrone C, Cracco F, Porpiglia F et al. Reassessing the current TNM lymph
node staging for Renal Cell Carcinoma. European Urology 2006; In press.

La Lettre du Cancérologue - Vol. XV - n° 5 - octobre 2006
Dossier thématique
Dossier thématique
240
DDB - Ciel & Terre - ASY 201 - 09/06 - © Pfizer. Tous droits réservés - SAS 2005 au capital de 38200 euros - RCS PARIS 433 623 550 - Locataire gérant de Pfizer Holding France
Aromasine®est indiqué dans le traitement adjuvant du cancer du sein
invasif à un stade précoce exprimant des récepteurs aux œstrogènes,
chez les femmes ménopausées, à la suite d'un traitement adjuvant
initial d'une durée de 2 à 3 ans par tamoxifène**.
DÉNOMINATION : AROMASINE®25 mg, comprimé enrobé. COMPOSITION* : Exemestane 25 mg.
DONNÉES CLINIQUES* Indications thérapeutiques : Aromasine®est indiqué dans le traitement
adjuvant du cancer du sein invasif à un stade précoce exprimant des récepteurs aux estrogènes,
chez les femmes ménopausées, à la suite d’un traitement adjuvant initial d’une durée de 2 à
3 ans par tamoxifène. Aromasine®est indiqué dans le traitement du cancer du sein à un stade
avancé chez la femme ménopausée naturellement ou artificiellement après échec du traitement par
antiestrogènes. L’efficacité n’a pas été démontrée chez les patientes dont les cellules tumorales ne possèdent
pas de récepteurs aux estrogènes. Posologie et mode d'administration* : Adultes et personnes âgées : Dose recommandée :
25 mg par jour de préférence après un repas. Maintien du traitement jusqu'à apparition des signes de progression de la tumeur. Cancer
du sein, stade précoce : Maintien du traitement par Aromasine®jusqu’à 5 ans d’hormonothérapie séquentielle (tamoxifène suivi d’Aromasine®). Arrêt du traitement
si rechute de la tumeur. Cancer du sein, stade avancé : Maintien du traitement par Aromasine®jusqu'à apparition des signes de progression de la tumeur. Insuffisance
hépatique ou rénale : aucun ajustement posologique. CTJ : 4,81 �. Enfants : non recommandé. Contre-indications : Aromasine®est contre-indiqué chez les patientes
présentant une hypersensibilité connue au principe actif ou aux excipients, chez la femme en pré-ménopause et chez la femme enceinte ou qui allaite. Mises en
garde spéciales et précautions particulières d’emploi* : Ne pas administrer chez la femme en pré-ménopause (confirmer si nécessaire la ménopause par dosages
de LH, FSH et estradiol). Administrer avec précautions en cas d’insuffisance hépatique ou rénale. Contient du saccharose : ne pas administrer en cas de maladies
héréditaires rares d’intolérance au fructose, de malabsorption glucose/galactose ou d’un déficit en sucrase-isomaltase. Contient du parahydroxybenzoate de méthyle :
possibilité de réactions allergiques (retardées). Aromasine®étant un puissant inhibiteur de la synthèse oestrogénique, possibilité de diminution de la densité minérale
osseuse (DMO). Impact non démontré sur le risque de fracture à long terme. En début de traitement adjuvant par Aromasine®, évaluer la DMO par ostéo-densitométrie
chez les femmes atteintes ou à risque d’ostéoporose. Malgré l’absence de données sur les effets d’un traitement sur la DMO induite par Aromasine®, mettre en
place un traitement de l’ostéoporose si besoin. Les patientes traitées par Aromasine®devront être surveillées étroitement. Interactions avec d’autres médicaments
et autres formes d’interactions* : • In vitro, métabolisation par le CYP3A4 et les aldocétoréductases. Pas d’inhibition des principales isoenzymes du CYP. • Inhibiteur
du CYP3A4 (kétoconazole) : aucun effet significatif sur la pharmacocinétique de l’exemestane en clinique. • Inducteurs du CYP3A4 (rifampicine, anticonvulsivants
comme phénytoïne, carbamazépine, préparations à base de millepertuis) : possible réduction de l’efficacité d’Aromasine®. • Médicaments à marge thérapeutique
étroite et métabolisés par le CYP3A4 : précaution. • Autres médicaments anticancéreux : pas d’expérience clinique d’une utilisation concomitante. • Médicaments
contenant des estrogènes : pas de co-administration car risque d’annulation de l’action pharmacologique. Grossesse et allaitement* : Contre-indiqué. Effets sur
l’aptitude à conduire des véhicules et à utiliser des machines*: Avertir les patientes du risque d'altération des capacités physiques et/ou mentales nécessaires pour
conduire des voitures ou utiliser des machines si apparition d’assoupissement, somnolence, asthénie, vertiges. Effets indésirables : Effets indésirables généralement
légers à modérés. Patientes atteintes de cancer du sein à un stade précoce et recevant un traitement adjuvant par Aromasine®après un traitement adjuvant initial
par tamoxifène : taux d’arrêt du traitement pour effets indésirables dans les études cliniques : 6,3% ; effets indésirables les plus fréquemment rapportés : bouffées
de chaleur (22%), arthralgies (17%) et fatigue (17%). Patientes atteintes de cancer du sein à un stade avancé et recevant la dose standard de 25 mg : taux d’arrêt
du traitement pour effets indésirables dans les études cliniques : 2,8% ; effets indésirables les plus fréquemment rapportés : bouffées de chaleur (14%) et nausées
(12%). La plupart des effets indésirables peut être attribuée aux conséquences pharmacologiques normales de la carence en estrogènes (bouffées de chaleur,
par exemple). Les effets indésirables rapportés sont listés ci-dessous par fréquence. Leur fréquence est définie comme suit : très fréquent (≥1/10), fréquent
(> 1/100 à < 1/10), peu fréquent (> 1/1000 à ≤1/100), rares (> 1/10000 à ≤1/1000).
• Très fréquents : insomnie, céphalées, bouffées de chaleur, nausées, augmentation de la
sudation, douleurs articulaires et musculosquelettiques (arthralgies et, moins fréquemment,
douleurs au niveau des membres, ostéoarthrite, douleurs dorsales, arthrite, myalgie et raideurs
articulaires), fatigue. • Fréquents : anorexie, dépression, sensations vertigineuses, syndrome du
canal carpien, douleurs abdominales, vomissements, constipation, dyspepsie, diarrhée, éruption cutanée
transitoire, alopécie, douleurs, œdème périphérique. • Peu fréquents : somnolence, asthénie. Affections
hématologiques et du système lymphatique : Patientes atteintes d’un cancer du sein à un stade avancé : cas de
thrombocytopénies et de leucopénies rarement rapportées. Diminution occasionnelle des lymphocytes chez approximativement 20 %
des patientes recevant Aromasine®, en particulier chez celles présentant déjà une lymphocytopénie. Pas de modification significative au cours du temps des valeurs
moyennes des lymphocytes et aucune augmentation des infections virales n'a été observée. Patientes atteintes d’un cancer du sein à un stade précoce : ces effets
n’ont pas été observés. Affections hépatobiliaires : Très fréquent : légère élévation des phosphatases alcalines (pouvant être due à une accélération du renouvellement
osseux). Fréquents : légère élévation de la bilirubine (dans la plupart des cas, non associée à une élévation des enzymes hépatiques). La fréquence des événements
indésirables et affections prédéfinis dans l’étude sur le cancer du sein à un stade précoce (IES), quelle que soit la causalité, rapportés chez des patientes sous
traitement et jusqu’à 30 jours après l’arrêt de celui-ci est listée ci-après. Nombre d’évènements indésirables et affections respectivement par traitement par exemestane
(n = 2252) ou par tamoxifène (n=2279) : Bouffées de chaleur : 488 (21,7%) - 456 (20,0%) - Fatigue : 372 (16,5%) - 345 (15,1%) – Céphalées : 303 (13,5%)
- 255 (11,2%) – Insomnie : 279 (12,4%) - 199 (8,7%) – Augmentation de la sudation : 270 (12,0%) - 242 (10,6%) – Sensations vertigineuses : 225 (10,0%)
- 197 (8,6%) – Nausées : 199 (8,8%) - 205 (9,0%) – Ostéoporose : 116 (5,2%) - 65 (2,9%) – Hémorragie vaginale : 87 (3,9%) - 109 (4,8%) – Affections gynécologiques :
81 (3,6%) - 154 (6,8%) – Autre cancer primitif : 56 (2,5%) - 84 (3,7%) – Vomissements : 51 (2,3%) - 52 (2,3%) – Troubles de la vision : 44 (2,0%) - 48 (2,1%)
– Affection cardiovasculaire : 21 (0,9%) - 39 (1,7%) – Fracture ostéoporotique : 17 (0,8%) - 13 (0,6%) – Complications thromboemboliques : 15 (0,7%)
- 40 (1,8%) – Infarctus du myocarde : 14 (0,6%) - 4 (0,2%). Surdosage*. PROPRIÉTÉS PHARMACOLOGIQUES* : Propriétés pharmacodynamiques* : Classe
pharmaco-thérapeutique : Inhibiteur stéroïdien de l’aromatase. Agent antinéoplasique. Code ATC : L02BG06. Propriétés pharmacocinétiques*.
Données de sécurité précliniques*. DONNÉES PHARMACEUTIQUES*. PRÉSENTATION ET NUMÉRO D'IDENTIFICATION ADMINISTRATIVE : A.M.M.
352 796-6 : 30 comprimés sous plaquettes thermoformées (Aluminium-PVDC/PVC-PVDC). CONDITIONS DE PRESCRIPTION ET DE
DÉLIVRANCE : Liste I. Remb. Séc. Soc. 100 %, Agrée collect. L’indication « traitement adjuvant du cancer du sein invasif à
un stade précoce exprimant des récepteurs aux estrogènes, chez les femmes ménopausées, à la suite d’un traitement
adjuvant initial d’une durée de 2 à 3 ans par tamoxifène » : non remboursable et non agréé. Collect. à la date
du 13 décembre 2005. Prix : 144,24 �. PFIZER - 23-25, Av du Dr. Lannelongue - 75014 Paris.
Tél. (Standard) : 01.58.07.30.00 ; Tél. (Information Médicale) : 01.58.07.34.40. ®: marque
déposée. Date de révision d’AMM : 13 décembre 2005. * Pour plus d’informations,
se référer au Résumé des Caractéristiques du Produit. Version 002-12/05.
**Indication non remboursable à la date du 19/12/2005.
AROM_AP_21X27 1/09/06 10:24 Page 1
10. Fuhrman SA, Lasky LC, Limas C. Prognostic signifi cance of morphologic pa-
rameters in renal cell carcinoma. Am J Surg Pathol 1982;6:655-63.
11. Lang H, Lindner V, de Fromont M et al. Multicenter determination of op-
timal interobserver agreement using the Fuhrman grading system for renal cell
carcinoma: Assessment of 241 patients with > 15-year follow-up. Cancer 2005;
103:625-9.
12. Eble JN, Sauter G, Epstein JI, Sesterhenn IA. Pathology and genetics of tu-
mours of the urinary system and male genital organs. World Health Organiza-
tion Classifi cation of Tumours. Lyon, France: IARC Press 2004;7.
13. Cheville JC, Lohse CM, Zincke H et al. Comparisons of outcome and pro-
gnostic features among histologic subtypes of renal cell carcinoma. Am J Surg
Pathol 2003;27:612-24.
14. Patard JJ, Leray E, Rioux-Leclercq N et al. Prognostic value of histolo-
gic subtypes in renal cell carcinoma: a multicenter experience. J Clin Oncol
2005;23:2763-71.
15. Delahunt B, Eble JN, McCredie MR et al. Morphologic typing of papillary
renal cell carcinoma: comparison of growth kinetics and patient survival in 66
cases. Hum Pathol 2001;32:590-5.
16. Patard JJ, Leray E, Cindolo L et al. Multi-institutional validation of a symp-
tom based classifi cation for renal cell carcinoma. J Urol 2004;172:858-62.
17. Lam JS, Shvarts O, Leppert JT et al. Renal cell carcinoma 2005: new fron-
tiers in staging, prognostication and targeted molecular therapy. J Urol 2005;
173:1853-62.
18. Kim HL, Seligson D, Liu X et al. Using protein expressions to predict survival
in clear cell renal carcinoma. Clin Cancer Res 2004;10:5464-71.
19. Kattan MW, Reuter V, Motzer RJ et al. A postoperative prognostic nomo-
gram for renal cell carcinoma. J Urol 2001;166:63-7.
20. Cindolo L, Patard JJ, Chiodini P et al. Comparison of predictive accuracy
of four prognostic models for nonmetastatic renal cell carcinoma after nephrec-
tomy: a multicenter European study. Cancer 2005;104:1362-71.
21. Zisman A, Pantuck AJ, Wieder J et al. Risk group assessment and clinical
outcome algorithm to predict the natural history of patients with surgically
resected renal cell carcinoma. J Clin Oncol 2002;20: 4559-66.
22. Patard JJ, Kim HL, Lam JS et al. Use of the University of California
Los Angeles integrated staging system to predict survival in renal cell
carcinoma: an international multicenter study. J Clin Oncol 2004;22: 3316-22.
23. Ficarra V, Martignoni G, Lohse C et al. External validation of the Mayo
Clinic Stage, size, grade and necrosis (SSIGN) score to predict cancer specifi c
survival using a European series of conventional Renal Cell Carcinoma. J Urol
2006;175:1235-9.
24. Negrier S, Escudier B, Gomez F et al. Prognostic factors of survival and
rapid progression in 782 patients with metastatic renal carcinomas treated by
cytokines: a report from the Groupe Francais d’Immunothérapie. Ann Oncol
2002;13:1460-8.
25. Motzer RJ, Mazumdar M, Bacik J et al. Survival and prognostic stratifi cation of
670 patients with advanced renal cell carcinoma. J Clin Oncol 1999;17:2530-40.
26. Mekhail TM, Abou-Jawde RM, Boumerhi G et al. Validation and exten-
sion of the Memorial Sloan-Kettering prognostic factors model for survival in
patients with previously untreated metastatic renal cell carcinoma. J Clin Oncol
2005;23:832-41.
27. Motzer RJ, Rini BI, Bukowski RM et al. Sunitinib in patients with metastatic
renal cell carcinoma. JAMA 2006;295:2516-24.
28. Upton MP, Parker RA, Youmans A et al. Histologic predictors of renal
cell carcinoma response to interleukin-2-based therapy. J Immunother 2005;
28:488-95.
29. Atkins M, Regan M, McDermott D et al. Carbonic anhydrase IX expres-
sion predicts outcome of interleukin 2 therapy for renal cancer. Clin Cancer Res
2005;11:3714-21.
30. Leppert JT, Pantuck AJ. Signifi cance of gene expression analysis of renal cell
carcinoma. Expert Rev Anticancer er 2006;6:293-9.
Université René-Descartes, Paris-V,
et université Pierre-et-Marie-Curie,
Paris-VI
Diplôme interuniversitaire
d’hématologie
et de cancérologie du sujet âgé
Pr. Olivier Saint-Jean (hôpital Geor-
ges-Pompidou, 75015 Paris)
Pr Véronique Lebond (hôpital de la
Pitié-Salpêtrière, 75013 Paris)
Pr. Jean-Pierre Lotz (hôpital Tenon,
75020 Paris)
L’enseignement effectué sur un an
comporte une partie théorique de
100 heures, à raison de trois séminaires
thématiques (gériatrie, hématologie
maligne, oncologie) ; il portera sur les
aspects spécifiques du vieillissement
normal et pathologique, des cancers
chez les patients âgés et des hémopa-
thies malignes chez les malades âgés.
La validation des études se fait par un
examen écrit et par la rédaction d’un
mémoire.
Les dates retenues pour l’année univer-
sitaire 2006-2007 sont les suivantes :
✓ pour la partie gériatrie :
22-24/11 et 13-15/12/06
✓ pour la partie oncologie :
10-12/01 et 14-16/02/07
✓ pour la partie hémato :
15-16/03 et 03-04/05/07
Les inscriptions sont programmées en
septembre-octobre 2006, au niveau des
deux universités :
✓ service des spécialités médicales,
faculté de médecine Necker - Enfants
Malades, 156, rue de Vaugirard, 75015
Paris. Tél. : 01 40 61 56 00 ou 56 01.
✓ service scolarité troisième cycle,
faculté de médecine Saint-Antoine
- 27, rue Chaligny, 75012 Paris - Tél. :
01 40 01 14 49.
Les documents administratifs (CV, photo-
copies du Diplôme de Docteur en Méde-
cine s’il a été obtenu à l’étranger, lettre
de motivation, photo d’identité, trois
enveloppes timbrées libellées au nom et
à l’adresse) sont à adresser au secrétariat
de l’enseignement du Professeur Olivier
Saint-Jean - hôpital européen Georges-
Pompidou - 20, rue Leblanc - 75015 Paris,
du Professeur Véronique Leblond, service
d’Hématologie - hôpital de la Pitié-Salpê-
trière - boulevard de l’Hôpital - 75013 Paris,
et du Professeur Jean-Pierre Lotz - service
d’Oncologie médicale - hôpital Tenon - 4,
rue de la Chine - 75970 Paris Cedex 20.
Les informations sont disponibles sur
les sites suivants :
http://www.univ-paris5.fr et
http://www.hegp-geriatrie.fr/
pour Paris-V
http://www2.upmc.fr/fc/diumed_
hemato_cancero_age.pdf
pour Paris-VI
Agenda
1
/
5
100%